
分析 (1)赤铁矿炼铁是工业上利用一氧化碳进行还原制取.
(2)铁生锈的条件是与氧气和水接触;
(3)考虑铁锈的主要成分是氧化铁,氧化铁和稀硫酸反应生成硫酸铁和水;
(4)根据金属活动性顺序表及其应用分析,氢前的金属能与酸反应生成氢气,位置在前的金属能将位于其后的金属从其盐溶液中置换出来.
解答 (1)一氧化碳具有还原性,能把铁从它的氧化物中还原出来,该反应是:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2
故填Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2
(2)普通钢板在空气中锈蚀,实际上是铁跟空气中的氧气和水共同作用的结果;
(3)稀硫酸去除铁锈的化学反应方程式为:Fe2O3+3H2SO4═Fe2(SO4)3+3H2O;
(4)由金属活动性顺序表及其应用可知,运用稀盐酸首先可验证镁比铁活泼,镁、铁比铜、银活泼.因为稀盐酸和铁镁能反应生成氢气,而铜银与稀盐酸不反应不产生氢气,且镁比铁产生氢气的速度快.但不能验证铜和银的金属活动性.利用金属活动顺序表中前面的金属能把后面的金属从它的化合物的溶液中置换出来,可用硝酸银溶液来比较铜银的活动性.
故答案为:
(1)Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.(2)氧气和水.
(3)Fe2O3+3H2SO4═Fe2(SO4)3+3H2O.(4)硝酸银溶液.
点评 本题主要考查了炼铁的反应原理、铁生锈条件、金属资源保护及对金属活动性顺序的实验探究,培养了学生对知识的灵活应用,考查学生分析问题的能力.


科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
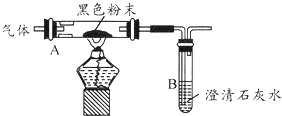 类比法是化学研究物质的重要方法之一.草酸(H2C2O4)的化学性质与碳酸相似.已知碳酸易分解,草酸在受热条件下也分解,仅生成三种氧化物.某校研究性学习小组对此展开探究:
类比法是化学研究物质的重要方法之一.草酸(H2C2O4)的化学性质与碳酸相似.已知碳酸易分解,草酸在受热条件下也分解,仅生成三种氧化物.某校研究性学习小组对此展开探究:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 原子不能再分 | |
| B. | 原子核都是由质子和中子构成的 | |
| C. | 原子可以构成分子,也可以直接构成物质 | |
| D. | 相对原子质量只是一个比,没有单位 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com