
【题目】某化学兴趣小组有一次活动的内容是:对一包干燥的红色粉末组成进行探究。请你参与并回答有关问题。
【教师提醒】:它由Cu、Fe2O3、Fe(OH)3三种固体中的一种或两种组成。
【提出猜想:】红色粉末可能的组成有: ①只有Cu;②只有Fe2O3;③只有Fe(OH)3;④是Fe2O3、Fe(OH)3的混合物;⑤是Cu、Fe2O3的混合物;⑥是Cu、Fe(OH)3的混合物。
【资料获悉】:
(1)氢氧化铁受热分解为氧化铁和水。(2)白色无水硫酸铜遇水变蓝。
(3)氧化铁可以和稀盐酸反应生成氯化铁和水。
(4)铜在黄色氯化铁溶液中可以发生反应生成氯化亚铁和氯化铜。
【探究思路】:利用物质的性质不同设计实验加以甄别,先分别探究其中是否含有Fe(OH)3, Cu等,逐步缩小范围,然后再选择适当的试剂和方法通过实验探究其组成。 (装置内空气中的水蒸气、二氧化碳忽略不计)
【实验探究】:
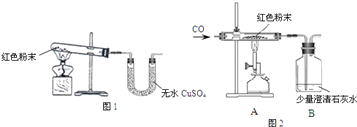
(1)甲同学取适量红色粉末装入试管中,按图1进行实验。结果无水硫酸铜没有变蓝,从而排除猜想中的_________。(填猜想中的序号)
(2)在甲同学实验结论的基础上,乙同学另取少量红色粉末于试管中,滴加足量稀盐酸,振荡后观察,发现固体全部溶解,溶液变色。乙同学认为可以排除猜想中的①和⑤,而丙同学认为只能排除猜想①,你认为_________的观点正确(填"乙"或"丙")。
(3)丁同学为进一步确定红色粉末的组成,称取5.0g该粉末装入硬质玻璃管中,按图2在通风橱中进行实验.开始时缓缓通入CO气体,过一段时间后再加热使其充分反应。待反应完全后,停止加热,仍继续通CO气体直至玻璃管冷却。反应前后称量相关装置和物质的总质量,其数据如下表:
组别 | 反应前 | 反应后 |
Ⅰ组 | 玻璃管和红色粉末总质量为37.3g | 玻璃管和固体物质总质量为36.1g |
Ⅱ组 | 洗气瓶和所盛溶液总质量为180.0g | 洗气瓶和物质总质量为183.1g |
【交流讨论】:
(1)在装置中先通CO气体的作用是________。
(2)应该选择_________组的实验数据计算来确定红色粉末的组成。最终计算结果表明:该红色粉末的组成是猜想中的第_________组(填序号)。
(3)实验中观察到A装置中的现象为___________。
(4)为了防止溶液倒吸,本实验停止加热前是否需要先断开A和B的连接处?_______(填"需要"或"不需要"),理由是________。
【反思评价】:从环保角度,图二缺少尾气处理装置。
【答案】 346 丙 排尽装置中空气,防止爆炸。 Ⅰ 5 部分红色粉末变黑 不需要 实验结束后,一直在通一氧化碳
【解析】本题主要对炼铁的实验原理、实验现象、操作步骤、装置连接及实验分析与评价等方面进行考查。熟练掌握该实验的反应原理以及实验注意事项是解决此类问题的关键。
实验探究:
(1)根据提供的资料:氢氧化铁受热分解为氧化铁和水,白色无水硫酸铜遇水变蓝。加热红色粉末,结果无水CuSO4没有变蓝,从而排除猜想中的含有Fe(OH)3的选项③④⑥;
(2)取红色粉末于试管中,滴加足量稀盐酸,振荡后观察,发现固体全部溶解,溶液变色;铜不能与稀盐酸反应,可推断排除猜想中的①,氧化铁能与稀盐酸反应生成氯化铁和水,根据提供的资料:铜在黄色氯化铁溶液中可以发生反应生成氯化亚铁和氯化铜;红色粉末可能是Fe2O3或Cu、Fe2O3的混合物,不能排除⑤;所以说同学的观点正确;
交流讨论:
(1)CO具有可燃性,与玻璃管中的空气混合受热会发生爆炸,因此,应先通CO排尽玻璃管中的空气,然后再加热。所以在装置A中先通CO气体的作用是:排尽装置中空气,防止爆炸;
(2)Ⅱ组实验使用的是石灰水吸收二氧化碳,吸收的不够完全使实验数据不准确,应该使用Ⅰ组数据进行确定;
设:粉末中氧化铁的质量为x
3CO+Fe2O3![]() 2Fe+3CO2 固体△m
2Fe+3CO2 固体△m
160 112 160-112=48
x 37.3g-36.1g=1.2g
![]() x=4g,粉末共有5g,氧化铁4g,所以含有铜粉;该红色粉末的组成是猜想中的第⑤组;
x=4g,粉末共有5g,氧化铁4g,所以含有铜粉;该红色粉末的组成是猜想中的第⑤组;
(3)A装置中发生反应的化学方程式为:3CO+Fe2O3![]() 2Fe+3CO2;红色粉末是Cu、Fe2O3的混合物,因此实验中观察到A装置中的现象为:部分红色粉末变黑;
2Fe+3CO2;红色粉末是Cu、Fe2O3的混合物,因此实验中观察到A装置中的现象为:部分红色粉末变黑;
(4)实验结束后,一直在通一氧化碳直至冷却,B中溶液不会倒吸到A装置中,不需要先断开A和B的连接处。


科目:初中化学 来源: 题型:
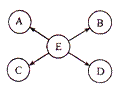
【题目】如图所示是几种常见物质的转化关系,→指示方向的物质为生成物,其中A、B组成元素相同的氧化物,A为黑色固体,B为红棕色固体,D是密度最小的气体,C、E是金属单质。(部分反应物、生成物及反应条件已略去)
(1)E的化学式为_____。
(2)写出E→D转化的化学方程式_____。
(3)E与某化合物溶液反应可得到C,则E和C的金属活动性强弱顺序为_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
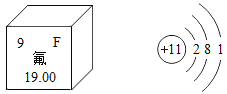
【题目】氟化钠是某些牙膏的添加剂,能有效预防龋齿,如图是氟元素在元素周期表中的相关信息及钠原子结构示意图,则氟原子的核外电子数是_______,钠原子在化学反应中易______(填“得”或“失”)电子,氟化钠可以用钠与氟气(F2)反应制得,反应的化学方程式是_______________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】向一定量稀硫酸中加入一定量铜粉,无气泡冒出;用导管向稀硫酸中通入空气并加热,铜粉逐渐减少,溶液由无色变为蓝色。测得溶液质量与实验时间的关系如下图。下列说法错误的是( )
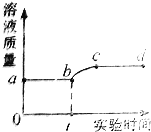
A.ab段说明Cu不能转换出硫酸中的氢
B.从b点到c点,溶液的PH逐渐增大
C.从c点到d点,溶液中的溶质只可能有一种
D.bc段发生的反应为2Cu+2H2SO4+O2 △ 2CuSO4+2H2O
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】镁将成为21世纪重要的轻型环保材料,我国含有丰富的镁资源,从海水中提取镁的流程如下:
![]()
(1)在实验室进行蒸发操作时需要用到玻璃棒,其作用是______;
(2)电解熔融氯化镁的过程中,_____能转化为______能;
(3)Mg(OH)2与盐酸的反应属于______反应(填化学反应的基本类型);
(3)用一个化学反应可以证明镁比铜活动性强,该反应的化学方程式是_________.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】白云石粉是一种生产高级玻璃器皿、医药用瓶、光学玻璃的原料,某化学兴趣小组对白云石粉极其好奇,决定对其进行探究。
【查阅资料】
白云石属于碳酸盐矿物,白云石粉主要成分的化学式可表示为xMgCO3·yCaCO3 ( 杂质是二氧化硅,其不溶于水,也不与盐酸反应,受热不分解)
一、定性探究:白云石粉的成分和性质
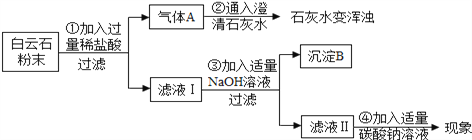
【实验分析】
(1)由步骤①②的现象可得出白云石粉中一定含有的离子是_________ (填离子符号)。
(2)步骤③生成氢氧化镁的化学方程式是________;步骤④的反应现象是_______。
【结论】综合上述实验现象可初步证明白云石由碳酸钙、碳酸镁组成。
【实验质疑】小组同学经过讨论认为:因氢氧化钙微溶于水,导致沉淀B中除了氢氧化镁之外应该还混有氢氧化钙,对定量测定白云石粉的组成干扰较大,在老师的指导下该兴趣小组采用热分解法进行定量探究。
二、定量探究:白云石的组成
【查阅资料】碳酸钙开始分解的温度为898℃,1000℃时完全分解生成生石灰和二氧化碳气体;碳酸钙与碳酸镁的化学性质相似;碳酸镁开始分解的温度为540℃,700℃时完全分解。
【实验设计】为测定白云石中的含钙量及x:y的值,该兴趣小组设计了如下装置并进行实验:

【实验步骤】
①组装仪器,检查装置的气密性;
②准确称取15.0g 白云石粉末放在A装置中,打开弹簧夹,鼓入一段时间氮气,称量B、C、D、E装置的质量;
③关闭弹簧夹,打开控温电加热器,缓缓调升温度至700℃,持续加热至固体质量不变;
④打开弹簧夹,缓缓鼓入一段时间氮气,准确称量B、C、D、E装置的质量;
⑤关闭弹簧夹,调升温度至1000℃,持续加热至固体质量不变,打开弹簧夹,缓缓鼓入一段时间氮气,准确称量B、C、D、E装置的质量。
实验数据记录如表:
B中溶液质量/g | C中溶液质量/g | D中溶液质量/g | E的质量/g | |
反应前 | 50.0 | 100.0 | 50.0 | 120.5 |
700℃ | 50.0 | 102.1 | 50.1 | 120.5 |
1000℃ | 50.0 | 106.3 | 50.3 | 120.5 |
【实验分析和数据处理】
(3)装置D的作用是______________________。
(4)持续加热至固体质量不变后缓缓鼓入一段时间氮气的目的是__________。
(5)计算白云石中钙元素的质量分数______。(写出计算过程,结果保留小数点后一位,)
(6)设计实验证明白云石粉已完全分解的实验方法是 ______(写出实验方法、现象、结论)
(7)白云石(xMgCO3·yCaCO3)中的 x:y=________ (最简整数比),若加热前没有鼓入一段时间的氮气,将会导致 x:y的值___________(填偏大、偏小或不变).
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】通过一年的化学学习,相信你已经初步掌握了实验室制取气体的有关知识。请结合图示回答问题。

(1)写出图中标示的仪器名称:②__________。
(2)实验室用KMnO4制取O2,可以选用的装置组合为_____(填字母序号,下同),取用KMnO4药品时,应选用仪器_____,该反应的化学方程式为______________。
(3)注射器C可用于检查装置E的气密性,步骤如下:
①向锥形瓶中加入少量水至_____________处。
②将注射器C连接到装置E的导管口处。
③缓慢向外拉动注射器C的活塞,观察到___________,表示装置E的气密性良好。
(4)某兴趣小组的同学利用下图装置研究二氧化碳的性质。(仪器的固定装置已经省略)
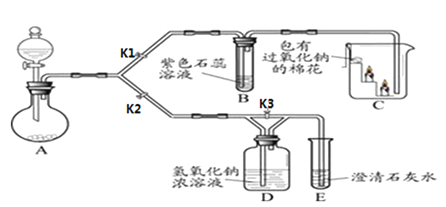
①A装置用于实验室制取二氧化碳,其反应的化学方程式为_____________________。
②实验开始后,关闭K2、打开K1,可观察到B中现象为___________________;C中的蜡烛由下至上依次熄灭,说明二氧化碳具有的性质是___________________;待蜡烛熄灭后,铁片上的棉花剧烈燃烧起来,由此可得到的推论是_____________。
③实验开始后,关闭K1和K3,打开K2,观察到E中的现象是_____________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】称取NaCl和BaCl2的固体混合物32.5g,加入100g蒸馏水,完全溶解后向该混合溶液中逐滴加入 90.8gNa2SO4溶液后恰好不再产生沉淀,反应生成BaSO4沉淀的质量与反应时间关系如下图所示。试回答下列问题:
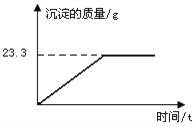
(1)完全反应后生成BaSO4沉淀。
(2)求反应后溶液中溶质的质量分数。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图是四种物质的溶解度曲线图。
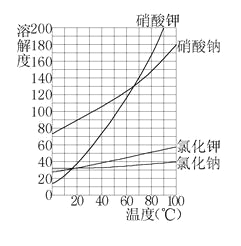
①溶解度的单位是______。
②由图可知 10℃时,溶解性最好的是____。
③50g 水中投入 75g 硝酸钠固体得到饱和溶液, 此时,实验溶液温度为 _______℃。
④四个烧杯中分别放入硝酸钾、硝酸钠、氯化钾氯化钠各 10g,然后加入水都完全溶解得到 50℃ 时饱和溶液。则最后得到饱和溶液质量最多的是________(选填下列编号)。 A.硝酸钾 B.硝酸钠 C.氯化钾 D.氯化钠
⑤有一包固体混合物,可能由硝酸钾和氯化钾中的一种或二种构成。现取混合物 40g,加入50g 50℃的热水(水温保持不变),固体完全溶解。对该包固体的主要成分判断正确的是_____(选填下列编号)。
A.一定是硝酸钾和氯化钾的混合物 B.可能只有氯化钾
C.可能是硝酸钾和氯化钾的混合物 D.一定只有硝酸钾
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com