
【题目】某溶液由NaOH、HCl、H2SO4和MgCl2中的一种或几种组成。向该溶液中滴加Ba(OH)2 溶液,产生沉淀的质量与加入Ba(OH)2 溶液体积的关系如图所示。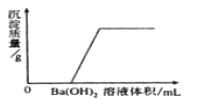
请你从图中获得的信息来分析,该溶液中不可能存在的物质是;写出产生沉淀的化学方程式是。
【答案】H2SO4和NaOH;MgCl2+ Ba(OH)2=Mg(OH)2↓+ BaCl2
【解析】硫酸根离子和钡离子只要接触就会生成硫酸钡沉淀,而沉淀的起点不是从零开始,所以一定没有硫酸,沉淀从x轴的某一点开始,说明了开始部分在发生中和反应,一定有盐酸和氯化镁,有盐酸和氯化镁就不含有氢氧化钠,则一定存在的是HCl、MgCl2 , 一定不存在的是NaOH、H2SO4 , 滴加氢氧化钡溶液生成的沉淀为氢氧化镁,发生反应的化学方程式为:MgCl2+ Ba(OH)2=Mg(OH)2↓+ BaCl2。
故答案为:(1)H2SO4和NaOH(2)MgCl2+ Ba(OH)2=Mg(OH)2↓+ BaCl2从图像上看刚加入氢氧化钡没有沉淀,可得出原混合液中有硫酸,同时可以获知原溶液显酸性,因此必含有盐酸,后又有沉淀,说明原溶液中有氯化铜,进而可以排除氢氧化钠


 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:
【题目】某物质X与O2发生反应的化学方程式是:X+3O2 ![]() 2CO2+2H2O。下列说法中错误的是( )
2CO2+2H2O。下列说法中错误的是( )
A.X的化学式为C2H4
B.X具有可燃性
C.该反应为置换反应
D.X是一种有机物
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图表示X、Y、Z三种物质的溶解度曲线,下列说法错误的是( )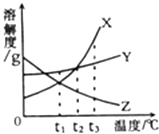
A.Y中含有少量X,用海水晒盐的原理提纯Y
B.t1℃时,三种物质的饱和溶液升温到t2℃,溶液中溶质质量分数的大小关系是Y>X>Z
C.t3℃时,X、Y的饱和溶液降温到t2℃,析出晶体较多的是X
D.t3℃时,等质量的X、Y分别配成该温度下的饱和溶液,所得溶液质量X<Y
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com