
【题目】同学们做甲、乙两个中和反应实验的探究。
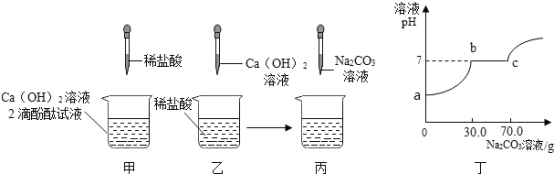
(1)甲实验恰好中和,则该溶液中的溶质是___________________(填化学式)。
(2)取乙反应后的溶液![]() ,滴加质量分数为
,滴加质量分数为![]() 的
的![]() 溶液(见图丙),溶液
溶液(见图丙),溶液![]() 的变化如图3-4-7所示。则与
的变化如图3-4-7所示。则与![]() 反应的碳酸钠溶液的质量为__________
反应的碳酸钠溶液的质量为__________![]() ;请计算该溶液中
;请计算该溶液中![]() 的质量分数_________(写出计算过程,精确到
的质量分数_________(写出计算过程,精确到![]() )。
)。
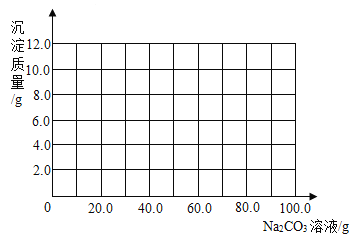
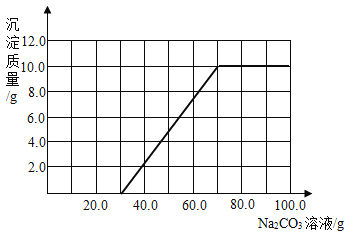
(3)根据计算所得数据在下图中画出产生沉淀的曲线_________。
(4)乙组的中和反应实验设计存在的不足是_______________
【答案】![]()
![]()
![]() 。
。  无法判断是否恰好反应
无法判断是否恰好反应
【解析】
(1)稀盐酸与![]() 溶液恰好完全中和,反应生成
溶液恰好完全中和,反应生成![]() 和
和![]() ,故溶液中的溶质是
,故溶液中的溶质是![]() 。
。
(2)从题图3-4-7中可知刚开始滴入的碳酸钠溶液先与乙中过量的盐酸反应,溶液的![]() 逐渐增大,当溶液的
逐渐增大,当溶液的![]() 刚达到
刚达到![]() 时,盐酸恰好全部反应完,此时消耗碳酸钠溶液
时,盐酸恰好全部反应完,此时消耗碳酸钠溶液![]() ;继续滴入碳酸钠溶液,碳酸钠再与
;继续滴入碳酸钠溶液,碳酸钠再与![]() 溶液反应,因反应生成
溶液反应,因反应生成![]() 沉淀和
沉淀和![]() ,溶液的
,溶液的![]() 保持不变,当
保持不变,当![]() 恰好完全反应时,此时消耗碳酸钠溶液的总质量为
恰好完全反应时,此时消耗碳酸钠溶液的总质量为![]() ;继续滴入碳酸钠溶液,因碳酸钠溶液呈碱性,溶液的
;继续滴入碳酸钠溶液,因碳酸钠溶液呈碱性,溶液的![]() 且
且![]() 逐渐增大。因此与
逐渐增大。因此与![]() 溶液反应的碳酸钠溶液的质量
溶液反应的碳酸钠溶液的质量![]() ,
,![]() 碳酸钠溶液中溶质的质量
碳酸钠溶液中溶质的质量![]() ,根据化学方程式,由碳酸钠的质量可求出
,根据化学方程式,由碳酸钠的质量可求出![]() 的质量,因所取乙溶液的质量为
的质量,因所取乙溶液的质量为![]() ,根据计算公式:溶质质量分数
,根据计算公式:溶质质量分数![]() ,可求出溶液中
,可求出溶液中![]() 的质量分数,
的质量分数,
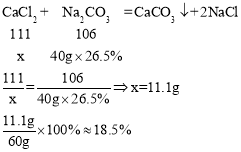
故该溶液中![]() 的质量分数是18.5%。
的质量分数是18.5%。
故填:40.0g;18.5%。
(3)当滴入碳酸钠溶液的质量为![]() 时,溶液开始产生沉淀;随着碳酸钠溶液的不断滴入,沉淀质量逐渐增多;当滴入的碳酸钠溶液的总质量为
时,溶液开始产生沉淀;随着碳酸钠溶液的不断滴入,沉淀质量逐渐增多;当滴入的碳酸钠溶液的总质量为![]() 是,沉淀达到最大量,可根据化学方程式
是,沉淀达到最大量,可根据化学方程式![]() ,由
,由![]() 碳酸钠可求出生成
碳酸钠可求出生成![]() 沉淀的最大量
沉淀的最大量![]() ;当
;当![]() 全部反应后,再继续滴入碳酸钠溶液,沉淀质量不再增加。根据沉淀质量随所滴入碳酸钠溶液质量的变化情况可画出曲线。
全部反应后,再继续滴入碳酸钠溶液,沉淀质量不再增加。根据沉淀质量随所滴入碳酸钠溶液质量的变化情况可画出曲线。

(4)乙中稀盐酸与![]() 溶液反应无明显现象,也未加指示剂,无法判断是否恰好反应。
溶液反应无明显现象,也未加指示剂,无法判断是否恰好反应。


 教材全解字词句篇系列答案
教材全解字词句篇系列答案科目:初中化学 来源: 题型:
【题目】如下图所示,将①中液体滴入②中与固体混合,观察到气球逐渐变大。则下表中液体①与固体②的组合,不符合题意的是
选项 | A | B | C | D |
|
① | 稀盐酸 | 水 | 水 | 氢氧化钠溶液 | |
② | 铁粉 | 生石灰 | 硝酸铵 | 氯化铵 |
A.AB.BC.CD.D
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是汽车尾气中有毒气体转变为无毒气体的微观示意图,图中不同的圆球代表不同原子。下列说法错误的是
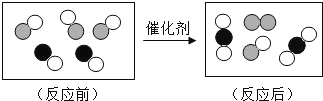
A.反应前后原子的种类、数目均无变化
B.此反应不属于置换反应
C.反应中有单质生成
D.参加反应的两种分子的个数比为 3:2
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】以白云石(主要成分化学式为 MgCO3CaCO3)为原料制备氢氧化镁的工艺流程如下图(流程图方框中的文字均表示操作过程):
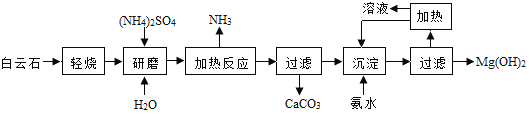
(1)白云石属于________物(选填“混合”“纯净”),白云石“轻烧”过程中只发生了碳酸镁的分解,写出碳酸镁分解反应的化学方程式________________。
(2)流程图中“加热反应”是指硫酸铵与氧化镁在加热条件下反应生成一种盐、氨气和水,其化学方程式为____________________; 流程图中“沉淀”过程是指氨水和硫酸镁发生复分解反应,其化学方程式为_________________; 硫酸铵中氮元素的化合价是_________价。
(3)该工艺中可以循环使用的物质是_______________、(NH4)2SO4 等.
(4)传统制备氢氧化镁的工艺是将白云石高温下分解为氧化镁和氧化钙后再提取,而本工艺流程采用轻烧白云石的方法,其优点是______________(填写一条,合理即可).
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】我国科学家侯德榜,在氨碱法的基础上,创立了更为先进的联合制碱法生产纯碱碳 酸钠。某海边工厂利用贝壳、海盐等生产纯碱的主要工艺流程如下:
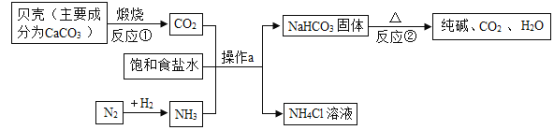
(1)反应①的化学方程式为_____。反应②属于_____反应(填基本反应类型)。
(2)工业上常用_____的方法制取氮气,该过程属于_____变化。
(3)操作 a 的名称是_____,实验室在进行该操作时,用到的玻璃仪器有烧杯、漏斗和_____。
(4)在工农业生产过程中,会排放 CO2 加剧温室效应。下列做法能减少二氧化碳排放的是_____(填序号)。
a 焚烧秸秆肥田 b 提高火力发电量 c 大力使用清洁能源
(5)有一种处理 CO2 的方法,是将 CO2 与氢气在一定条件下反应生成甲烷和水,该反应的化学方程式 为:_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学反应的微观过程用图表示.则下列说法中,正确的是( )
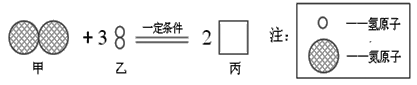
A. 该反应中分子和原子的种类都发生了改变
B. 物质丙的化学式为NH3
C. 甲、乙两物质参加反应的质量比为1:3
D. 图示反应属于分解反应
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】学习小组测定某工业废水中 H2SO4的含量。取 100g 废水于烧杯中,加入200gBaCl2 溶液,恰好完全反应,经过滤得到 253.4g 溶液(H2SO4 + BaCl2 = BaSO4 ↓+2HCl)(可溶性杂质不参加反应,过滤后滤液的损失忽略不计)
(1)充分反应后生成沉淀的质量为______g;
(2)该工业废水中硫酸的质量分数为____________?(写出计算过程)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室有一瓶失去标签的溶液,知道只含有一种阳离子钾离子,为了弄清其到底含有几种溶质(都是初中常见的物质),四九芳华小组做了如下实验:(不考虑微溶和碳酸氢根)
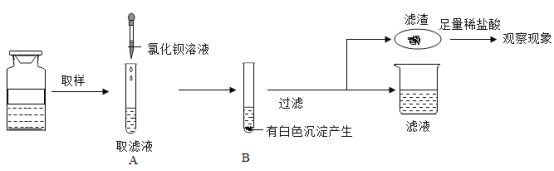
根据上述实验过程:小四同学根据滤渣处产生的_____________现象,从而确定了一定含有的两种溶质为___________,写出此过程反应的化学方程式:________。
还有那些溶质呢?小九同学继续探究如下图:
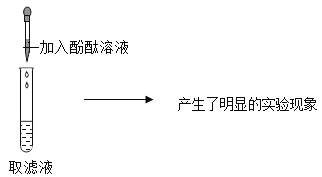
得出结论:该溶液一定含有氢氧化钾,请你对其结论进行评价_________;四九芳华小组经过讨论,觉得上述过程所加的试剂有一处不够明确和准确,从而对后续其他溶质的确定带来了影响,决定对一种试剂稍作调整,其他不变,调整为__________________,然后重新取滤液加入________,立即向所得溶液中加入__________,从而可推出瓶中溶液的溶质最多有__________种。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据如图所示实验,Y 烧杯中溶液由红色变为无色。
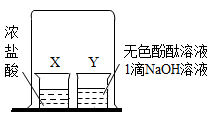
(1)该实验可证明分子具有的性质是__________。
(2)请用化学方程式表示红色变为无色的原因:_____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com