
”¾ĢāÄæ”æij»ÆѧĢ½¾æŠ”×éŅŌ”°Ń°ÕŅ¹żŃõ»ÆĒā·Ö½āŠĀµÄ“߻ƼĮ”±ĪŖæĪĢā£¬æŖÕ¹ĮĖĻĀĮŠŹµŃ锣
£ØĢį³öĪŹĢā£©Ńõ»ÆĢśÄÜ·ń×÷¹żŃõ»ÆĒāČÜŅŗ·Ö½āµÄ“߻ƼĮ£æČē¹ūÄÜ£¬Ęä“߻Ɗ§¹ūČēŗĪ£æ
£Ø²ĀĻėÓė¼ŁÉč£©_____”£
£ØŹµŃéĢ½¾æ£©
ŹµŃé²½Öč | ŹµŃéĻÖĻó | ŹµŃé½įĀŪ |
¢ń£®·Ö±šĮæČ”5mL 5%¹żŃõ»ÆĒāČÜŅŗ·ÅČėA”¢B Į½Ö§ŹŌ¹ÜÖŠ£¬ĻņAŹŌ¹ÜÖŠ¼ÓČėa gŃõ»ÆĢś·ŪÄ©£¬²¢·Ö±šŌŚA”¢BĮ½Ö§ŹŌ¹ÜÖŠ²åČė“ų»šŠĒľĢõ£¬¹Ū²ģĻÖĻó”£ | AŹŌ¹ÜÖŠ²śÉś½Ļ¶ąĘųÅŻ£¬“ų»šŠĒľĢõ_____£¬BŹŌ¹ÜÖŠĪŽĆ÷ĻŌĻÖĻó | ¢ŁAŹŌ¹Ü²śÉśµÄĘųĢåŹĒ_____(Ģī»ÆѧŹ½)Ńõ»ÆĢśæɼÓæģ¹żŃõ»ÆĒāµÄ·Ö½āĖŁĀŹ |
¢ņ£®“żAŹŌ¹Ü֊ƻӊĻÖĻó·¢ÉśŹ±£¬ÖŲŠĀ¼ÓČė¹żŃõ»ÆĒāČÜŅŗ£¬²¢°Ń“ų»šŠĒµÄľĢõÉģČėŹŌ¹Ü£¬Čē“Ė·“ø“¶ą“ĪŹŌŃ飬¹Ū²ģĻÖĻó”£ | ŹŌ¹ÜÖŠ¾ł²śÉśĘųÅŻ£¬“ų»šŠĒľĢõ¾łø“Č¼ | Ńõ»ÆĢśµÄ_____ŌŚ·“Ó¦Ē°ŗó¾łĆ»ÓŠ·¢Éś±ä»Æ”£ |
¢ó£®½«ŹµŃéIIÖŠµÄŹ£ÓąĪļ________(Ģī²Ł×÷Ćū³Ę)£¬²¢½«ĖłµĆĀĖŌü½ųŠŠĻ“µÓ”¢øÉŌļ”¢³ĘĮæ | ĖłµĆ¹ĢĢåÖŹĮæČŌĪŖa g | Ńõ»ÆĢśµÄ_____ŌŚ·“Ó¦Ē°ŗó¾łĆ»ÓŠ·¢Éś±ä»Æ”£ |
£ØŹµŃé½įĀŪ£©
(1)ŹµŃéII”¢IIIµĆ³ö½įĀŪ£ŗ_____”£
(2)ĒėŠ“³öŃõ»ÆĢś“߻ƹżŃõ»ÆĒāČÜŅŗ·Ö½āµÄ»Æѧ·½³ĢŹ½_____”£
£ØŹµŃéĶŲÕ¹£©
(3)²éŌÄ׏ĮĻµĆÖŖ£¬CuO”¢CuSO4”¢ÖķøĪ”¢ĀķĮåŹķµČŅ²æÉŅŌ×ö¹żŃõ»ÆĒāČÜŅŗ·Ö½āµÄ“߻ƼĮ”£ĻĀĮŠÓŠ¹Ų“߻ƼĮµÄĖµ·ØÖŠÕżČ·µÄŹĒ_____”£
A MnO2Ö»ÄÜ×÷¹żŃõ»ÆĒāČÜŅŗ·Ö½āµÄ“߻ƼĮ
B Ķ¬Ņ»øö»Æѧ·“Ó¦æÉŅŌÓŠ¶ąÖ֓߻ƼĮ
C “߻ƼĮÖ»ÄܼÓæģ»Æѧ·“Ó¦µÄĖŁĀŹ
D ÓĆ×÷“߻ƼĮµÄĪļÖŹ²»æÉÄÜŹĒĘäĖū·“Ó¦µÄ·“Ó¦Īļ»ņÉś³ÉĪļ”£
”¾“š°ø”æŃõ»ÆĢśæÉ×÷¹żŃõ»ÆĒā·Ö½āµÄ“߻ƼĮ£»(ŗĻĄķ¼“æÉ) ø“Č¼ O2 »ÆѧŠŌÖŹ ¹żĀĖ ÖŹĮæ Ńõ»ÆĢśŌŚ»Æѧ·“Ó¦Ē°ŗóµÄÖŹĮæŗĶ»ÆѧŠŌÖŹ²»±ä 2H2O2![]() 2H2O+O2”ü B
2H2O+O2ӟ B
”¾½āĪö”æ
[²ĀĻėÓė¼ŁÉč]Ńõ»ÆĢśæÉ(»ņ²»æÉ)×÷¹żŃõ»ÆĒā·Ö½āµÄ“߻ƼĮ£»¹Ź“š°øĪŖ£ŗŃõ»ÆĢśæÉ×÷¹żŃõ»ÆĒā·Ö½āµÄ“߻ƼĮ£»(ŗĻĄķ¼“æÉ)
[ŹµŃéĢ½¾æ]
¢ń£®·Ö±šĮæČ”5mL5%¹żŃõ»ÆĒāČÜŅŗ·ÅČėA”¢BĮ½Ö§ŹŌ¹ÜÖŠ£¬ĻņAŹŌ¹ÜÖŠ¼ÓČėagŃõ»ÆĢś·ŪÄ©£¬²¢·Ö±šŌŚA”¢BĮ½Ö§ŹŌ¹ÜÖŠ²åČė“ų»šŠĒľĢõ£¬¹Ū²ģĻÖĻó£»AŹŌ¹ÜÖŠ²śÉś½Ļ¶ąĘųÅŻ£¬“ų»šŠĒľĢõø“Č¼£¬BŹŌ¹ÜÖŠĪŽĆ÷ĻŌĻÖĻó£»AŹŌ¹Ü²śÉśµÄĘųĢåŹĒŃõĘų£¬Ńõ»ÆĢśæɼÓæģ¹żŃõ»ÆĒāµÄ·Ö½āĖŁĀŹ£»¢ņ£®“żAŹŌ¹Ü֊ƻӊĻÖĻó·¢ÉśŹ±£¬ÖŲŠĀ¼ÓČė¹żŃõ»ÆĒāČÜŅŗ£¬²¢°Ń“ų»šŠĒµÄľĢõÉģČėŹŌ¹Ü£¬Čē“Ė·“ø“¶ą“ĪŹŌŃ飬¹Ū²ģĻÖĻó£»ŹŌ¹ÜÖŠ¾ł²śÉśĘųÅŻ£¬“ų»šŠĒľĢõ¾łø“Č¼£»Ńõ»ÆĢśµÄ»ÆѧŠŌÖŹŌŚ·“Ó¦Ē°ŗó¾łĆ»ÓŠ·¢Éś±ä»Æ£»¢ó£®½«ŹµŃéIIÖŠµÄŹ£ÓąĪļ¹żĀĖ£¬²¢½«ĖłµĆĀĖŌü½ųŠŠĻ“µÓ”¢øÉŌļ”¢³ĘĮ棻ĖłµĆ¹ĢĢåÖŹĮæČŌĪŖag£»Ńõ»ÆĢśµÄÖŹĮæŌŚ·“Ó¦Ē°ŗó¾łĆ»ÓŠ·¢Éś±ä»Æ£»¹Ź“š°øĪŖ£ŗ¢ń”¢ø“Č¼£»O2£»¢ņ”¢»ÆѧŠŌÖŹ£»¢ó”¢¹żĀĖ£»ÖŹĮ棻
[ŹµŃé½įĀŪ]
(1)ŹµŃéII”¢IIIµĆ³ö½įĀŪ£ŗŃõ»ÆĢśŌŚ»Æѧ·“Ó¦Ē°ŗóµÄÖŹĮæŗĶ»ÆѧŠŌÖŹ²»±ä£»¹Ź“š°øĪŖ£ŗŃõ»ÆĢśŌŚ»Æѧ·“Ó¦Ē°ŗóµÄÖŹĮæŗĶ»ÆѧŠŌÖŹ²»±ä£»
(2)¹żŃõ»ÆĒāŌŚŃõ»ÆĢś×ö“߻ƼĮµÄĢõ¼žĻĀÉś³ÉĖ®ŗĶŃõĘų£¬ŅŖ×¢ŅāÅäĘ½£»¹Ź“š°øĪŖ£ŗ2H2O2![]() 2H2O+O2”ü£»
2H2O+O2”ü£»
[ŹµŃéĶŲÕ¹]
(3)²éŌÄ׏ĮĻµĆÖŖ£¬CuO”¢CuSO4”¢ÖķøĪ”¢ĀķĮåŹķµČŅ²æÉŅŌ×ö¹żŃõ»ÆĒāČÜŅŗ·Ö½āµÄ“߻ƼĮ”£ÓŠ¹Ų“߻ƼĮµÄĖµ·ØÖŠÕżČ·µÄŹĒ£ŗĶ¬Ņ»øö»Æѧ·“Ó¦æÉŅŌÓŠ¶ąÖ֓߻ƼĮ£»¹Ź“š°øĪŖ£ŗB
[µć¾¦]
øĆĢāĪŖæĘѧĢ½¾æĢā£¬Ģ½¾æÓ°Ļģ·“Ó¦ĖŁĀŹµÄŅņĖŲ£Ø“߻ƼĮ£©£»½āĢā¹Ų¼üŹĒĄĪ¼Ē“߻ƼĮµÄ”°Ņ»±ä£¬Į½²»±ä”±ĢŲÕ÷£¬¼“øıä»Æѧ·“Ó¦ĖŁĀŹ£¬µ«±¾ÉķµÄ»ÆѧŠŌÖŹŗĶÖŹĮæ²»±ä”£


 “ŗÓź½ĢÓżĶ¬²½×÷ĪÄĻµĮŠ“š°ø
“ŗÓź½ĢÓżĶ¬²½×÷ĪÄĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĀČ»ÆÄĘŹĒŅ»ÖÖÖŲŅŖµÄ׏Ō“£¬ŌŚŗ£Ė®ÖŠ“¢ĮæŗÜ·įø»”£»Ų“šĪŹĢā£ŗ
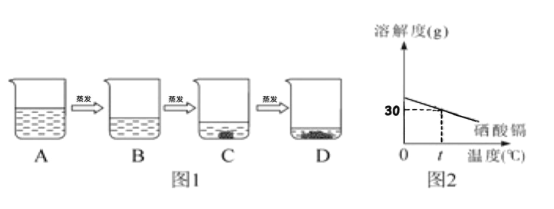
£Ø1£©ŗ£Ė®É¹ŃĪŹĒŗ£Ė®ŌŚ³£ĪĀĻĀÕō·¢µĆµ½ĀČ»ÆÄĘµÄ¹ż³Ģ, ÓĆĀČ»ÆÄĘČÜŅŗÄ£ÄāøĆ¹ż³Ģ (ČēĶ¼1ĖłŹ¾)”£ŅŃÖŖBČÜŅŗĒ”ŗĆŹĒĀČ»ÆÄʵı„ŗĶČÜŅŗ,ÓėBČÜŅŗÖŠČÜÖŹÖŹĮæĻąµČµÄČÜŅŗŹĒ___(Ģī×ÖÄøŠņŗÅ,ĻĀĶ¬)£¬ÓėBČÜŅŗÖŠČÜÖŹµÄÖŹĮæ·ÖŹżĻąµČµÄČÜŅŗŹĒ___.
£Ø2£©Ķ¼2ĪŖĪųĖįļÓµÄČܽā¶ČĒśĻß”£t ”ꏱ£¬½«15gĪųĖįļÓ¼ÓČė____gĖ®ÖŠ£¬ĶźČ«Čܽāŗó£¬Ē”ŗƵƵ½±„ŗĶČÜŅŗ”£ŅŖ½ųŅ»²½ĢįøßĪųĖįļÓČÜŅŗÖŠČÜÖŹµÄÖŹĮæ·ÖŹż£¬½ųŠŠµÄ²Ł×÷ŹĒ_________ ”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĶعżĻĀĮŠŹµŃéĻÖĻó£¬ÄÜĖµĆ÷ĒāŃõ»ÆÄĘÓėĻ”ĮņĖį·¢ÉśĮĖ»Æѧ·“Ó¦µÄŹĒ£Ø””””£©
A. ŌŚĻ”ĮņĖįÖŠ¼ÓČėŅ»¶ØĮæµÄĒāŃõ»ÆÄĘ¹ĢĢ壬ÓĆĪĀ¶Č¼Ę²āµĆČÜŅŗµÄĪĀ¶ČĻŌÖųÉżøß
B. ŌŚ![]() µÄĒāŃõ»ÆÄĘČÜŅŗÖŠ¼ÓČėŅ»¶ØĮæµÄĻ”ĮņĖį£¬ÓĆpH¼Ę²āµĆČÜŅŗµÄpHÖµ±äĪŖ8
µÄĒāŃõ»ÆÄĘČÜŅŗÖŠ¼ÓČėŅ»¶ØĮæµÄĻ”ĮņĖį£¬ÓĆpH¼Ę²āµĆČÜŅŗµÄpHÖµ±äĪŖ8
C. ŌŚĒāŃõ»ÆÄĘČÜŅŗÖŠĻȵĪ¼ÓĪŽÉ«·ÓĢŖ£¬ŌŁÖšµĪ¼ÓČėĻ”ĮņĖį£¬æ“µ½·ÓĢŖŗģÉ«Öš½„±äĒ³
D. ŌŚĒāŃõ»ÆÄĘČÜŅŗÖŠĻČ¼ÓČėŅ»¶ØĮæµÄĻ”ĮņĖį£¬ŌŁÖšµĪ¼ÓČėĮņĖįĶČÜŅŗ£¬ĪŽĆ÷ĻŌĻÖĻó
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æij¹¤³§²śÉśµÄÉÕŌü(Ö÷ŅŖŗ¬FeO”¢Fe2O3£¬»¹ÓŠŅ»¶ØĮæµÄSiO2)æÉÓĆÓŚÖʱøĘßĖ®ŗĻĮņĖįŃĒĢś¾§Ģå(FeSO4 ”¤7H2O)£¬Ę乤ŅÕĮ÷³ĢČēĻĀ£ŗ

²éŌÄ׏ĮĻ£ŗSiO2²»ČÜÓŚĖ®£¬Ņ²²»ÓėĻ”ĮņĖį·“Ó¦”£
¢Å ”°½žČ””±²½ÖčÖŠ£¬FeO”¢Fe2O3ŗĶĻ”ĮņĖį·¢Éś·“Ó¦µÄ»Æѧ·½³ĢŹ½·Ö±šĪŖFeO+H2SO4=FeSO4+H2O”¢__________________”£
¢Ę ¹żĀĖÓƵ½µÄ²£Į§ŅĒĘ÷ÓŠ______________”£
¢Ē ”°»¹Ō”±²½ÖčŹĒ½«Fe3+×Ŗ»ÆĪŖFe2+£¬ŹŌ¼ĮXæÉÓĆSO2»ņFe”£
¢Ł ČōŹŌ¼ĮXŹĒSO2£¬×Ŗ»ÆŌĄķĪŖSO2+Fe2(SO4)3+2H2O=2FeSO4+2Y£¬ŌņYµÄ»ÆѧŹ½ŹĒ£ŗ____________”£
¢Ś ČōŹŌ¼ĮXŹĒFe£¬×Ŗ»ÆŌĄķµÄ»Æѧ·½³ĢŹ½ĪŖ______________________”£
²āµĆ”°»¹Ō”±ŗóČÜŅŗµÄpHĆ÷ĻŌŌö“ó£¬ĘäŌŅņŹĒ______________________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÓĆ»ÆѧÓĆÓļĢīæÕ£ŗ
(1)2øöµŖŌ×Ó_____£»
(2)3øöļ§øłĄė×Ó_____£»
(3)±£³ÖĢśµÄ»ÆѧŠŌÖŹµÄ×īŠ”Ī¢Į£_____£»
(4)Ńõ»ÆĀĮÖŠĀĮŌŖĖŲµÄ»ÆŗĻ¼Ū_____£»
(5)¾ēĮŅČ¼ÉÕ£¬»šŠĒĖÄÉä£¬Éś³ÉŗŚÉ«¹ĢĢåµÄ»Æѧ·“Ó¦_____£»
(6)µē½āĖ®µÄ»Æѧ·“Ó¦_____”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĶ¼1±ķŹ¾¼×”¢ŅŅĮ½ÖÖ¾§ĢåµÄČܽā¶ČĒśĻß”£ t1”ꏱ£¬·Ö±š½«20g¼×”¢ŅŅĮ½ÖÖ¾§Ģå£Ø²»ŗ¬½į¾§Ė®£©¼ÓČėŹ¢ÓŠ100gĖ®µÄĮ½øöÉÕ±ÖŠ£¬Ē”ŗĆĶźČ«Čܽā£»ÉżĪĀµ½t2”ꏱ£¬¼×”¢ŅŅÉÕ±ÖŠ³öĻÖĶ¼2ĖłŹ¾µÄĻÖĻó”£ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ
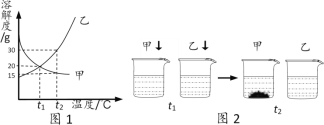
A. t2”ꏱÉÕ±ÖŠŅŅĪļÖŹŠĪ³ÉµÄČÜŅŗŹĒ²»±„ŗĶČÜŅŗ
B. t2”ꏱÉÕ±ÖŠ¼×ĪļÖŹČÜŅŗČÜÖŹÖŹĮæ·ÖŹżŌ¼ĪŖ15%
C. ±ŲŠė½µĪĀÖĮt1”ęŅŌĻĀ²ÅÄܽ«t2”ęÉÕ±ÖŠ¼×µÄČÜŅŗ×Ŗ±äĪŖ²»±„ŗĶČÜŅŗ
D. ½«t1”ꏱ¼×”¢ŅŅĮ½ĪļÖŹŠĪ³ÉµÄČÜŅŗÉżĪĀµ½t2”ꏱ£¬ĖłµĆČÜŅŗČÜÖŹÖŹĮæ·ÖŹż¼×£¼ŅŅ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĢś¼°Ęä»ÆŗĻĪļŌŚÉś²śÉś»īÖŠÓ¦ÓĆ¹ć·ŗ”£
£ØŅ»£©ĢśµÄŠŌÖŹŗĶÓ¦ÓĆ
£Ø1£©Ķ¼1ĪŖijŠ”¶łĮņĖįŃĒĢśĢĒ½¬”£
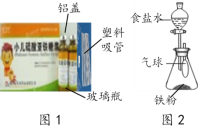
¢ŁŹŹµ±·žÓĆøĆĢĒ½¬æÉÖĪĮĘ______(Ń”ĢīŠņŗÅ£©”£
A ŲžŁĶ²” B ʶŃŖÖ¢ C ŁŖČåÖ¢
¢ŚĶ¼ÖŠ²»Éę¼°µ½µÄ²ÄĮĻŹĒ_______(Ń”ĢīŠņŗÅ£©”£
A ĪŽ»ś²ÄĮĻ B ŗĻ³É²ÄĮĻ C ø“ŗĻ²ÄĮĻ
£Ø2£©Ź³Ę·±£ĻŹ”°Ė«Īü¼Į”±ŗ¬Ģś·Ū”¢Ź³ŃĪµČ£¬Ķ¼2ĪŖĘäŌĄķĢ½¾æŹµŃé£ŗ
¢ŁµĪČėŹ³ŃĪĖ®ŗ󣬹Ų±Õ·ÖŅŗĀ©¶·»īČū”£Ņ»¶ĪŹ±¼äŗó£¬Ģś·ŪÉĻ³öĻÖŗģÉ«¹ĢĢ壬ĘųĒņ___£ØŃ”Ģī”°±ä“ó”±”¢”°²»±ä”±»ņ”°±äŠ””±£©”£
¢ŚŹ³ŃĪĖ®µÄ×÷ÓĆŹĒ______”£
£Ø¶ž£©ĢśµÄ»ÆŗĻĪļÖʱø
ÓĆ·ĻĢśŠ¼ÖʱøĢśŗģ(Ö÷ŅŖ³É·ÖĪŖFe2O3)ŗĶK2SO4µÄ²æ·ÖĮ÷³ĢČēĻĀĶ¼ĖłŹ¾£ŗ
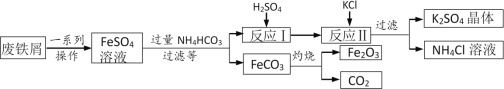
£Ø1£©¼Ó¹żĮæNH4HCO3·“Ó¦Ź±ĪĀ¶Č²»ŅĖ¹żøßµÄŌŅņĪŖ______”£
£Ø2£©·“Ó¦¢ńÉś³ÉµÄĘųĢå»ÆѧŹ½ŹĒ______”£
£Ø3£©K2SO4ŗĶNH4ClŌŚÅ©ŅµÉś²śÖŠ¶¼æÉ×ö______”£
£Ø4£©ĪŖ¼ģŃéK2SO4ÖŠŹĒ·ń»ģÓŠCl”Ŗ£¬ŅŖĻČ¼ÓČė×ćĮæ_____ČÜŅŗ£¬¾²ÖĆŗóŌŁ¼ÓĻņÉĻ²ćĒåŅŗÖŠµĪ¼ÓÉŁĮæ_____ČÜŅŗ”£
£Ø5£©ŌŚæÕĘųÖŠ×ĘÉÕFeCO3µÄ»Æѧ·½³ĢŹ½ĪŖ_____”£
£ØČż£©ĢśµÄŅ±Į¶ŗĶĢ½¾æ
Č”64.0g Fe2O3·ŪÄ©£¬Š”×éĶ¬Ń§ÓĆĻĀĶ¼×°ÖĆÄ£ÄāĮ¶Ģś£¬²¢²ā¶Ø·“Ó¦ŗó¹ĢĢå³É·Ö”£
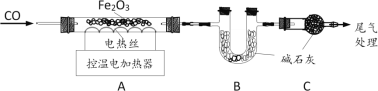
׏ĮĻ£ŗ¼īŹÆ»ŅæÉĪüŹÕH2OŗĶCO2”£
£Ø1£©Į¬½Ó×°ÖĆ£¬ĻČ_________£¬ŌŁ×°ČėŅ©Ę·”£
£Ø2£©ŹµŃ鏱ĻČĶØČėCO£¬ÄæµÄŹĒ_____________”£
£Ø3£©æŲÖĘAÖŠĪĀ¶Č·“Ó¦£¬¼ĢŠųĶØCOÖĮĄäČ“ŗóµĆµ½FeŗĶFeOµÄŗŚÉ«¹ĢĢ壬װÖĆBÖŠÖŹĮæŌöÖŲ30.8g”£ĒėĶعż¼ĘĖć»Ų“šŅŌĻĀĪŹĢā£ŗ
¢Ł¹ĢĢåÖŠFeOÖŹĮæĪŖ_______g”£
¢ŚAÖŠ·“Ó¦µĆµ½øĆŗŚÉ«¹ĢĢåµÄ»Æѧ·½³ĢŹ½ĪŖ_______”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĪŅ¹śŌŚ2017Äź”°ŹĄ½ē»·¾³ČÕ”±(6ŌĀ5ČÕ)Č·¶ØµÄÖ÷ĢāŹĒ”°ĀĢĖ®ĒąÉ½£¬¾ĶŹĒ½šÉ½Ņųɽ”±£®»ŖŃ©ÓėĶ¬Ń§ĆĒ»ż¼«²Ī¼ÓĮĖÕāŅ»Ö÷ĢāµÄ»ī¶Æ£¬ŌŚĄĻŹ¦µÄÖøµ¼ĻĀ£¬ĖūĆĒ¶ŌŅ»ŌģÖ½³§ÅŷŵÄĪŪĖ®½ųŠŠ¼ģ²ā£¬·¢ĻÖĘäÖ÷ŅŖµÄĪŪČ¾ĪļĪŖNaOH£®ĪŖĮĖ²ā¶ØĪŪĖ®ÖŠNaOHµÄŗ¬Į棬ĖūĆĒŹ×ĻČ°ŃČÜÖŹÖŹĮæ·ÖŹżĪŖ98%(ĆܶČ1.84g/cm3)µÄÅØĮņĖį20g£¬Ļ”ŹĶĪŖÖŹĮæ·ÖŹżĪŖ10%µÄĮņĖį£»Č»ŗóČ”80gĪŪĖ®ÓŚÉÕ±ÖŠ£¬ÖšµĪ¼ÓČė10%µÄĮņĖįÖĮ49gŹ±Ē”ŗĆĶźČ«·“Ó¦(¼Ł¶ØĪŪĖ®ÖŠµÄĘäĖü³É·Ö²»ÓėĮņĖį·“Ó¦)£®Ēė¼ĘĖć£ŗ
(1)°Ń20gÉĻŹöÅØĮņĖįĻ”ŹĶĪŖÖŹĮæ·ÖŹżĪŖ10%µÄĮņĖį£¬ŠčŅŖĖ®µÄÖŹĮæŹĒ______g£®
(2)ĪŪĖ®ÖŠĖłŗ¬NaOHµÄÖŹĮæ·ÖŹżŹĒ___________£æ(Š“³ö¼ĘĖć¹ż³Ģ)
(3)Č”80gøĆĪŪĖ®ÓŚÉÕ±ÖŠ·ÅÖĆ¼øĢģŗó£¬ČōĘäÖŠµÄĒāŃõ»ÆÄĘČ«²æ×Ŗ»ÆĪŖĢ¼ĖįÄĘ£®Ōņ“ĖŹ±Ó¦ÖšµĪ¼ÓČė10%µÄĮņĖį______æĖ²ÅÄÜŹ¹Ģ¼ĖįÄĘĒ”ŗĆĶźČ«±ä³ÉĮņĖįÄĘ£®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠŹµŃéÄÜ“ļµ½ÄæµÄŹĒ£Ø £©
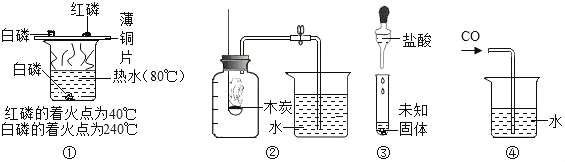
A. ¢ŁŃéÖ¤æÉČ¼ĪļČ¼ÉÕµÄĢõ¼ž
B. ¢Ś²ā¶ØæÕĘųÖŠO2µÄŗ¬Įæ
C. ¢Ū¼ģŃéCO32©µÄ“ęŌŚ
D. ¢ÜÓĆĖ®ĪüŹÕCO
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com