
分析 根据铁和硫酸反应生成硫酸亚铁和氢气,镁和硫酸反应生成硫酸镁和氢气,依据烧杯中物质增加的质量相等进行计算.
解答 解:铁和硫酸反应生成硫酸亚铁和氢气,化学方程式为:Fe+H2SO4=FeSO4+H2↑;
镁和硫酸反应生成硫酸镁和氢气,
Fe+H2SO4=FeSO4+H2↑ 烧杯中增加的质量
56 2 54
5.6g 5.4g
设需要镁的质量为x
Mg+H2SO4=MgSO4+H2↑ 烧杯中增加的质量
24 2 22
x 5.4g
$\frac{24}{x}$=$\frac{22}{5.4g}$
x=5.9g
故答案为:Fe+H2SO4=FeSO4+H2↑;5.9.
点评 由于反应放出气体,所加固体的质量并非烧杯内物质总质量实际增加的质量,实际增加质量为加入固体质量与放出气体质量的差.


科目:初中化学 来源: 题型:推断题
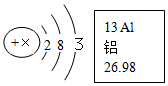 回答下列问题:
回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
| 第一次 | 第二次 | 第三次 | |
| O2质量(g) | 3 | 4 | 5 |
| SO2质量(g) | 6 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题

 ,则
,则查看答案和解析>>
科目:初中化学 来源: 题型:填空题
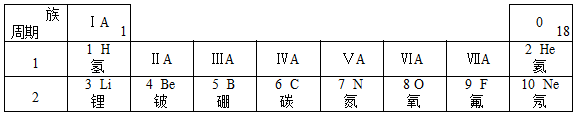
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com