
【题目】图是氯化钠和硝酸钾两种固体物质的溶解度曲线.
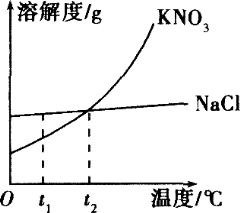
某兴趣小组为了研究NaCl和KNO3的溶解和结晶,做了两组实验(室温下),其过程如下:
[第一组]

[第二组]
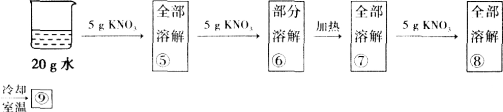
(1)①中溶质的质量分数为________________,⑨的现象是________________.
(2)第一组实验中操作a为________,所得氯化钠固体质量增多可能是下列原因中的(填字母序号)________.
A.溶解NaCl固体时,没有用玻璃棒搅拌
B.称量5g NaCl固体后,称量纸上仍留有固体
C.蒸发时,未及时停止加热,有固体溅出
D.蒸发后所得NaCl固体中仍含有水分
(3)上述实验过程中一定属于饱和溶液的是(填数字序号,下同)________,溶质与溶剂质量比一定相等的是________.
【答案】(1)20% 有晶体析出 (2)蒸发 D (3)②⑥⑨ ①和⑤(或⑥和⑨)
【解析】(2)由于氯化钠的溶解度受温度影响比较小,所以使氯化钠从溶液中结晶的方法一般采用蒸发溶剂的方法,当溶液达到饱和后继续蒸发会有白色晶体析出;所得氯化钠晶体的质量为11g,大于10g,可能原因为蒸发所得的氯化钠固体中仍含有水分.
(3)确定溶液是否饱和,关键要看该温度下能否继续溶解该溶质,不能继续溶解该溶质的溶液是饱和溶液,能继续溶解的是不饱和溶液.②⑥⑨中均有不能继续溶解的溶质存在,故实验过程中所得溶液一定达到饱和的是②⑥⑨;①和⑤中20g水中溶解的溶质质量相等,故溶质与溶剂的质量比一定相等;⑥、⑨都是同一温度下硝酸钾的饱和溶液,故溶质与溶剂的质量比也一定相等.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:
【题目】下列叙述中,正确的是
A.原子中一定含有质子、中子、电子三种粒子
B.“花香四溢”的现象说明分子之间有一定的间隔
C.氯化钠是由钠原子和氯原子构成的
D.蔗糖溶液里有不同种分子,属于混合物
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲、乙、丙三种固体物质的溶解度曲线如图所示,回答下列问题:
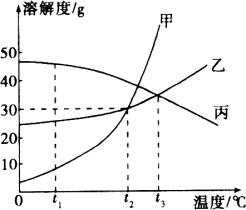
(1)t1℃时,甲、乙、丙三种物质的溶解度由大到小的顺序是________;
(2)t2℃时,甲和乙的溶解度________(填“相等”或“不相等”);
(3)t2℃时,甲物质的饱和溶液中溶质与溶剂的质量比为________(写最简比);
(4)t3℃时,将乙和丙两种物质的饱和溶液降低到t1℃,所得溶液中溶质的质量分数大小关系为:乙________丙(填“>”“<”或“=”).
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图所示,一物体悬挂在饱和的氯化钠溶液中,在恒温条件下向烧杯内的溶液中分别加入下列物质(悬挂物不参与反应),说明弹簧测力计读数变化情况(填写“变大”“不变”或“变小”).

(1)如果加入氯化钠晶体,弹簧测力计读数________;
(2)如果加入蒸馏水,弹簧测力计读数________;
(3)如果加入氯化钾晶体,弹簧测力计读数________.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某同学在一定温度下进行硝酸钾的溶解实验,实验数据如下表:
实验序号 | 实验1 | 实验2 | 实验3 | 实验4 |
水的质量(g) | 100 | 100 | 100 | 100 |
加入硝酸钾的质量(g) | 80 | 100 | 120 | 140 |
溶液质量(g) | 180 | 200 | 210 | 210 |
根据上述实验数据,下列叙述正确的是( )
A.实验1所得溶液的溶质质量分数为80%
B.实验2所得溶液为饱和溶液
C.实验4所得溶液的溶质质量分数比实验3大
D.该温度下,硝酸钾饱和溶液的溶质质量分数为52.4%
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室欲配制1000g溶质质量分数为4%的氢氧化钠溶液.配制步骤为:
(1)计算:需氢氧化钠固体________g,水________mL.(水的密度是1g/cm3)
(2)称量:用质量为23.1g的烧杯作称量容器,在托盘天平上称取氢氧化钠固体时,盛有氢氧化钠固体的烧杯应放在________盘.在下表所列的砝码中,选出所需砝码(打“√”表示选用):
砝码/g | 100 | 50 | 20 | 20 | 10 | 5 |
打“√”表示选用 |
并在下列标尺中选出能正确表示游码位置的选项________(填字母).
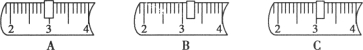
(3)溶解:将氢氧化钠固体溶于水,用________搅拌,使氢氧化钠全部溶解,冷却至室温.
(4)装瓶:把配制好的溶液装入试剂瓶,盖好瓶盖并贴上标签,放入试剂柜中.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】铜镁合金具有优良的导电性,常用作飞机天线等导电材料.欲测定合金的组成(其他元素忽略不计),进行如下实验:取铜镁合金20g放入烧杯,将280g稀硫酸分4次加入烧杯中,充分反应后,测得剩余固体的质量记录如下.请计算:
次数 | 1 | 2 | 3 | 4 |
加入稀硫酸质量/g | 70 | 70 | 70 | 70 |
剩余固体质量/g | 18.2 | 16.4 | 14.6 | 13.2 |
(1)合金中铜、镁的质量比.
(2)所加稀硫酸的溶质的质量分数.(写出计算过程)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】韩国“岁月号”沉船事故发生后,几百名潜水员参与了打捞工作,他们携带的水下供氧设备中供氧剂是过氧化钠(Na2O2),它与人呼出的二氧化碳及水蒸气反应生成氧气供人呼吸.某同学想进一步探讨过氧化钠与水的反应(2Na2O2+2H2O=4NaOH+O2↑),将15.6g过氧化钠加入盛有147.6g水(过量)的烧杯中充分反应,直至固体完全消失,不再有气泡产生.请计算:
(1)反应生成的氧气质量.
(2)反应后所得溶液中溶质的质量分数.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com