
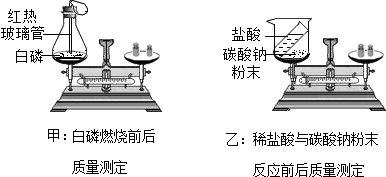
分析 (1)根据白磷燃烧的反应物和产物分析解答;
(2)根据反应生成气体且反应在敞口容器进行反应分析;
(3)在化学反应里肯定不变的是:物质的总质量、元素的种类、元素的质量、原子的种类、原子的质量、原子的数目;
(4)验证质量守恒定律时,应必须考虑密闭容器;
(5)用质量守恒定律解决一些常见类型的题目,主要利用守恒的原因来解答.
解答 解:(1)白磷燃烧放出热量,产生大量白烟,答:放出热量,产生大量白烟,化学方程式为:4P+5O2 $\frac{\underline{\;点燃\;}}{\;}$2P2O5;
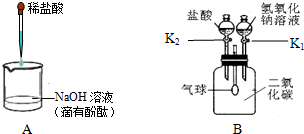
(2)由于装置是敞口的装置,碳酸钠和稀盐酸反应产生的二氧化碳从烧杯中逸出,总质量减少,所以天平不平衡;
(3)在化学反应里肯定不变的是:物质的总质量、元素的种类、元素的质量、原子的种类、原子的质量、原子的数目,可以据此选择为①②⑤⑥;
(4)验证质量守恒定律时,当有气体参加或生成的反应,应在密闭条件进行实验;
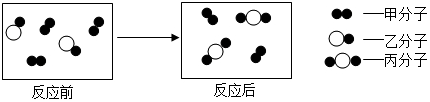
(5)根据反应前后元素的种类不变,可知X中含Na、C、O元素.根据反应前后原子的数目不变,可知X的化学式为Na2CO3;
故答案为:(1)4P+5O2 $\frac{\underline{\;点燃\;}}{\;}$2P2O5;
(2)装置是敞口的装置,碳酸钠和稀盐酸反应产生的二氧化碳从烧杯中逸出,总质量减少;
(3)①②⑤⑥;
(4)应在密闭条件进行实验;
(5)Na2CO3
点评 要验证质量守恒定律需根据反应物的状态和产物的状态选择敞口或密闭装置,若有气体参加或生成的反应需在密闭容器中进行.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:选择题
| A. | 铁锈蚀发生了缓慢氧化 | |
| B. | 同样的铁制品在海南比在兰州更易锈蚀 | |
| C. | 铝的抗锈蚀性能比铁强,铝的金属活动性也比铁强 | |
| D. | 铝的抗锈蚀性能比铁强,生活中可用钢丝球洗刷铝锅 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 用过氧化氢制氧气时,若二氧化锰用量偏少则所得氧气质量会偏少 | |
| B. | 测定空气中氧气含量时,若红磷量不足则测得氧气的含量会偏大 | |
| C. | 配制10%的食盐水时,若仰视读取水的体积则所配溶液的浓度会偏大 | |
| D. | 制取二氧化碳时,若用浓盐酸则制得的气体通入石灰水有可能不变浑浊 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
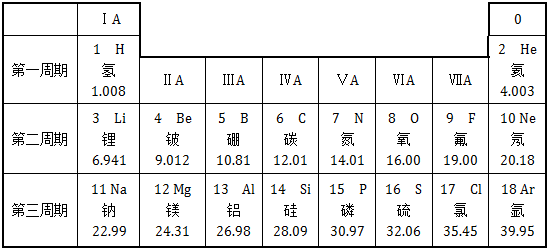
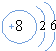 ,该微粒是元素周期表中的氧元素,它的核电荷数是8,碳元素的核电荷数是6,由此可知不同元素的本质区别是核电荷数不同.
,该微粒是元素周期表中的氧元素,它的核电荷数是8,碳元素的核电荷数是6,由此可知不同元素的本质区别是核电荷数不同.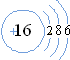 ,在化学反应中易得(填“得”或“失”)电子,是非金属(填“金属”或“非金属”)元素.则硫形成的离子符号为S2-
,在化学反应中易得(填“得”或“失”)电子,是非金属(填“金属”或“非金属”)元素.则硫形成的离子符号为S2-查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com