
����Ŀ�������������Ȼ���ֲ���С����ᾧ��(H2C2O4��2H2O)��ɫ���۵�Ϊ101�棬������ˮ��������ˮ��������170�����Ϸֽ⡣���������������Ʒ�Ӧ���ɳ�����H2C2O4��Ca(OH)2 === CaC2O4����2H2O��
��ش��������⣺
(1)����ͬѧ������ͼ��ʾ��װ�ã�ͨ��ʵ�������ᾧ��ķֽ�������a��������_________��װ��B����Ҫ������_________________��װ��C���������ݳ�������ʯ��ˮ����ǡ��ɴ˿�֪���ᾧ��ֽ�IJ�����һ����______________��
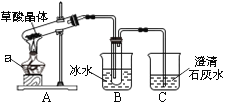
(2)����ͬѧ��Ϊ���ᾧ��ֽ�IJ����л���CO��Ϊ������֤��ѡ�ü���ʵ���е�װ��A��B����ͼ��ʾ�IJ���װ��(�����ظ�ѡ��)����ʵ�顣
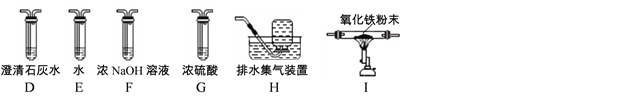
������ͬѧ��ʵ��װ���������ӵĺ���˳��ΪA��B����____������____������____����I��D��H��
��װ��I��ʢ�е���������������ɫ�仯����֤�����ᾧ��ֽ�IJ�������CO������ͬѧ��Ҫ����ʹ��װ��D��������ֱ���___________________________________��
���𰸡� �ƾ��� ��ֹ�����IJ������C�У�Ӱ��CO2�ļ��� CO2(�������̼) F D G ��һ��D�������Ա仯���ڶ���D�г���ʯ��ˮ����ǡ�
����������1������a�������Ǿƾ��ƣ�װ��B����Ҫ�����Ƿ�ֹ�����IJ������C�У�Ӱ��CO2�ļ��飻����ʯ��ˮ����������̼����ǣ���˵���ж�����̼�������ɣ�
��2����װ��AB����������Ҫ�Ⱦ���Ũ����������ҺF���ն�����̼����������ʯ��ˮD���������̼�Ƿ���ȫ���գ�Ȼ���پ���Ũ����G��ˮ����ͨ�뵽Iװ�û�ԭ����������������ʯ��ˮ�����ж�����̼���ɣ�����F��D��G���ڵ�һ��Dװ���еij���ʯ��ˮӦ�ò�����ǣ��ڶ�������ʯ��ˮװ��Ӧ�ñ���ǡ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��п��ϡ���ᷢ����Ӧʱ����������Һ������ʱ��ı仯������ͼ��ʾ��������ˮ�ֵ���ʧ������˵����ȷ���ǣ�������
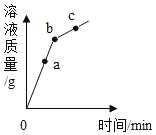
A. ��ʵ���ǽ�п����ϡ������
B. a���c���Ӧ��Һ����������Ӹ�����ͬ
C. b���c���Ӧ��Һ��п���Ӹ�������ͬ
D. ��Һ������������ʱ��ı仯Ҳ���ϸ����ߵı仯����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���±���NaCl��KNO3�ڲ�ͬ�¶�ʱ���ܽ�ȡ�
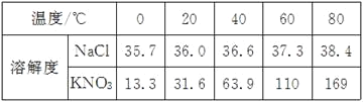
(1)��Ҫ�Ƚ�KNO3��NaCl��ˮ�е��ܽ���������Ҫ���Ƶı�����ˮ��������________��
(2)20��ʱ����ȡNaCl��KNO3����3.5g�ֱ����10gˮ�У�����ܽ��ﵽ����״̬����________��Һ��
(3)�����ϱ�����������ϵ�л��Ƴ�NaCl��KNO3���ܽ�����ߣ��������ߵĽ����Ӧ���¶ȷ�Χ��________(�����)��
A 0 ����20 �� B 20 ����40 ��
C 40 ����60 �� D 60 ����80 ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ˮ��Ӧ�����Ʊ�ˮú����������壩���䷴Ӧ����ʾ��ͼ��ͼ��ʾ������������ʾ��ͼ�ó��Ľ����У���ȷ���ǣ�������
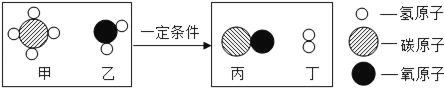
A. ˮú���ijɷ���һ����̼������
B. ��Ӧ�мͱ�������֮��Ϊ4��7
C. ��Ӧ�к���Ԫ�صĻ�����������
D. ��Ӧǰ��̼Ԫ�صĻ��ϼ�δ�����仯
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��a��b��c�������ʵ��ܽ�����ߣ�����˵����ȷ����
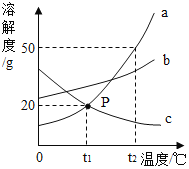
A. P���ʾt1��ʱ��a��c������Һ�������������
B. t2��ʱ����30ga���ʼ��뵽50gˮ�г�ֽ��裬�õ�80ga�ı�����Һ
C. t2��ʱ�����������ֱ�����Һ������t1�棬������Һ���ܼ�����c��b��a
D. ��t1��ʱa��b��c�������ʵ���Һ�ֱ�������t2�棬���������������������ܷ����仯
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��NSR����ͨ��BaO��Ba(NO3)2���ת��ʵ��NOx(��������)�Ĵ���ͻ�ԭ������Ч���Ͳ��ͷ������ڿ������������µ�NOx�ŷš��乤��ԭ������ͼ��ʾ��
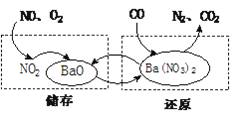
(1)��ԭʱ��ԭβ��������CO��H2�ȣ��������·�Ӧ��5CO + Ba(NO3)2 == N2 + X + 5CO2
����Ӧ�У�̼Ԫ�صĻ��ϼ�_______(��������������������)��
��X�Ļ�ѧʽ��______��
(2)����ʱ������NO������Ӧ�Ļ�ѧ����ʽΪ___________������NOx(��NO��NO2)��������_____________��
(3)NO����ͨ��NSR����ת��ΪN2���ܷ�Ӧ����ʽ��_________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������CO2����ͨ��KOH��Ba��OH��2��KAlO2�Ļ����Һ�У����ɳ�����ͨ��CO2�����Ĺ�ϵ��ͼ��ʾ�����к������ǣ���֪��Al��OH��3+KOH�TKAlO2+2H2O��2KAlO2+CO2+3H2O�T2Al��OH��3��+K2CO3��CO32��+CO2+H2O�T2HCO3������������
A. 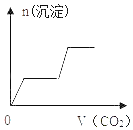 B.
B. 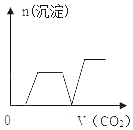
C. 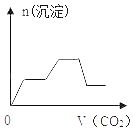 D.
D. 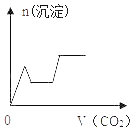
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij���������Na2SO4��NaCl��Na2CO3��KNO3�е�һ�ֻ�����ɣ���ʵ�����£�
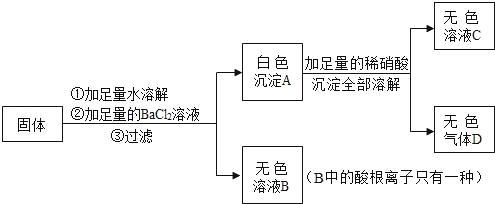
�Իش�
��1����ɫ����A�Ļ�ѧʽΪ_____����ɫ����D�Ļ�ѧʽΪ_____
��2��ԭ������һ������_____��һ��������_____�����ܺ���_____��
��3��Ϊ�����������ܺ��е������Ƿ�һ�����ڣ�ijͬѧ�����������ʵ�鷽����
��ȡ������������ˮ������������Ba��NO3��2��Һ����ַ�Ӧ���ˣ�
��ȡ��Һ����AgNO3��Һ���۲����ް�ɫ�������ɣ��ɴ˵ó����ۣ�������ijͬѧ��ʵ�鷽�����У�����������Ba��NO3��2��Һ��Ŀ����_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������������̽����
�������龰��ij��ѧʵ��С��ͬѧ������Ͷ������ͭ��Һ�У��������ɺ�ɫ�������ʵ�ͬʱ�н϶�����ݷų�����һ������ͬѧ�ǵ�̽�����������ɵ���ʲô���壿
��������룩���������Ԫ�صĽǶȣ��ų������������SO2��O2��H2
���������ϣ�SO2������ˮ��������NaOH��Ӧ������Na2SO3
��������ƣ������������룬ʵ��С��ͬѧ�ֱ���������·�����
��1����ͬѧ��Ϊ��O2�������___________���м��顣
��2����ͬѧ��Ϊ��SO2����ֻ�轫�ų�������ͨ��ʢ��NaOH��Һ��ϴ��ƿ�У�����ͨ��ǰ��ϴ��ƿ��������д��SO2��NaOH��Ӧ�Ļ�ѧ����ʽ ____________��
��3��ʵ��С��ͬѧ����������������ʵ�鷽�����ų�����֤��������塣����ų�����O2��H2������Ϊ�����еİ�ȫ������_____________ ��
��ͬѧ��Ϊ��Ϊȷ����ȫ��ʵ��ǰӦ���ռ�һ�Թ����壬����_______ʵ�飬���ɲ��������װ�ý���ʵ�顣
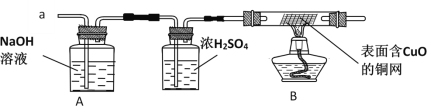
��ʵ��̽��������ͬѧȷ�ϰ�ȫ��С��ͬѧ���ȶ�װ��A���г������ٽ��ռ����������aͨ�룬��һ�����ȼB���ƾ��ƣ�һ��ʱ����ֱ��溬CuO��ͭ���ɺ�ɫ��Ϊ�����ĺ�ɫ��ֹͣͨ�����ٴγ���װ��A������������������
���ۣ�����������ͭ��Һ��Ӧʱ��������������_____________��
��˼ά��չ��
�����鷢�֣�������ͭ��Һ��ֻ����һ�������ӣ���������ʵ������Ƴ�������ͭ��Һ�к��е���������____________��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com