
| A. | 喝了汽水会打嗝,说明压强减小气体的溶解度增大 | |
| B. | 金刚石和石墨物理性质存在着明显差异,是因为构成它们的碳原子的排列方式不同 | |
| C. | 二氧化锰可以加快过氧化氢分解速率,所以二氧化锰可以做任何化学反应的催化剂 | |
| D. | C、H2、CO都具有还原性,在一定条件下它们都能跟氧化铁发生置换反应 |
分析 A、根据气体溶解度的影响因素解答;
B、根据金刚石和石墨的性质差异的原因解答;
C、根据催化剂的特点解答;
D、根据置换反应的概念解答.
解答 解:A、喝了汽水会打嗝,是因为温度升高,气体的溶解度减小的缘故,错误;
B、金刚石和石墨物理性质存在着明显差异,是因为构成它们的碳原子的排列方式不同,正确;
C、二氧化锰可以加快过氧化氢分解速率,但并不是任何反应的催化剂,错误;
D、置换反应是一种单质和一种化合物生成另一种单质和另一种化合物的反应,一氧化碳与氧化铁是两种化合物的反应,故不是置换反应,错误;
故选B.
点评 本题考查的是气体溶解度的影响因素以及物质性质差异的原因,完成此题,可以依据已有的知识进行.


 补充习题江苏系列答案
补充习题江苏系列答案 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案科目:初中化学 来源: 题型:填空题
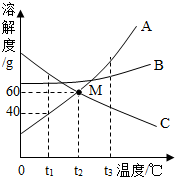 图是常见固体物质的溶解度曲线,根据图示回答:
图是常见固体物质的溶解度曲线,根据图示回答:查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 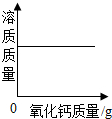 表示向一定温度下的饱和氢氧化钙溶液中不断加入氧化钙固体 | |
| B. | 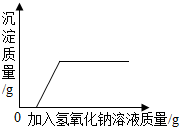 表示向盐酸和氯化铜的混合溶液中加人过量的氢氧化钠溶液 | |
| C. | 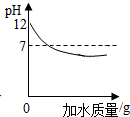 表示向pH=12的氢氧化钠溶液中加水稀释 | |
| D. | 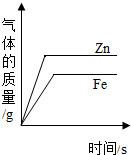 表示分别向等质量的锌和铁中加人溶质质量分数相同的稀盐酸至过量 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 除去铁粉中混有的铜粉 | B. | 用浓盐酸与锌粒制取氢气 | ||
| C. | 用稀盐酸除去水壶中的水垢 | D. | 除去硫酸钠溶液中的氢氧化钠 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | Cu Zn Ag | B. | Fe Cu Mg | C. | Zn Ag Fe | D. | Mg Al Cu |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
| 序号 | ① | ② | ③ | ④ |
| 物质 | 醋酸 | 高锰酸钾 | 熟石灰 | 纯碱 |
| 化学式 | CH3COOH | KMnO4 | Ca(OH)2 | Na2CO3 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 某小组同学对木炭还原氧化铜实验进行如下探究活动.
某小组同学对木炭还原氧化铜实验进行如下探究活动.| 木炭与氧化铜的质量比 | 1:7 | 1:11 | 1:13 |
| 实验现象 | 红热,产生大量气泡, 石灰水变浑浊 | 红热,产生大量气泡, 石灰水变浑浊 | 偶尔红热,有气泡, 石灰水变浑浊 |
| 实验结果 | 表层铜珠较大,有较多 黑色粉末 | 亮红色金属光泽, 网状铜块 | 暗红色层状粉末里含 微细铜粒 |
| 反应前质量 | 反应后质量 | |
| 硬质玻璃管+固体混合物/g | 79.8 | 75.4 |
| 洗气瓶+澄清石灰水/g | 158.8 | 162.6 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com