
| 20℃时,一些物质的溶解度 | ||
| | OH- | CO32- |
| Na+ | 溶 | 溶 |
| Ca2+ | 微 | 不 |
| Mg2+ | 不 | 微 |

| 物质 | NaCl | NaHCO3 | NH4Cl | NH3 | CO2 |
| 溶解度 | 36.0g | 9.6g | 37.2g | 710 | 0.9 |



 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源:不详 题型:单选题
| 加入物质 | 碳酸钠溶液 | 氢氧化钡溶液 | 氧化铜粉末 |
| 现象 | 产生无色气体 | 产生白色沉淀 | 固体溶解 |
查看答案和解析>>
科目:初中化学 来源:不详 题型:单选题
| | 物质 | 所含杂质 | 除去杂质的试剂或方法 |
| A | Cu | Fe | 加过量稀盐酸后过虑、洗涤、干燥 |
| B | NaCl | Na2CO3 | 加适量的稀盐酸后,蒸发溶剂 |
| C | CO2 | HCl | 通人盛有氢氧化钠溶液的洗气瓶,然后干燥 |
| D | FeCl2 | CuCl2 | 加入过量的铁粉后,再过虑 |
查看答案和解析>>
科目:初中化学 来源:不详 题型:单选题
| A.NH4+、H+、NO3- | B.H+、Na+、HCO3- |
| C.Fe2+、OH-、SO42- | D.K+、H+、MnO4- |
查看答案和解析>>
科目:初中化学 来源:不详 题型:单选题
| A.加水得澄清溶液,样品中一定没有CaCl2 |
| B.样品中一定含有NaCl,可能含有NaHCO3 |
| C.样品中一定含有NaHCO3,可能含有NaCl |
| D.所加的稀盐酸溶质质量分数小于7.3% |
查看答案和解析>>
科目:初中化学 来源:不详 题型:单选题
| A.酸中一定含有氢元素 |
| B.呈碱性的溶液一定是碱的溶液 |
| C.生成盐和水的反应一定是中和反应 |
| D.在化学反应中,质量和化学性质都不改变的物质一定是催化剂 |
查看答案和解析>>
科目:初中化学 来源:不详 题型:单选题
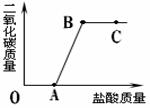
| A.OA段没有发生任何化学反应 |
| B.A点溶液中的溶质只有NaCl |
| C.B点表示加入的盐酸与原溶液中的溶质恰好完全反应 |
| D.C点的溶液的pH=7 |
查看答案和解析>>
科目:初中化学 来源:不详 题型:单选题
| A.烧碱可以用来改良酸性土壤 |
| B.人体代谢产生的CO2如不能及时排出,会使血液的pH增大 |
| C.用稀盐酸除去铁制品表面的锈 |
| D.“加碘盐”是在食盐中加入适量碘单质,食用“加碘盐”对健康无益 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com