
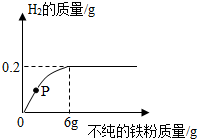
 向一定量的稀盐酸中逐渐加入某种不纯的铁粉,加入铁粉的量与生成H2的关系如图所示,请回答有关问题:
向一定量的稀盐酸中逐渐加入某种不纯的铁粉,加入铁粉的量与生成H2的关系如图所示,请回答有关问题:分析 (1)P点表示铁粉的量不足,盐酸过量;
(2)根据图示可得最终生成氢气的质量为0.2g,结合方程式可得参加反应的铁粉的质量,进一步求该铁粉中杂质的质量分数.
解答 解:(1)P点表示铁粉的量不足,盐酸过量,所以溶液的pH>7;
(2)设铁粉中含铁的质量为x
Fe+2HCl=FeCl2+H2↑
56 2
x 0.2g
$\frac{56}{x}=\frac{2}{0.2g}$
x=5.6g
该铁粉中杂质的质量分数为$\frac{6g-5.6g}{6g}$×100%=6.7%.
答:该铁粉中杂质的质量分数为6.7%.
点评 本题主要考查学生运用化学方程式进行计算和推断的能力,比较简单,计算时要注意规范性和准确性.


 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案科目:初中化学 来源: 题型:推断题

查看答案和解析>>
科目:初中化学 来源: 题型:推断题
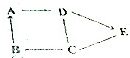 A、B、C、D为初中常见的四种不同类型的化合物.其中A为常见的钠盐,B常温下为气体,其固体常用于人工降雨,E是蓝色的硫酸盐溶液,它们之间关系如图.(图中“-”表示相互能反应,“→”表示转化关系.)
A、B、C、D为初中常见的四种不同类型的化合物.其中A为常见的钠盐,B常温下为气体,其固体常用于人工降雨,E是蓝色的硫酸盐溶液,它们之间关系如图.(图中“-”表示相互能反应,“→”表示转化关系.)查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
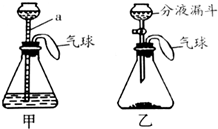 某化学兴趣小组设计了一组“吹气球”实验,两套装置如图所示:
某化学兴趣小组设计了一组“吹气球”实验,两套装置如图所示:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
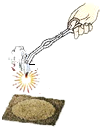 为了加深对质量守恒定律的理解,某校化学实验小组以“镁条在空气中燃烧”实验进行了再探究:
为了加深对质量守恒定律的理解,某校化学实验小组以“镁条在空气中燃烧”实验进行了再探究:查看答案和解析>>
科目:初中化学 来源: 题型:推断题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 时间/h | 1 | 1.5 | 4 | 8 | 12 | 24 | 48 | 60 | |
| 吸水 质量/g | 硫酸甲 | 1.6 | 2.2 | 5.2 | 10.3 | 14.0 | 20.9 | 29.2 | 32.1 |
| 硫酸乙 | 1.2 | 1.5 | 3.5 | 5.9 | 8.1 | 12.9 | 19.5 | 21.0 | |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com