
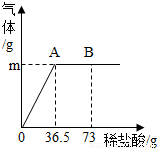
 某纯碱样品中含有少量的氯化钠杂质.现称取6g该纯碱样品放在烧杯中并滴加稀盐酸.当盐酸滴加至36.5g时,烧杯内溶液的总质量为40.3g(假设产生的气体全部逸出),产生气体的质量与滴入稀盐酸的质量关系如图所示.试回答:
某纯碱样品中含有少量的氯化钠杂质.现称取6g该纯碱样品放在烧杯中并滴加稀盐酸.当盐酸滴加至36.5g时,烧杯内溶液的总质量为40.3g(假设产生的气体全部逸出),产生气体的质量与滴入稀盐酸的质量关系如图所示.试回答:
 ×100%=16.3%
×100%=16.3%

科目:初中化学 来源: 题型:
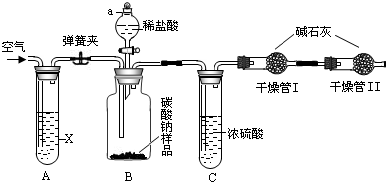
查看答案和解析>>
科目:初中化学 来源: 题型:
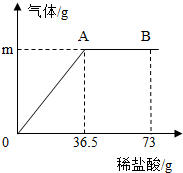 某纯碱样品中含有少量的氯化钠杂质.现称取6g该纯碱样品放在烧杯中并滴加稀盐酸.当盐酸滴加至36.5g时,烧杯内溶液的总质量为40.3g(假设产生的气体全部逸出),产生气体的质量与滴入稀盐酸的质量关系如图所示.试回答:
某纯碱样品中含有少量的氯化钠杂质.现称取6g该纯碱样品放在烧杯中并滴加稀盐酸.当盐酸滴加至36.5g时,烧杯内溶液的总质量为40.3g(假设产生的气体全部逸出),产生气体的质量与滴入稀盐酸的质量关系如图所示.试回答:查看答案和解析>>
科目:初中化学 来源: 题型:
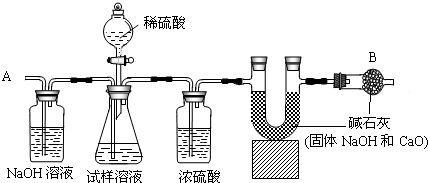
查看答案和解析>>
科目:初中化学 来源: 题型:
 如图是配制好的盐酸溶液的标签,请根据标签上的文字信息,进行计算:
如图是配制好的盐酸溶液的标签,请根据标签上的文字信息,进行计算:查看答案和解析>>
科目:初中化学 来源: 题型:
 (2013?贵港一模)某纯碱样品中含有少量的氯化钠杂质.现称取6g该纯碱样品放在烧杯中并滴加稀盐酸.当盐酸滴加至36.5g时,烧杯内溶液的总质量为40.3g(假设产生的气体全部逸出),产生气体的质量与滴入稀盐酸的质量关系如图所示.试回答:
(2013?贵港一模)某纯碱样品中含有少量的氯化钠杂质.现称取6g该纯碱样品放在烧杯中并滴加稀盐酸.当盐酸滴加至36.5g时,烧杯内溶液的总质量为40.3g(假设产生的气体全部逸出),产生气体的质量与滴入稀盐酸的质量关系如图所示.试回答:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com