
| 选项 | 亊 实 | 解 释 |
| A | 4毫升水和4毫升酒精混合后体积小于8毫升 | 分子不断运动 |
| B | NaOH溶液、Ca(OH)2溶液均显碱性 | 溶液中都含有金属离子 |
| C | CO和CO2的化学性质不同 | 物质组成元素不同 |
| D | 装空气的注射器比装水的注射器容易压缩 | 气体分子间间隔大于液体分子间间隔 |
| A. | A | B. | B | C. | C | D. | D |
分析 根据分子的基本特征:分子质量和体积都很小;分子之间有间隔;分子是在不断运动的;同种物质的分子性质相同,不同物质的分子性质不同,结合事实进行分析判断即可.
解答 解:A、4毫升水和4毫升酒精混合后体积小于8毫升,是因为分子之间有间隔,一部分水分子和酒精分子会互相占据分子之间的间隔,故选项解释错误.
B、NaOH溶液、Ca(OH)2溶液均显碱性,是因为溶液中都含有氢氧根离子,故选项解释错误.
C、CO和CO2的化学性质不同,是因为它们分子的构成不同,不同种的分子性质不同,而不是物质组成元素不同,故选项解释错误.
D、装空气的注射器比装水的注射器容易压缩,是因为气体分子间间隔大于液体分子间间隔,故选项解释正确.
故选:D.
点评 本题难度不大,掌握分子的基本性质及利用分子的基本性质分析和解决问题的方法是解答此类题的关键.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
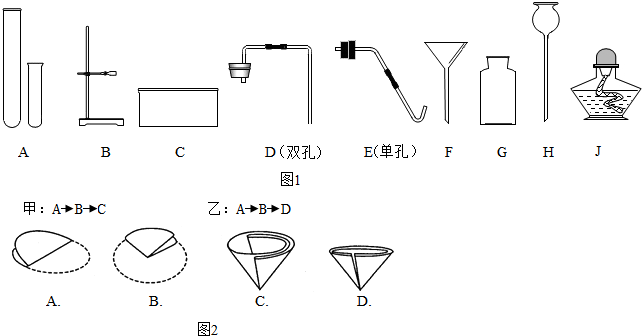
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
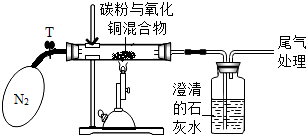 某小组同学对木炭还原氧化铜实验进行如下探究活动.
某小组同学对木炭还原氧化铜实验进行如下探究活动.| 木炭与氧化铜的质量比 | 1:7 | 1:11 | 1:13 |
| 实验现象 | 红热,产生大量气泡,石灰水变浑浊 | 红热,产生大量气泡,石灰水变浑浊 | 偶尔红热,有气泡,石灰水变浑浊 |
| 实验结果 | 表层铜珠较大,有较多黑色粉末 | 亮红色金属光泽,网状铜块 | 暗红色层状粉末里含微细铜粒 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com