
| 实验方案 | 测溶液的pH | 滴加Na2CO3溶液 | 滴加BaCl2溶液 |
| 实验操作 | 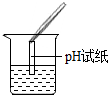 | 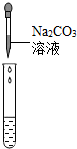 | 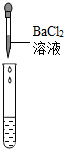 |
| 实验现象 | 试纸变色,对比比色卡,pH<7 | 有气泡产生 | 产生白色沉淀 |
| 实验结论 | 溶液中有H2SO4 | 溶液中有H2SO4 | 溶液中有H2SO4 |
分析 【学生板演】硫酸和氢氧化钠反应生成硫酸钠和水,注意化学式的写法和配平;
【假设猜想】根据酸碱不能共存判断不合理的猜想;
【实验探究】根据碳酸钠和硫酸反应能生成二氧化碳气体解答;
【评价反思】(1)根据图示操作判断,检测溶液的pH时,pH试纸不能伸入溶液中;
(2)检验一种物质时要排除其他物质的干扰,硫酸钠也能与氯化钡反应生成白色沉淀.
解答 解:【学生板演】硫酸和氢氧化钠反应生成硫酸钠和水,化学方程式为H2SO4+2NaOH═Na2SO4 +2H2O;
【假设猜想】硫酸和氢氧化钠反应生成硫酸钠和水,酸或碱可能过量,当氢氧化钠过量时,反应后溶液中的溶质为硫酸钠和氢氧化钠,故猜想三为氢氧化钠和硫酸钠,酸碱过量,但不能同时过量,因为酸碱不能共存,会继续反应,故猜想三不合理;
【实验探究】(1)硫酸铜和氢氧化钠反应能生成氢氧化铜蓝色沉淀,因此溶液中滴加几滴CuSO4溶液,无明显变化,说明溶液中一定没有氢氧化钠.
(2)溶液中有硫酸,滴加碳酸钠后,碳酸钠会和硫酸反应生成二氧化碳气体,因此会看到产生气泡.
【评价反思】(1)根据图示操作判断,检测溶液的pH时,pH试纸不能伸入溶液中,应用玻璃棒蘸取少量溶液涂到pH试纸上;
(2)检验一种物质时要排除其他物质的干扰,硫酸钠也能与氯化钡反应生成白色沉淀,故不能证明溶液中一定存在硫酸;
故答案为:【学生板演】H2SO4+2NaOH=Na2SO4+2H2O;
【假设猜想】有Na2SO4和NaOH;猜想三;H2SO4和NaOH在溶液中不能共存;
【实验探究】(1)NaOH;(2)有气泡产生;
【评价反思】①pH试纸浸入溶液中;②Na2SO4与BaCl2反应也会生成白色沉淀,不能证明一定有H2SO4存在.
点评 此题通过中和反应考查了化学方程式的书写,实验方案设计、实验操作以及实验方案的评价,解答时要全面审题,认真解答.


 期末集结号系列答案
期末集结号系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
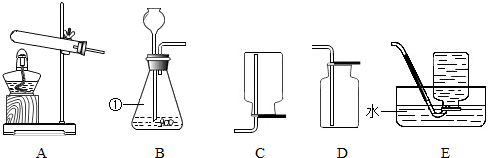
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 北方的冬天,树枝上的雾凇是凝华形成的 | |
| B. | 打开冰箱门,看见门前冒白气,这是汽化现象 | |
| C. | 档案材料要用碳素笔填写,这是因为碳的化学性质活泼 | |
| D. | 在化学变化中原子总数一定不变,而分子总数一定发生变化 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | M的化学性质很稳定 | B. | M中有氨气 | ||
| C. | M由四种元素组成 | D. | M可能是碳酸氢钠 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 生活中常见物质的性质、制法的是化学研究的重要内容.
生活中常见物质的性质、制法的是化学研究的重要内容.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com