
分析 ①氧化铁和一氧化碳在高温条件下反应能生成铁和二氧化碳;根据生铁和钢的组成以及合金的概念来分析;
②根据钢铁锈蚀的条件来分析;
③根据反应原理来书写化学方程式;
④根据金属活动顺序以及根据化学式来分析计算相关问题.
解答 解:①氧化铁和一氧化碳在高温条件下反应能生成铁和二氧化碳;生铁和钢都是铁的合金,属于金属材料,均属于混合物.故填:3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;故填:ABC;
②铁与氧气、水共存时最易生锈,把钢铁制品放置在干燥的环境中,主要是为了减少与水接触;故填:水;
③铁与硫酸铜反应生成硫酸亚铁和铜;故填:Fe+CuSO4═Cu+FeSO4;
④根据金属活动性由强到弱的顺序:锌>铁>H>铜,向硫酸亚铁、硫酸铜的混合溶液中加入一些锌粉,铜首先被置换出来,待铜被完全置换后,铁开始被置换;
将过滤得到固体不溶物放入少量的稀硫酸中,有气体产生,说明固体中有活动性较强的铁或锌,若锌过量,固体中含有锌;若锌量不足或恰好完全反应,则固体中不含锌;充分反应后剩余的固体为铜,质量为1.6g.在硫酸铜中,铜元素的质量分数为:$\frac{64}{64+32+16×4}×100%$=40%.则含1.6g铜元素需要硫酸铜的质量为$\frac{1.6g}{40%}$=4g.
故填:Fe,Cu; 4.
点评 考查了铁的冶炼原理、铁合金、铁的锈蚀因素、金属的活动性顺序以及根据物质组成的相关计算.难度适中.


科目:初中化学 来源: 题型:解答题
| 盐溶液 | NaCl | Na2CO3 | BaCl2 |
| pH | 等于7 | 大于7 | 等于7 |
| 实验步骤 | 实验现象 | 实验结论 |
| ①称取上述氢氧化钠固体样品10.0g溶于50ml水配成溶液,向溶液中滴加氯化钡溶液至过量,充分反应后,静置. | 产生白色沉淀 | 说明久置固体中,一定含有Na2CO3 |
| ②用玻璃棒蘸取少量①中充分反应后的上层清液滴在一小块pH试纸上,与标准比色卡对比,测出pH | pH=11 | 说明久置固体中,还一定含有NaOH |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
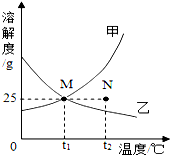
| A. | 甲物质的溶解度随温度的升高而增大 | |
| B. | 在t1℃时,甲、乙两物质的溶解度相等 | |
| C. | 在 t2℃时,N点表示甲物质的不饱和溶液 | |
| D. | 在t1℃时,100g乙物质的饱和溶液中溶质的质量是25g |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 只含有Mg2+、SO42- | |
| B. | 一定含有Cl-、K+,可能含有Mg2+、SO42- | |
| C. | 一定含有Mg2+、SO42-,可能含有Cl-、K+ | |
| D. | 一定含有K+、Mg2+、Cl-、SO42- |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
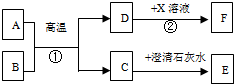 A-F和X都是初中化学中的常见物质,其中A、C是无色气体,B、F是红色固体,它们的转化关系如下图所示(部分生成物已省略):
A-F和X都是初中化学中的常见物质,其中A、C是无色气体,B、F是红色固体,它们的转化关系如下图所示(部分生成物已省略):查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com