
����Ŀ������и�ǿ�ȡ����۵㡢����ʴ���ŵ㣬�ڹ�ҵ�ϵõ��㷺�����á�ͼ1�ǻ����������Ʊ�������IJ�������ͼ���������ʲ��������Ӧ����
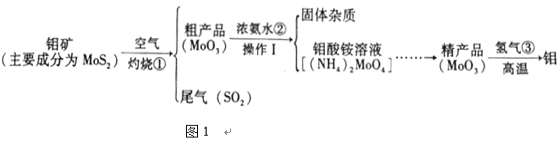
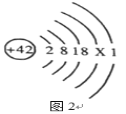
��1���������弰��ֲ������_______________��ѡ������Ԫ������������Ԫ��������ԭ�ӵĽṹʾ��ͼ2������X��_________________��
��2������ٷ�Ӧ�Ļ�ѧ����ʽ_________________________________��
��3���������ʿ�����������SO2β������_________������ĸ����
A ����������Һ B Ũ���� C ��ˮ
��4��(NH4)2MoO4��Mo�Ļ��ϼ���_____________����ũҵ�ϼ����������_______�ʡ�
��5�������ʵ����ģ�����������Ҫʹ�õ���Ҫ����������©������������________��
��6������H2��CO�ֱ�ԭ�������ľ���Ʒ��MoO3��������Ļ�ԭ����������Ϊ____��
���𰸡���Ԫ�� 13 2Mo+7O2![]() 2MoO3+4SO2 AC +6 �� �ձ� 1��14
2MoO3+4SO2 AC +6 �� �ձ� 1��14
��������
��1���������弰��ֲ��������Ԫ�أ���ԭ���У��˵�����������������ԭ�ӵĽṹʾ��ͼ2������X��42-2-8-18-1=13��
��2����������ͼ��֪������ٷ�Ӧ��MoS2��O2�ڸ��������·�Ӧ����SO2��MoO3����Ӧ�Ļ�ѧ����ʽΪ��2Mo+7O2![]() 2MoO3+4SO2��
2MoO3+4SO2��
��3���������������������ơ���ˮ��Ӧ��������Ũ���ᷴӦ������������SO2β����������������Һ�Ͱ�ˮ����ѡAC��
��4����(NH4)2MoO4�У�笠��ӡ���Ԫ�صĻ��ϼ۷ֱ�Ϊ+1��-2���裺(NH4)2MoO4����Ļ��ϼ�Ϊx�����ݻ�������Ԫ�صĻ��ϼ۵Ĵ�����Ϊ�㣬���У���+1����2+x+��-2����4=0
���x=+6��(NH4)2MoO4��Mo�Ļ��ϼ���+6��(NH4)2MoO4�к��е�Ԫ�أ���ũҵ�ϼ���������ǵ��ʣ�
��5���������ǽ�������Һ����롣�����ʵ����ģ�����������Ҫʹ�õ���Ҫ����������©�������������ձ���
��6������H2��CO�ֱ�ԭ�������ľ���Ʒ��MoO3��������Ļ�ԭ���ֱ�ΪH2��CO��
�裺MoO3������Ϊm������Ļ�ԭ���ֱ�ΪH2��CO�����ֱ�Ϊx��y��

![]()
![]() ��
��
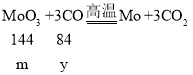
![]()
![]() ��
��![]() ������H2��CO�ֱ�ԭ�������ľ���Ʒ��MoO3��������Ļ�ԭ����������Ϊ1:14��
������H2��CO�ֱ�ԭ�������ľ���Ʒ��MoO3��������Ļ�ԭ����������Ϊ1:14��


 ��Ч���ܿ�ʱ��ҵϵ�д�
��Ч���ܿ�ʱ��ҵϵ�д� �ݾ�ѵ������ϵ�д�
�ݾ�ѵ������ϵ�д� С����ȫ�ܼ��ϵ�д�
С����ȫ�ܼ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���˵�վ�к�ȼ���˻��������ӵ�ײ���£�ԭ�Ӻ˷������ѣ�����믡��ȵ�ԭ�Ӽ�һЩ���Ӻ����ߣ�ͬʱ�ͷŴ�������������Щ�����������������ֻ����磮��Ԫ����Ԫ�����ڱ�����ʾ����Ϣ�����ӽṹʾ��ͼ��ͼ��ʾ�����±�������ȷ���ǣ� ��
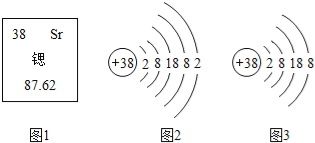
A. ͼ2��ͼ3��������Ԫ�� B. ͼ3����ʾ���ӵĻ�ѧ������Sr
C. ��ԭ�ӵ�������Ϊ38 D. ��ԭ�ӵ����ԭ��������87.62g
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ͨ������ʵ������ܵó���Ӧ���۵���
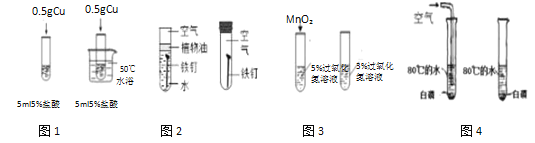
A. ͨ��ͼ 1 ̽��ʵ�飬�¶ȶԷ�Ӧ���ҳ̶ȵ�Ӱ��
B. ͨ��ͼ 2 ̽��ʵ�飬���������������Ҫ������ˮ��ͬ����
C. ͨ��ͼ 3 ̽��ʵ�飬���������ܼӿ����������Һ�ֽ������
D. ͨ��ͼ 4 ̽��ʵ�飬��ȼ��ȼ����Ҫ�ﵽ�Ż�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ����������������ͭ�����������Ļ����Һ�м���п�ۣ���ַ�Ӧ��������Һ�����������п�۵�������ϵ��ͼ��ʾ����ش�
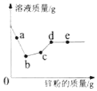
��1��д��ab�η�����Ӧ�Ļ�ѧ����ʽ��_____
��2��c�㴦��Һ�е���������Щ��_____
��3��cd����Һ������Ϊʲô������_____
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼΪʵ������ȡ������̼����֤�����ʵ�ʵ�飨�г�װ����ȥ����
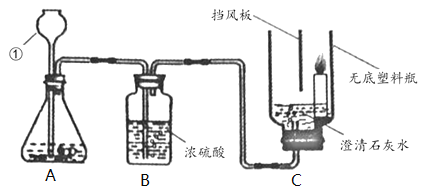
��1�������ٵ�����___________��
��2��װ��A�з�����Ӧ�Ļ�ѧ����ʽΪ_________________________________________��ʵ���һ������ø�װ����ȡ_________________
��3��װ��B��Ũ���������_______________________________________��
��4��װ��C�й۲쵽������____________________��˵��CO2���е�����________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij���������Na2SO4��NaCl��Na2CO3��KNO3�е�һ�ֻ�����ɣ���ʵ�����£�
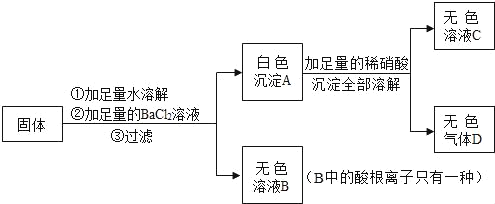
�Իش�
��1����ɫ����A�Ļ�ѧʽΪ_____����ɫ����D�Ļ�ѧʽΪ_____
��2��ԭ������һ������_____��һ��������_____�����ܺ���_____��
��3��Ϊ�����������ܺ��е������Ƿ�һ�����ڣ�ijͬѧ�����������ʵ�鷽����
��ȡ������������ˮ������������Ba��NO3��2��Һ����ַ�Ӧ���ˣ�
��ȡ��Һ����AgNO3��Һ���۲����ް�ɫ�������ɣ��ɴ˵ó����ۣ�������ijͬѧ��ʵ�鷽�����У�����������Ba��NO3��2��Һ��Ŀ����_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������һ����Ҫ�Ļ���ԭ�ϣ�Ҳ��ʵ���ҳ��õĻ�ѧ�Լ�����ҵ�ϳ����Ի�����(��Ҫ�ɷ���FeS2)Ϊԭ���������ᡣ�����ⶨij��������FeS2�ĺ���(���ʲ����뷴Ӧ)��ij��ȤС���ͬѧ����ʦ��ָ���£��������ϣ���4FeS2+11O2![]() 2Fe2O3+8SO2 ��Na2SO3+H2O2��Na2SO4+H2O������������ʵ�飺
2Fe2O3+8SO2 ��Na2SO3+H2O2��Na2SO4+H2O������������ʵ�飺
I����ȡ1.60 g��������Ʒ������ͼ��ʾװ��(�г�װ��ʡ��)��ʯӢ���У���a�����ϵػ���ͨ���������������ʯӢ���еĻ�������Ʒ����ȫ��Ӧ��
II. ��Ӧ��������ƿ�е���Һ������ͼ������
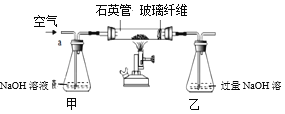
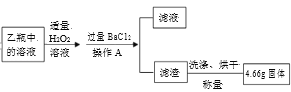
��ش��������⣺
(1)��ƿ��NaOH��Һ��������____��
(2)�ס�����ƿ�ڷ����Ļ�ѧ��Ӧ���ƣ���д����ƿ�ڷ�����Ӧ�Ļ�ѧ����ʽ____��
(3)����Aʹ�õIJ����������ձ��⣬����____��
(4)���յõ���4.66g������____(д��ѧʽ)��
(5)�û�������Ʒ��FeS2����������Ϊ___��
(6)���ȱ�ټ�װ�ã������ղ����Ʒ��FeS2��������������____(����ƫ������ƫС����������)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ�����������ߣ��������ǵ�����ϢϢ��ء�
��1��ȫ�桢����������ش�ʳ������ȡӪ�����ʣ������彡���Ļ�����֤���ڼ�����������ˡ�����������ʳ���и����������_____��
��2��ijƷ������ˮ��ǩ�����˸�ˮ���ơ��ء��Ƶȵĺ������ơ��ء��Ƶ���ָ_____��
A ԭ�� B ���� C ���� D Ԫ��
��3��������������Դ����_____��
A ʯ�͡��� B ��Ȼ������ C ̫���� D ú
��4����������ɽ��ʡ����������������ĵؼ��У���������������ʵʩ�����ڸ������ǵľ�ס��������Ϊ��ɫֲ�������ն�����̼�����ͷų��������䷴Ӧԭ��Ϊ6CO2+6H2O X+6O2����X �Ļ�ѧʽΪ_____��������ĸ��ţ�
X+6O2����X �Ļ�ѧʽΪ_____��������ĸ��ţ�
A CH4 B CH3OH C C2H5OH D C6H12O6
��5������ʱ�䣬�ҹ����ٳ��к͵��������������࣬����ˮ��������������Ⱦ����������ϸС�� ������ɣ���Ҫ��Դ���ȵ��ŷš���������������β����������ů�Լ�����ҳ��ȡ�����ʴ�����ǵĽ� ��������Ӱ�������ǵ�����ͳ��У��������������Ĵ�ʩ�У����е���_____��������ţ�
��ѹ����ʯȼ�Ϣڿ��Ƴ���ʹ�âۼ��ٻ����ܼ�ǿ�����̻��ݹرճ�����ҵ������Դ�ṹ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ȤС���ͬѧΪ���о���Cu��Zn�Ͻ���Ʒ��ͭ�ĺ�����ȡ����Ʒ20g��������ϡ�����ַ�Ӧ����������������������ϡ�����������ϵ����ͼ��ʾ������㣺
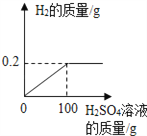
��1����Ӧ����������Ϊ����g��
��2������Ʒ��ͭ�ĺ�����
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com