��2013?��������ģ�������¹������������¹��ġ�����Ϊ��ʱ������ѧ�������Dz���Ҫѧϰ�Ļ�֪ʶ������Ҫ��ע��ᣬ��ע���
��1��2013��4��20��8��02���Ĵ�ʡ�Ű���«ɽ�ط���7.0�����𣮵�������ȫ����������֣���־�ɳǣ��������л���������������
�پ�����Ҫ���������������ҹ����Ƴ���Ư�۸���Ч������ˮ��������ClO
2�����䷴Ӧ���۹���ͼ���£�
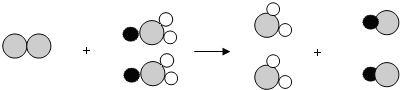
������

��ʾ��ԭ�ӣ�

��ʾ��ԭ�ӣ�

��ʾ��ԭ�ӣ�
�Իش�ClO
2����
��������
��������
�������ȵĻ��ϼ�Ϊ
+4
+4
�ۣ�
���ݷ�Ӧ���۹���ͼд����Ӧ�Ļ�ѧ����ʽΪ
Cl2+2NaClO2=2ClO2+2NaCl
Cl2+2NaClO2=2ClO2+2NaCl
��
�ڹ���ҩ��ֹ����Ŀ�����ּ���ҩеĿ¼�а�����һ���Է�����������̿�������֡��ǿ�����̶����ϵȣ����з���������Ҫ�����û���̿��
����
����
�ԣ�
�۵�������ȫ������Ϊ���������ṩ�������������ڵĸ��־�����Ʒ�����±��ش�
| ������Ӫ���ɷֱ���ÿ100g�к����� |
����
��g�� |
֬��
��g�� |
������
��g�� |
ˮ��
��g�� |
��
��mg�� |
��
��mg�� |
��
��mg�� |
��
��mg�� |
����C
��mg�� |
���� |
| 61.6 |
21.1 |
9.5 |
3.6 |
1144 |
134 |
80 |
25 |
0 |
�� |
������������Ӫ������Ҫ�е����ʡ�
����
����
����֬�����κ�ˮ��
��2���л��߷��Ӳ��ϡ��������Ϻ����ǽ�������������ʹ�õ�������������ϣ������Ը��Ե��ص����������������Ҫ��
���л��߷��Ӳ��ϡ��������ϡ�����ɽ��ⱻ�㷺�������һ������ĭ���ϣ����������ϡ���ʹ�ÿɼ��١�
��ɫ
��ɫ
��Ⱦ����
�ڽ��������У���һ������Ͻ��ܹ���������γɽ������������һ�������·ֽ��ͷų�������������ԭ������
��ѧ
��ѧ
�仯��ѡ���������ѧ������
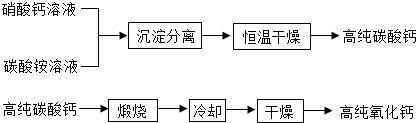
�����ǽ��������У����ڵ��ӹ�ҵ�ĸߴ�̼��ƺߴ������������������£�
ʵ���ҳ�����
����
����
�������г������룬�����ߴ�̼���ʱ��ѡ��220����¸��������ѡ���¡���������ɴ˲�����ԭ����
���û�ѧ����ʽ˵������
��3����������CO
2��������̼�����չ��̼�����ѳ�Ϊһ�ֻ���ʱ�У�����������г�����135�����У���1�������ڲ��У�3�������������г���5�������������ͨ���ߣ��ᳫ����̼���С�������ɫ���С���
������CO
2�ŷţ����ǻ���Ѱ�Ҳ���̼Ԫ�ص�ȼ�ϣ����о�����NH
3ȼ�յIJ���û����Ⱦ�����ͷŴ�����������һ��Ӧ��ǰ�����뽫NH
3ȼ�շ�Ӧ�Ļ�ѧ����ʽ����������4NH
3+3O
2 6H
2O+
2N2
2N2
��
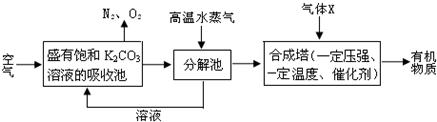
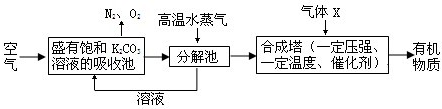
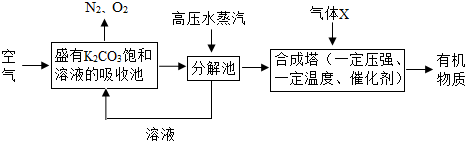
�ڷ�����ѧ��PaulSabatier���á����ת��������ʹCO
2��H
2�ڴ�������������CH
4��H
2O����д���÷�Ӧ�Ļ�ѧ����ʽ
��



 �������¿��ÿ�ʱ��ҵϵ�д�
�������¿��ÿ�ʱ��ҵϵ�д� Ӣ�żƻ�ͬ����ʱ��Чѵ��ϵ�д�
Ӣ�żƻ�ͬ����ʱ��Чѵ��ϵ�д�

 ��ʾ��ԭ�ӣ�
��ʾ��ԭ�ӣ� ��ʾ��ԭ�ӣ�
��ʾ��ԭ�ӣ� ��ʾ��ԭ�ӣ�
��ʾ��ԭ�ӣ�