
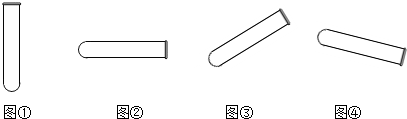
 Š”ŃļŗĶŠ”ĢĘĶ¬Ń§ŌŚŃ§Ļ°ĮĖ”°ÖŹĮæŹŲŗć¶ØĀÉ”±ŗó£¬ĖūĆĒµ½ŹµŃéŹŅĻėĒ××ŌĢ½¾æĘäĖū»Æѧ·“Ó¦ŹĒ·ńŅ²×ńŹŲÖŹĮæŹŲŗć¶ØĀÉ£¬Š”ŃīŗĶŠ”ĢʵďµŃé·½·ØČēĶ¼ĖłŹ¾£ŗ
Š”ŃļŗĶŠ”ĢĘĶ¬Ń§ŌŚŃ§Ļ°ĮĖ”°ÖŹĮæŹŲŗć¶ØĀÉ”±ŗó£¬ĖūĆĒµ½ŹµŃéŹŅĻėĒ××ŌĢ½¾æĘäĖū»Æѧ·“Ó¦ŹĒ·ńŅ²×ńŹŲÖŹĮæŹŲŗć¶ØĀÉ£¬Š”ŃīŗĶŠ”ĢʵďµŃé·½·ØČēĶ¼ĖłŹ¾£ŗ·ÖĪö £Ø1£©øł¾ŻĪļÖŹ·“Ó¦Ź±Éś³ÉĪļµÄדĢ¬ŗĶ·“Ó¦ŗóÉÕĘæÄŚÖŹĮæµÄ±ä»Æ·ÖĪö£»
øł¾ŻĪļÖŹ·“Ó¦Ź±Éś³ÉĪļµÄדĢ¬ŗĶ·“Ó¦ŗóÉÕĘæÄŚÖŹĮæµÄ±ä»Æ·ÖĪö£»
£Ø2£©»Æѧ·½³ĢŹ½Ź±ŅŖ×¢Ņā·“Ó¦ĪļŗĶÉś³ÉĪļµÄ»ÆѧŹ½£¬²¢ĒŅ²»ŅŖĶü¼ĒÅäĘ½ŗĶÉś³ÉĪļדĢ¬·ūŗÅ£®
£Ø3£©ŌŚ±ķ“ļÖŹĮæŹŲŗć¶ØĀɵĽįĀŪŹ±£¬Ņ»¶Ø²»ŅŖĀ©µō·“Ó¦Īļ»ņÉś³ÉĪļµÄÖŹĮ棬ĢŲ±šŹĒĘųĢåµÄĪļÖŹ£¬ČŻŅ×ŗöĀŌ£®
£Ø4£©øł¾ŻŠ”ĒæÓėŠ”·åĖł×öµÄŹµŃ飬æ¼ĀĒµĆµ½µÄĘōŹ¾£®
½ā“š ½ā£ŗ
£Ø1£©Š”ŃļŌŚŹµŃé¹ż³ĢÖŠ·¢ÉśµÄ·“Ó¦ŹĒĀČ»Æ±µŗĶĮņĖįÄĘ·“Ӧɜ³ÉĮņĖį±µ³Įµķ£¬·“Ó¦ŗóĪļÖŹµÄ×ÜÖŹĮæ²»±ä£¬æɹŪ²ģµ½µÄĻÖĻó£ŗ¢ŁÉÕ±ÖŠÓŠ°×É«³ĮµķÉś³É£¬¢ŚĢģĘ½±£³ÖĘ½ŗā£®
Š”ĢĘŌŚŹµŃé¹ż³ĢÖŠ·¢ÉśµÄ·“Ó¦ŹĒĢ¼ĖįÄĘŗĶŃĪĖįÉś³É¶žŃõ»ÆĢ¼ĘųĢ壬·“Ó¦ŗó׶ŠĪĘæÄŚÖŹĮæ¼õÉŁ£¬æɹŪ²ģµ½µÄĻÖĻó£ŗ¢ŁÉÕ±ÖŠÓŠĘųÅŻÉś³É£¬¢ŚĢģĘ½ÖøÕėĻņÓŅĘ«×Ŗ£®
£Ø2£©ÕāĮ½øöŹµŃéĖł·¢Éś·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ
Š”ŃļµÄŹµŃé£ŗCuSO4+2NaOH=Cu£ØOH£©2”ż+Na2SO4£»
Š”ĢʵďµŃé£ŗNa2C03+2HCl=2NaCl+H2O+CO2”ü£®
£Ø3£©Š”ŃļÓėŠ”ĢĘøł¾Żø÷×ŌµÄŹµŃéĻÖĻóµĆ³öĮĖ²»Ķ¬µÄ½įĀŪµÄŌŅņŹĒŠ”ŃļµÄŹµŃé֊ƻӊĀ©µō·“Ó¦ĪļŗĶÉś³ÉĪļµÄÖŹĮ棬Š”ĢʵďµŃéĀ©µōÉś³ÉĪļÖŠĘųĢåµÄÖŹĮ森
£Ø4£©øł¾ŻŠ”ŃļÓėŠ”ĢĘĖł×öµÄŹµŃ飬ÄćµĆµ½µÄĘōŹ¾ŹĒ£ŗÓŠĘųĢå²Ī¼Ó»ņÓŠĘųĢåÉś³ÉµÄŹµŃ飬Čē¹ūÓĆĄ“ŃéÖ¤ÖŹĮæŹŲŗć¶ØĀÉŅ»¶ØŅŖŌŚĆܱÕČŻĘ÷ÄŚ½ųŠŠ£®
¹Ź“š°øĪŖ£ŗ
£Ø1£©Ą¶É«³Įµķ£¬ĢģĘ½±£³ÖĘ½ŗā£»
ĘųÅŻ²śÉś£¬ĢģĘ½ÖøÕėĻņÓŅĘ«×Ŗ£»
£Ø2£©CuSO4+2NaOH=Cu£ØOH£©2”ż+Na2SO4£»Na2CO3+2HCl=2NaCl+CO2”ü+H2O£»
£Ø3£©Š”ĢʵďµŃéŌŚ³ØæŚČŻĘ÷ÄŚ½ųŠŠµÄ£¬Š”ĢʵďµŃéĀ©µōÉś³ÉĪļÖŠĘųĢåµÄÖŹĮ棬¶ųŠ”ŃļµÄŹµŃéŌŚĆÜ·āµÄČŻĘ÷ÄŚ½ųŠŠµÄ£®
£Ø4£©Ćܱգ®
µćĘĄ ŌŚŃéÖ¤ÖŹĮæŹŲŗć¶ØĀÉŹ±£¬ŗÜČŻŅ×ŗöĀŌĘųĢåµÄÖŹĮ棬²»¹ÜŹĒ·“Ó¦Īļ»¹ŹĒÉś³ÉĪļÖŠĘųĢåµÄÖŹĮ棬Ņņ“ĖŅ»¶ØŅŖ×¢Ņāµ½£®


 »ĘøŌĢģĢģĮ·æŚĖćĢāæØĻµĮŠ“š°ø
»ĘøŌĢģĢģĮ·æŚĖćĢāæØĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ė®ĶعżČżĢ¬±ä»Æ£¬ŹµĻÖĮĖ×ŌÉķµÄĢģȻѻ· | |
| B£® | ÓĆ·ŹŌķĖ®æÉŅŌĒų·ÖÓ²Ė®ÓėČķĖ® | |
| C£® | Éś»īÖŠæÉŅŌÓĆÖ󷊵ķ½·Ø½µµĶĖ®µÄÓ²¶Č | |
| D£® | ÓĆĀĖÖ½¹żĀĖæÉŅŌ³żČ„Ė®ÖŠĖłÓŠµÄĪļÖŹ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¼ĘĖćĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ÓĆ“óĄķŹÆ×ö²¹øĘ¼Į£¬ĪŖČĖĢå²¹³äøĘŌŖĖŲ | |
| B£® | ±»ĪĆ³ę¶£Ņ§ŗó£¬ĶæÄØ·ŹŌķĖ®æÉŅŌ¼õĒįĢŪŃ÷ | |
| C£® | ÓĆŃĒĻõĖįÄĘ“śĢęŹ³ŃĪėē×ÕŹ³Ę· | |
| D£® | ÓĆpHŹŌÖ½æɲāµĆÕż³£ÓźĖ®µÄpHŌ¼ĪŖ5.6 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | “æ¾»Īļ¶¼ŹĒÓÉĶ¬ÖÖŌŖĖŲ×é³ÉµÄ | B£® | ÓÉĶ¬Ņ»ÖÖ·Ö×Ó¹¹³ÉµÄĪļÖŹ½Šµ„ÖŹ | ||
| C£® | Ņ»ÖÖµ„ÖŹÖ»ÄÜÓÉŅ»ÖÖŌŖĖŲ×é³É | D£® | Óɲ»Ķ¬ÖÖŌŖĖŲ×é³ÉµÄĪļÖŹ½Š»ÆŗĻĪļ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¼ĘĖćĢā
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com