
【题目】实验室中有一瓶未知浓度的硫酸铜溶液,为了得知它的溶质质量分数,同学们进行了以下实验操作:向盛有100g溶质质量分数为15%的氢氧化钠溶液的烧杯中加入几滴酚酞溶液,随后向其中加入100g待测硫酸铜溶液.反应结束后,烧杯中的溶液为无色,并产生了蓝色沉淀.求:
(1)判断此时两种溶液是否完全反应,并说明理由
(2)待测硫酸铜溶液的溶质质量分数.
【答案】
(1)完全反应,若氢氧化钠有剩余,则溶液为红色;若硫酸铜有剩余,则溶液为蓝色
(2)33.3%
【解析】解:(1)氢氧化钠显碱性,能使酚酞变红色,反应结束后,烧杯中的溶液为无色,所以此时两种溶液完全反应,理由是:若氢氧化钠有剩余,则溶液为红色;若硫酸铜有剩余,则溶液为蓝色;
(2)设待测硫酸铜溶液的溶质质量分数为x,
2NaOH + CuSO4=Na2SO4+Cu(OH)2↓
80 160
100g×15% 100g×x![]() =
=![]()
x=33.3%
故答案为:(1)完全反应,若氢氧化钠有剩余,则溶液为红色;若硫酸铜有剩余,则溶液为蓝色;(2)33.3%.
(1)氢氧化钠显碱性,能使酚酞变红色;
(2)硫酸铜和氢氧化钠反应生成氢氧化铜沉淀和硫酸钠,然后根据氢氧化钠溶液的质量以及质量分数即可求出待测硫酸铜溶液的溶质质量分数.


 备战中考寒假系列答案
备战中考寒假系列答案科目:初中化学 来源: 题型:
【题目】某化学小组为测定一瓶失去标签的盐酸的溶质质量分数,分成甲、乙两组,分别用不同的方法进行测定。实验设计:
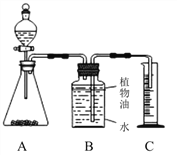
甲组:取纯净碳酸钙粉末5g于烧杯中,加入20g该盐酸溶液,充分反应后,过滤、洗涤、干燥,称量得剩余固体3g。
乙组:取纯净碳酸钙粉末5g于锥形瓶中,将20g该盐酸溶液加入分液漏斗,测定产生二氧化碳的体积0.4L(20℃、标准大气压,二氧化碳的密度为1.977g/L)计算盐酸浓度。
【数据处理】:
(1)你认为哪一种实验方法不准确,请说明原因_______________________________。
(2)请利用你认为实验合理的一组数据计算该盐酸的溶质质量分数为__________。(写出计算过程)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某同学编写的化学小报中,标题下文章中的主角是一氧化碳,则该标题可能是()
A.形成酸雨的罪魁祸首
B.新装修房屋内空气中的杀手
C.燃气热水器安装在居室内的危险
D.PM2.5与雾霾天气
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列有关做法中,化学在能源利用、环境保护等方面起不到正确作用的是
A.从电池中回收金属等再利用
B.使用新型的可降解塑料,减少白色污染
C.改进汽车尾气净化技术,减少有害气体排放
D.将生活污水倒入大河中流走,以免造成对人们生活环境的影响
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是R原子结构示意图和磷元素的相关信息,下列说法错误的是( )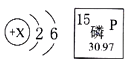
A.X=8
B.磷元素的相对原子质量为15
C.两种元素可形成化学式为P2R5的化合物
D.磷可以在R的单质中剧烈燃烧
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】我国约在南北朝时就开始冶炼黄铜,黄铜是铜和锌的合金(Cu-Zn),它可用来制造电器零件及日用品。小华利用一瓶稀盐酸和相关的仪器,测定黄铜样品的组成(不考虑黄铜中的其他杂质)。将30mL稀盐酸分三次加入到10g黄铜样品粉末中,每次充分反应后,测定生成氢气的质量,实验数据见下表:
第一次 | 第二次 | 第三次 | |
连续加入盐酸的体积/mL | 10 | 10 | 10 |
生成氢气的质量/g | 0.08 | 0.08 | 0.04 |
(1)从上表数据分析,小华用10 g合金粉末总共收集到氢气g。
(2)求该合金中铜的质量分数。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com