
有一包白色粉末A,由CuSO4、CaCO3、BaCl2、Na2SO4、NaOH中的两种或两种以上的物质混合而成。为探究其组成,进行如下实验(实验流程如图):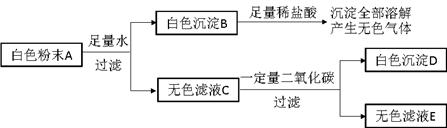
(1)取白色粉末A,向其中加入足量水,充分搅拌后过滤,得到白色沉淀B和无色滤液C。由此可判断,原白色粉末中一定不含有 。
(2)向白色沉淀B中加入足量稀盐酸,沉淀全部溶解,并产生无色气体。由此可判断,原白色粉末中一定含有 。
(3)向无色滤液C中通入一定量二氧化碳,充分反应后过滤,得到白色沉淀D和无色滤液E,由此可判断,原白色粉末中一定还含有 。
(4)若流程图中白色粉末A为20g,白色沉淀D为9.85g,无色滤液E中只含一种溶质。
①无色滤液E中的溶质为 ;
②通过计算确定20g白色粉末A中所含各物质的质量。
(请写出计算及推理过程)
 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:阅读理解
| 阴离子 阳离子 |
OH- | Cl- | CO32- | HCO3- |
| H+ | 溶、挥 | 溶、挥 | 溶、挥 | |
| Ca2+ | 微 | 溶 | 不 | 溶 |
| Ba2+ | 溶 | 溶 | 不 | 溶 |
| 实验步骤 | 实验操作 | 实验中可能出现的现象 | 相应结论 |
| 一 | 向A的试样中加入足量的水 | ①A的试样全部溶解 | A是 Na2CO3和NaHCO3 Na2CO3和NaHCO3 |
| ②A的试样部分溶解 | A是 Na2CO3和CaCO3或NaHCO3和CaCO3 Na2CO3和CaCO3或NaHCO3和CaCO3 | ||
| 二 | 若A的试样部分溶解则向其滤液中加入 酚酞试液 酚酞试液 |
③ 溶液显红色 溶液显红色 |
A是 Na2CO3和CaCO3 Na2CO3和CaCO3 |
| ④ 溶液显浅红色 溶液显浅红色 |
A是 NaHCO3和CaCO3 NaHCO3和CaCO3 |
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源:2012年江苏省南京市白下区中考化学一模试卷(解析版) 题型:解答题
查看答案和解析>>
科目:初中化学 来源:2011-2012学年江苏省南京市白下区中考一模化学试题(解析版) 题型:计算题
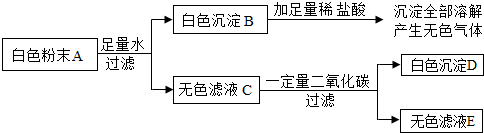
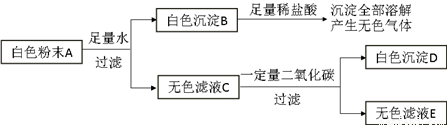
有一包白色粉末A,由CuSO4、CaCO3、BaCl2、Na2SO4、NaOH中的两种或两种以上的物质混合而成。为探究其组成,进行如下实验(实验流程如图):

(1)取白色粉末A,向其中加入足量水,充分搅拌后过滤,得到白色沉淀B和无色滤液C。由此可判断,原白色粉末中一定不含有 。
(2)向白色沉淀B中加入足量稀盐酸,沉淀全部溶解,并产生无色气体。由此可判断,原白色粉末中一定含有 。
(3)向无色滤液C中通入一定量二氧化碳,充分反应后过滤,得到白色沉淀D和无色滤液E,由此可判断,原白色粉末中一定还含有 。
(4)若流程图中白色粉末A为20g,白色沉淀D为9.85g,无色滤液E中只含一种溶质。
①无色滤液E中的溶质为 ;
②通过计算确定20g白色粉末A中所含各物质的质量。
(请写出计算及推理过程)
【解析】(1)硫酸铜溶于水得到的是蓝色溶液,可以据此判断该题;
(2)硫酸钡不溶于酸,所以根据白色沉淀全部溶解,可以判断该白色沉淀为碳酸钙,可以据此作答;
(3)通入二氧化碳产生了白色沉淀,根据二氧化碳的性质可以判断该混合物中还含有氢氧化钠和氯化钡;
(4)根据上述分析及题给的条件可以判断出反应为:二氧化碳和氢氧化钠反应生成了碳酸钠,然后氯化钡和碳酸钠的反应,所以最后得到的溶液为氯化钠溶液,可以据此解答该题.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com