
利用氢气还原灼热氧化铜的实验试样中氧化铜的质量分数(装置如下,杂质不发生反应,其中氯化钙用来吸收水分),得到下列结果:
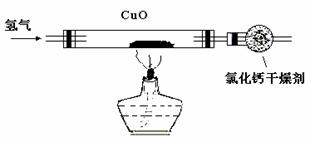
| 实验前 | 实验后 | |
| 氧化铜+玻璃管 | 20g | 16.8g |
| 氯化钙+干燥管 | 100.8g | 104.4g |
根据实验数据,求:
(1)完全反应后生成水的质量为___________;
(2)试样中氧化铜的质量分数为_______________;
若氢气量不足,则氧化铜的质量分数_______________(填偏大、偏向或不变)
 灵星计算小达人系列答案
灵星计算小达人系列答案 孟建平错题本系列答案
孟建平错题本系列答案科目:初中化学 来源: 题型:

| 实验前 | 实验后 | |
| (氧化铜+玻璃管)的质量/g | 75.6 | 69.2 |
| (氧化钙+U型管)的质量/g | 110.8 | 118.0 |
查看答案和解析>>
科目:初中化学 来源: 题型:
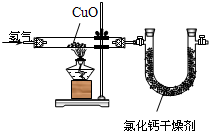 某学校探究学习小组,利用纯净的氢气还原氧化铜(杂质不与氢气反应)来测定氧化铜的纯度(装置如图所示),得到如下数据:
某学校探究学习小组,利用纯净的氢气还原氧化铜(杂质不与氢气反应)来测定氧化铜的纯度(装置如图所示),得到如下数据:| 实验前 | 实验后 | |
| A.氧化铜样品 | 40.0克 | 34.0克 |
| B.氯化钙+U型管 | 100.8克 | 108.0克 |
| ||
| ||
查看答案和解析>>
科目:初中化学 来源:2001年第十一届“天原杯”全国初中学生化学素质和实验能力竞赛复赛试卷(解析版) 题型:解答题
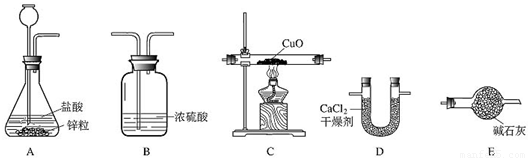
| 实验前 | 实验后 | |
| (氧化铜+玻璃管)的质量/g | 75.6 | 69.2 |
| (氧化钙+U型管)的质量/g | 110.8 | 118.0 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com