
ĻĀĶ¼ŹĒ¼×”¢ŅŅĮ½ÖÖ¹ĢĢåĪļÖŹµÄČܽā¶ČĒśĻß”£ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ

A.¼×µÄČܽā¶Č±ČŅŅ“ó
B.t2”ꏱ£¬½«20g¼×ĪļÖŹ¼ÓČėµ½50gĖ®ÖŠ£¬æɵƵ½70gČÜŅŗ
C.t2”ꏱ¼×µÄ±„ŗĶČÜŅŗµÄČÜÖŹÖŹĮæ·ÖŹż“óÓŚ30%
D.æɲÉÓĆ½µµĶĪĀ¶ČµÄ·½·ØŹ¹ŅŅµÄ²»±„ŗĶČÜŅŗ±äĪŖ±„ŗĶČÜŅŗ

| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗø£½ØŹ”ÄžµĀŹŠø£¶¦ĻŲ2019-2020ѧğ¾ÅÄź¼¶ÉĻѧʌʌ֊»ÆѧŹŌ¾ķ ĢāŠĶ£ŗĢīæÕĢā
Ķعż°ėøöѧʌµÄѧĻ°ĪŅĆĒŅŃ¾ČĻŹ¶ĮĖŅ»Š©»ÆѧÓĆÓļ£¬ĒėÓĆ»Æѧ·ūŗÅĢīæÕ£ŗ
(1)2øöĒāŌ×Ó____”£
(2)ĄÆÖņŌŚæÕĘųÖŠ³ä·ÖČ¼ÉÕ£¬²śĪļÓŠ____ŗĶ_____”£
(3)æÕĘųÖŠŗ¬Įæ×ī¶ąµÄĘųĢåŹĒ_____£¬ĖüæÉÓĆÓŚÖʵŖ·Ź”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗŗžÄĻŹ”³¤É³ŹŠ³¤É³ŃÅĄń¼ÆĶÅ2019-2020ѧğ¾ÅÄź¼¶ÉĻѧʌʌĩĮŖæ¼»ÆѧŹŌ¾ķ ĢāŠĶ£ŗĢīæÕĢā
2019Äź£¬³¤É³µŲĢś½ØÉč½ųČėŠĀµÄĄļ³Ģ±®”£
£Ø1£©µŲĢś½ØÉč¹ż³ĢÖŠ¹ć·ŗŹ¹ÓĆĮĖŅŌĻĀ²ÄĮĻ£¬ĘäÖŠŹōÓŚ½šŹō²ÄĮĻµÄŹĒ_____”£
A ²»ŠāøÖ B ĖÜĮĻ C “óĄķŹÆ D ĀĮŗĻ½š
£Ø2£©µŲĢśµÄæŖĶØ£¬øųČĖĆĒµÄ³öŠŠ“ųĄ“ĮĖ±ćĄū”£×÷ĪŖĪÄĆ÷µÄ³¤É³ŹŠĆńĪŅĆĒÓ¦øĆ×öµ½”°ĪÄĆ÷³öŠŠ£¬°²Č«³öŠŠ”±£¬ĻĀĮŠĪļĘ·²»ŅĖŠÆ“ų³Ė×ųµŲĢśµÄŹĒ_____”£
A æóČŖĖ® B ³ō¶¹øÆ C ŃĢ»Ø D Źé±¾
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗŗžÄĻŹ”³¤É³ŹŠ³¤É³ŃÅĄń¼ÆĶÅ2019-2020ѧğ¾ÅÄź¼¶ÉĻѧʌʌĩĮŖæ¼»ÆѧŹŌ¾ķ ĢāŠĶ£ŗµ„Ń”Ģā
ĻĀĮŠÓŠ¹ŲæÕĘų¼°Ęä³É·ÖµÄĖµ·ØÕżČ·µÄŹĒ£Ø £©
A.µŖĘųµÄ»ÆѧŠŌÖŹŗÜ»īĘĆ£¬³£ÓĆ×÷±£»¤Ęų
B.æÕĘųÖŠĻ”ÓŠĘųĢåµÄĮæĢ«ÉŁ£¬²»¾ß±øČĪŗĪ¼ŪÖµ
C.¶žŃõ»ÆĢ¼ŹĒæÕĘųĪŪČ¾ĪļÖ®Ņ»£¬ÄÜŠĪ³ÉĖįÓź
D.ŃõĘųµÄÓĆĶ¾ŗܹć·ŗ£¬Äܹ©øųŗōĪüŗĶÖ§³ÖČ¼ÉÕ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ2018ÄźĖÄ“ØŹ”ĄÖɽŹŠÉ³ĶåĒųÖŠæ¼Ä£Äā»ÆѧŹŌ¾ķ ĢāŠĶ£ŗĢīæÕĢā
Ė®ŗĶæÕĘų¶¼ŹĒČĖĄąÖŲŅŖµÄ׏Ō“”£
£Ø1£©½ą¾»µÄæÕĘųŹōÓŚ _£ØĢī”°»ģŗĻĪļ”±»ņ”°“æ¾»Īļ”±£©
£Ø2£©ŅŗŃõŗĶŅŗĒāŹĒŌĖŌŲ”°ÓńĶĆ”±ŗÅŌĀĒņ³µ»š¼żµÄŅ»“ŁĶĘ½ų¼Į£¬ĘäŌĄķŹĒĄūÓĆŅŗŃõŗĶŅŗĒā¾ēĮŅČ¼ÉÕ£¬·“Ó¦Ėł²śÉśµÄ¾Ž“óĶĘĮ¦Ź¹»š¼żÉĻÉż”£ŌŚøĆ»Æѧ·“Ó¦ÖŠ£¬ŅŗŃõĖłĘšµÄ×÷ÓĆŹĒ ”£
£Ø3£©ŠĀ°ę”¶Éś»īŅūÓĆĖ®ĪĄÉś±ź×¼”·ÖŠĖ®ÖŹ¼ģ²āÖø±ź“ÓŌĄ“µÄ35ĻīŌö¼Óµ½106Ļī”£
¢ŁŠĀ±ź×¼ÖŠ¶ŌĖ®µÄpHµÄ¹ę¶ØĪŖ6.5”ÜpH”Ü8.5”£ŹµŃéŹŅÓĆpHŹŌÖ½²āµĆ×ŌĄ“Ė®µÄpH=8£¬ĖµøĆ×ŌĄ“Ė®ĻŌ ŠŌ”£
¢ŚŠĀ±ź×¼ÖŠ¼ÓČėĮĖ¶ŌÓĆ³ōŃõµČĻū¶¾µÄ¹ę¶Ø”£³ōŃõ£ØO3£©ŌŚĻū¶¾¹ż³ĢÖŠ×Ŗ»ÆĪŖŃõĘų£¬³ōŃõ×Ŗ»ÆĪŖŃõĘųŹōÓŚ ±ä»Æ£ØĢīĪļĄķ»ņ»Æѧ£©”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ2018ÄźĖÄ“ØŹ”ĄÖɽŹŠÉ³ĶåĒųÖŠæ¼Ä£Äā»ÆѧŹŌ¾ķ ĢāŠĶ£ŗµ„Ń”Ģā
ĪļÖŹµÄÓĆĶ¾ÓėŠŌÖŹĆÜĒŠĻą¹Ų”£ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ
A.øɱłÓĆÓŚČĖ¹¤½µÓź£¬ŅņĪŖøɱłÉż»ŖĪüČČ
B.»īŠŌĢæÄܹ»³żČ„ŅģĪ¶£¬ŹĒŅņĪŖ»īŠŌĢæ¾ßÓŠĪüø½ŠŌ
C.C”¢CO”¢H2³£ÓĆĄ“Ņ±Į¶½šŹō£¬ŹĒŅņĪŖĖüĆĒ¶¼¾ßÓŠæÉČ¼ŠŌ
D.Ļ“µÓ¼Į³£ÓĆĄ“Ļ“µÓÓĶĪŪ£¬ŹĒŅņĪŖĻ“µÓ¼Į¾ßÓŠČé»Æ¹¦ÄÜ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗŗÓ±±Ź”ĢĘɽŹŠĀ·ÄĻĒų2019-2020ѧğ¾ÅÄź¼¶ÉĻѧʌʌ֊»ÆѧŹŌ¾ķ ĢāŠĶ£ŗæĘѧĢ½¾æĢā
ijŠĖȤŠ”×é¶ŌKClO3·Ö½ā·“Ó¦µÄ“߻ƼĮ½ųŠŠŃŠ¾æ£¬ŌŚĻąĶ¬µÄ¼ÓČČĢõ¼žĻĀ£¬ÓĆĻĀĶ¼×°ÖĆĶź³É±ķÖŠŹµŃé:

±ąŗÅ | KClO3ÖŹĮæ/g | “߻ƼĮ | “߻ƼĮÖŹĮæ/g | ŹÕ¼Æ50mLO2ĖłŠčŹ±¼ä/s |
ŹµŃé1 | 5 | - | - | 171 |
ŹµŃé2 | 5 | MnO2 | 0.5 | 49 |
ŹµŃé3 | 5 | Fe2O3 | 0.5 | 58 |
ŹµŃé4 | 5 | KCl | 0.5 | 154 |
(1)ÉčÖĆŹµŃé1µÄÄæµÄŹĒ___________________
(2)±ķÖŠĖłĮŠ3Ö֓߻ƼĮµÄ“߻Ɗ§¹ū×ī¼ŃµÄŹĒ______________
(3)Š“³öKClO3·Ö½āµÄ»Æѧ·½³ĢŹ½:_________________________
(4)ÓÉŹµŃé1ŗĶŹµŃé4æÉÖŖ£¬KCl____£ØĢī”°ÓŠ”±»ņ”°ĪŽ”±£©“ß»Æ×÷ÓĆ”£Ī¬³Ö¼ÓČČĢõ¼ž²»±ä£¬ÓĆŹµŃé1ŌŁ¼ĢŠųŹÕ¼ÆŹÕ¼Æ50mLO2£¬ĖłŠčŹ±¼äĆ÷ĻŌÉŁÓŚ171s£¬½āŹĶŌŅņ£ŗ_____________
(5)ŅŖ±Č½ĻKClO3·Ö½ā·“Ó¦ÖŠ²»Ķ¬“߻ƼĮµÄ“߻Ɗ§¹ū£¬³żĮĖ²āĮæŹÕ¼Æ50mLO2ĖłŠčŹ±¼äĶā£¬»¹æÉŅŌ²āĮæĻąĶ¬Ź±¼äÄŚ____________
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗŗÓ±±Ź”ĢĘɽŹŠĀ·ÄĻĒų2019-2020ѧğ¾ÅÄź¼¶ÉĻѧʌʌ֊»ÆѧŹŌ¾ķ ĢāŠĶ£ŗµ„Ń”Ģā
ÕįĢĒ£ØC12H22O11£©ŹĒŅ»ÖÖ³£ÓƵď³Ę·ĢšĪ¶¼Į”£ĻĀĮŠ¹ŲÓŚÕįĢĒµÄĖµ·ØÕżČ·µÄŹĒ
A.ÕįĢĒÖŠŗ¬ÓŠ45øöŌ×Ó
B.ÕįĢĒµÄĻą¶Ō·Ö×ÓÖŹĮæŹĒ342g
C.ÕįĢĒÖŠĒāŌŖĖŲµÄÖŹĮæ·ÖŹż×ī“ó
D.ÕįĢĒÓÉĢ¼”¢Ēā”¢ŃõČżÖÖŌŖĖŲ×é³É
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ½ĖÕŹ”ŃĪ³ĒŹŠĶ¤ŗžĒų2019-2020ѧğ¾ÅÄź¼¶ÉĻѧʌʌĩ»ÆѧŹŌ¾ķ ĢāŠĶ£ŗ×ŪŗĻĢā
øÖĢśŹĒÖŲŅŖµÄ½šŹō²ÄĮĻ£¬ŌŚ¹¤Å©ŅµÉś²śŗĶÉś»īÖŠÓ¦ÓĆ·Ē³£¹ć·ŗ”£
I£®ĢśµÄÓ¦ÓĆ
£Ø1£©ĻĀĮŠĢśÖĘĘ·µÄÓ¦ÓĆÓė½šŹōµ¼ČČŠŌÓŠ¹ŲµÄŹĒ_____”£
A Ģś“ø B Ģś¹ų C ²Ėµ¶
£Ø2£©”°ÄÉĆצĮ-Fe·Ū”±æÉŅŌÓĆÓŚŹ³Ę·±£ĻŹ£¬³ĘÖ®ĪŖ”°Ė«Īü¼Į”±£¬ŅņĪŖĖüÄÜĪüŹÕæÕĘųÖŠµÄ_____”£
II£®ĢśµÄŅ±Į¶
¹¤ŅµĮ¶ĢśµÄÖ÷ŅŖ·“Ó¦ŌĄķŹĒŌŚøßĪĀĻĀCO¶įČ”ĢśæóŹÆĄļµÄŃõ£¬½«Ģś»¹Ō³öĄ“”£Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©Š“³öŅŌ³ąĢśæóĪŖŌĮĻ£¬ŌŚøßĪĀĻĀĮ¶ĢśµÄ»Æѧ·½³ĢŹ½£ŗ_____£»
£Ø2£©øßĀÆĮ¶ĢśÖŠ£¬½¹ĢæµÄ×÷ÓĆ³żĮĖæÉŅŌÉś³ÉŅ»Ńõ»ÆĢ¼Ķā£¬»¹ÄÜ_____”£
¢ó£®ĢśµÄ»ī¶ÆŠŌĢ½¾æ
ĻÖÓĆŅ»¶ØĮæµÄAgNO3ŗĶCu £ØNO3£©2»ģŗĻČÜŅŗ£¬½ųŠŠĮĖČēĻĀĶ¼ĖłŹ¾µÄŹµŃ飬²¢¶ŌČÜŅŗAŗĶ¹ĢĢåBµÄ³É·Ö½ųŠŠĮĖ·ÖĪöŗĶŃŠ¾æ”£
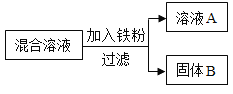
£ØĢį³öĪŹĢā£©ČÜŅŗAÖŠµÄČÜÖŹ³É·ÖæÉÄÜÓŠÄÄŠ©£æ
£Ø×÷³ö²ĀĻė£©
¢ŁÖ»ÓŠFe£ØNO3£©2
¢ŚÓŠFe£ØNO3£©2”¢AgNO3
¢ŪÓŠFe£ØNO3£©2”¢Cu£ØNO3£©2
¢ÜÓŠFe£ØNO3£©2”¢Cu£ØNO3£©2”¢AgNO3
£Ø½»Į÷ĢÖĀŪ£©²»ŗĻĄķµÄ²ĀĻėŹĒ_____£ØĢīŠņŗÅ£©”£
£ØŹµŃéĢ½¾æ£©øł¾ŻĻĀ±ķÖŠµÄŹµŃé²½Öč¼°ĻÖĻó£¬Ķź³É±ķÖŠµÄŹµŃé½įĀŪ”£
ŹµŃé²½Öč | ĻÖĻó | ŹµŃé½įĀŪ |
ȔɣĮæ¹ĢĢåB£¬µĪ¼ÓĻ”ŃĪĖį | ÓŠĘųÅŻ²śÉś | ČÜŅŗAÖŠµÄČÜÖŹ³É·Ö·ūŗĻ²ĀĻė_____£ØĢīŠņŗÅ£©£¬¹ĢĢåBÖŠÓŠ_____ÖÖ½šŹō”£ |
¢ō£®ÉśĢśÖŠĢśŗ¬ĮæµÄ²ā¶Ø
ijæĪĶāŠĖȤŠ”×é²ā¶ØÉśĢś£Øŗ¬ŌÓÖŹµÄĢś£¬ŌÓÖŹ¼Č²»ČÜÓŚĖ®Ņ²²»ČÜÓŚĖį£©ÖŠĢśµÄÖŹĮæ·ÖŹż£¬ĖūĆĒČ”6·ŻŃłĘ·£¬·Ö±šÓėĻ”ĮņĖį·“Ó¦”£²āµĆŹż¾ŻČēĻĀ£¬Ēėøł¾ŻÓŠ¹ŲŠÅĻ¢»Ų“šĪŹĢā”£
ŹµŃé“ĪŹż | 1 | 2 | 3 | 4 | 5 | 6 |
Ȕѳʷ֏Įæ£Øg£© | 30.0 | 30.0 | 30.0 | 30.0 | 30.0 | 30.0 |
Č”Ļ”ĮņĖįÖŹĮæ£Øg£© | 50.0 | 100.0 | 150.0 | 200.0 | 250.0 | 300.0 |
²śÉśĘųĢåÖŹĮæ£Øg£© | 0.2 | 0.4 | 0.6 | 0.8 | 1.0 | 1.05 |
£Ø1£©µŚ5“ĪŹµŃé½įŹųŗó£¬ĖłµĆČÜŅŗÖŠČÜÖŹµÄ»ÆѧŹ½ĪŖ_____”£
£Ø2£©ĖłÓĆĻ”ĮņĖįÖŠČÜÖŹµÄÖŹĮæ·ÖŹżĪŖ_____”£
£Ø3£©ČōÅäÖĘÉĻŹöÅØ¶ČµÄĻ”ĮņĖį100æĖ£¬ŌņŠčÖŹĮæ·ÖŹżĪŖ98%µÄÅØĮņĖį_____æĖ”£
£Ø4£©¼ĘĖćøĆѳʷ֊ĢśµÄÖŹĮæ·ÖŹżŹĒ_____”££ØŠ“³ö¼ĘĖć¹ż³Ģ£©
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com