
分析 找出反应物中化合价升降的元素,化合价升高的元素所在物质前的系数定为化合价降低的元素降低的化合价数,化合价降低的元素所在的物质前的系数定为化合价升高的元素升高的化合价数,然后根据原子守恒依次配平即可.
解答 解:1、Fe(OH)2+O2+H2O═Fe(OH)3反应中:O由0→-2价,降低2价,Fe由+2→+3价,升高1价,根据得失电子数目相等可知二者计量数之比为1:2,由于O2中的氧原子数是2,所以Fe(OH)2前应为4,再根据原子守恒配平化学方程式为4Fe(OH)2+O2+2H2O═4Fe(OH)3;故答案为:4Fe(OH)2+O2+2H2O═4Fe(OH)3;
2、Cu+HNO3(浓)═Cu(NO3)2+NO2↑+H2O反应中:Cu由0→+2价,升高2价,NO2中的氮元素由+5→+4价,降低1价;根据氧化还原反应化合价升降数目相等,所以Cu前配1,NO2前配2(不在HNO3前写上2是因为有一部分的HNO3中的N没有改变化合价;即HNO3在这个反应里一部分充当酸,一部分充当氧化剂);根据元素守恒Cu(NO3)2前配1;计算右边的氮原子有4个,那就在左边的HNO3前配4;最后计算左边的氢原子,氢原子有4个,那么右边H2O前就写上2;故反应的化学方程式为1Cu+4 HNO3(浓)=Cu(NO3)2+2NO2↑+4H2O,
故答案为:Cu+4 HNO3(浓)=Cu(NO3)2+2NO2↑+4H2O;
3、Cu+HNO3(稀)═Cu(NO3)2+NO↑+H2O反应中:Cu由0→+2价,升高2价,NO中的氮元素由+5→+2价,降低3价;根据氧化还原反应化合价升降数目相等,所以Cu前配3,NO前配2(不在HNO3前写上2是因为有一部分的HNO3中的N没有改变化合价;即HNO3在这个反应里一部分充当酸,一部分充当氧化剂);根据元素守恒Cu(NO3)2前配3;计算右边的氮原子有8个,那就在左边的HNO3前配8;最后计算左边的氢原子,氢原子有8个,那么右边H2O前就写上4;故反应的化学方程式为3Cu+8 HNO3=3 Cu(NO3)2+2NO↑+4H2O,
故答案为:3Cu+8 HNO3(稀)=3 Cu(NO3)2+2NO↑+4H2O;
4、镉元素的化合价由+3价升高到+6价,而锰元素的化合价由+7价降低到+2价,根据得失电子数目相等可知二者计量数之比为5:3,由于K2Cr2O7中Cr原子数为2,故CrCl3和KMnO4的计量数分别为10和6,再根据原子守恒配平化学方程式为10CrCl3+6KMnO4+11H2O═3K2Cr2O7+4MnCl2+22HCl+2MnCr2O7;
故答案为:10CrCl3+6KMnO4+11H2O═3K2Cr2O7+4MnCl2+22HCl+2MnCr2O7;
点评 本题难度较大,掌握利用氧化还原反应得失电子守恒进行配平的方法并能灵活运用不同的方法进行配平,如部分氧化还原反应的配平是正确解答本题的关键.


科目:初中化学 来源: 题型:解答题
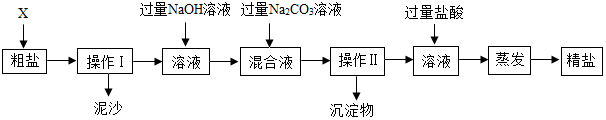
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
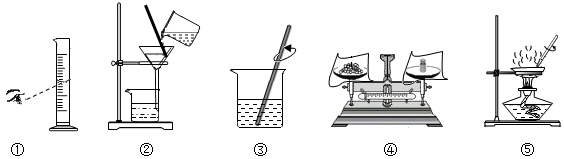
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
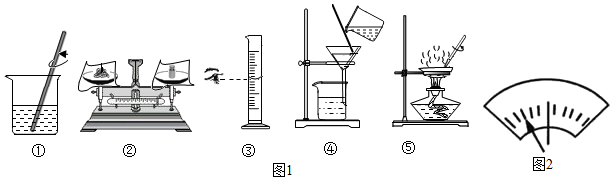
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
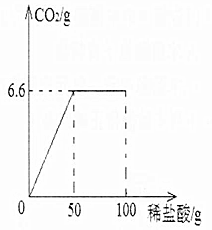 为测定某石灰石样品中碳酸钙的含量,小华同学取20.0g该样品于烧杯中,向其中加入100g稀盐酸,产生气体的质量与稀盐酸的关系如图所示(杂质不与稀盐酸反应,也难溶于水),求:
为测定某石灰石样品中碳酸钙的含量,小华同学取20.0g该样品于烧杯中,向其中加入100g稀盐酸,产生气体的质量与稀盐酸的关系如图所示(杂质不与稀盐酸反应,也难溶于水),求:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | NH4H2PO4 | B. | CO(NH2)2 | C. | K2CO3 | D. | Ca3(PO4)2 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com