
【题目】下列实验操作先后顺序不正确的是()
A.加热碱式碳酸铜固体时,先均匀加热,后集中加热
B.使用胶头滴管吸取液体时,先将胶头滴管伸入液体中,后挤压胶头吸入液体
C.高锰酸钾制取氧气结束时,先熄灭酒精灯,后移导管
D.用托盘天平称量药品时,先调平,后称量
科目:初中化学 来源: 题型:
【题目】碳酸锂是一种重要的锂盐,广泛应用于锂离子电池生产中。工业上可以用锂辉石精矿(主要成分是Li2O、含有Al2O3、SiO2等杂质) 为原料制取高纯的碳酸锂。某校化学活动小组收集了碳酸锂的溶解度数据如表:
温度(℃) | 0 | 20 | 40 | 60 | 80 | 100 |
溶解度(g) | 1.54 | 1.33 | 1.17 | 1.01 | 0.85 | 0.72 |
设计了制取碳酸锂的工艺流程(如图):
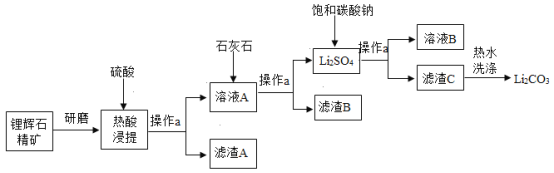
请回答:
(1)操作a所需的玻璃仪器有烧杯、玻璃棒和_____。
(2)热酸浸提中可能发生反应的化学方程式:
①_____;
②Li2O+H2SO4=Li2SO4+H2O。
(3)“洗涤”滤渣C时应该使用热水,其原因是_____。
(4)为了探究热酸浸提的最佳条件,将矿石在一定条件下酸浸4小时,测量锂元素浸出率的部分数据如表:
编号 | 矿酸比 | 硫酸浓度(%) | MgSO4用量(g) | 温度(℃) | 锂元素浸出率(%) |
1 | 1:1 | 90 | 0.00 | 100 | 70.34 |
2 | 1:1 | 98 | 0.00 | 100 | 73.89 |
3 | 1:1 | 98 | 0.00 | 150 | 78.24 |
4 | 1:3 | 98 | 0.00 | 200 | 85.53 |
5 | 1:3 | 98 | 1.25 | 250 | 90.26 |
6 | 1:3 | 98 | 2.50 | 250 | 95.88 |
①对比分析编号1和编号2的实验数据,可以得到的结论是_____。
②有同学想在实验6的基础上,从降低成本角度继续研究提高锂元素的浸出率,下面设计合理的是_____。
A 矿酸比1:2,硫酸浓度98%,MgSO4用量0.00,温度150℃
B 矿酸比1:2,硫酸浓度98%,MgSO4用量2.50,温度200℃
C 矿酸比1:2,硫酸浓度98%,MgSO4用量2.50,温度250℃
D 矿酸比1:3,硫酸浓度98%,MgSO4用量2.00,温度250℃
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】BMH[化学式为Mg2ClO(OH)3·H2O]是一种白色粉末。难溶于水,是常用的无机抗菌剂。BMH的一种生产工艺如图所示。
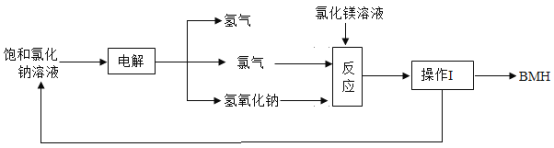
(1)BMH中氯元素的化合价为____价。
(2)流程中操作I的名称为_____。
(3)流程中“反应”步骤生成BMH的化学方程式为_____。
(4)该流程中除水外,可循环利用的物质是_______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】有A、B、C、D四种元素,A元素是人体中含量最多的元素,B元素形成的单质是空气中含量较多且化学性质不活泼的气体,C2+的核外有两个电子层,D元素是人体必需的一种微量元素,如缺少将导致贫血。试回答:
(1)A元素的名称是:_____。
(2)B元素形成的单质的化学式:_____。
(3)D元素的单质在氧气中燃烧的化学方程式为:_____。
(4)A、B、C三种元素组成的化合物的化学式:_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图所示是一个具有刻度和活塞的可滑动玻璃容器,具有空气和足量的白磷,将他盛放在有废水的烧杯上方进行试验(提示:白磷和红磷化学性质类似,其燃点只需达到 40℃)
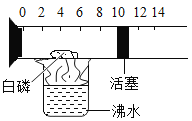
(1)容器内的白磷在沸水的蒸发下燃烧说明燃烧的条件是需要__________
(2)反应结束后,活塞应运动到刻度为_____的位置(假如恰好完全反应)
(3)该实验时使用的白磷量不足,则反应结束后的活塞应运动到较(2)中刻度的_________(选填“偏左”或“偏右”)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列有关![]() 和
和![]() 的知识归纳,正确的是( )
的知识归纳,正确的是( )
A.组成:都是由两种元素组成的,但![]() 比
比![]() 多一个氧元素
多一个氧元素
B.性质:都能溶于水并能与水反应;都能使澄清石灰水变浑浊
C.用途:![]() 可用于光合作用、灭火等;
可用于光合作用、灭火等;![]() 可用于冶炼金属、作燃料
可用于冶炼金属、作燃料
D.危害:![]() 有毒,会造成“温室效应”;
有毒,会造成“温室效应”;![]() 易与血液中的血红蛋白结合引起中毒
易与血液中的血红蛋白结合引起中毒
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(1)空气、水和食物是人类生命活动离不开的物质
①下列行为能导致空气中PM2.5含量增加的是______________(填字母)。
a.大量使用化石燃料 b.露天焚烧垃圾 c.发展轨道交通,低碳出行
②合理搭配饮食是我们的健康理念。比如早餐搭配:牛奶、面包、黄油、水果等,其中含有的营养素有油脂、糖类、___________、维生素、无机盐和水等。
(2)近年比较流行的“自热火锅”给人们生活带来方便。“自热火锅”主要由料包和发热包(主要成分为生石灰、焙烧硅藻土、活性炭、铁粉、铝粉、碳酸钠等)组成,食用方法如图所示。请回答:
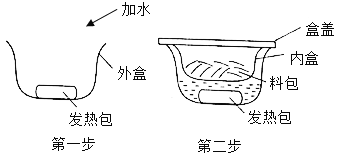
①发热包发热的一种原理是生石灰与水反应放热。反应的化学方程式为____________。
②焙烧硅藻土、活性炭都有疏松多孔的结构,能起到______________作用。
③“自热火锅”的内、外盒由聚丙烯塑料材质制成,随意丢弃会带来______________问题。
(3)东晋葛洪《抱朴子》记载:“以曾青(硫酸铜)涂铁,铁赤色如铜”。请用化学方程式表示其原理____________。
(4)春秋末期齐国的工艺官书《考工记》中载有“洓帛”的方法,即利用“灰(草木灰)和“蜃”(贝壳灰)混合加水所得的溶液来洗涤丝帛。这种溶液能洗涤丝帛主要是因为其中含有______________(写化学式)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列实验方案的设计中,没有正确体现对比这种科学思想的是
A. 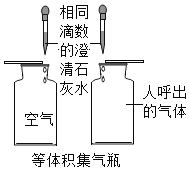 比较二氧化碳的含量
比较二氧化碳的含量
B. 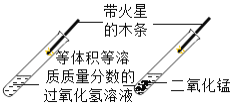 研究二氧化锰的催化作用
研究二氧化锰的催化作用
C.  区分硬水和软水
区分硬水和软水
D. 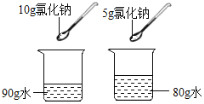 比较氯化钠溶解的快慢
比较氯化钠溶解的快慢
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学兴趣小组对某品牌牙膏中的摩擦剂成分及其含量进行以下探究:
(查得资料)
(1)该牙膏摩擦剂由碳酸钙、氢氧化铝组成;牙膏中其它成分遇到盐酸时无气体产生。
(2)饱和碳酸氢钠溶液不吸收二氧化碳。
(3)碱石灰的主要成分为氧化钙和氢氧化钠。
(设计实验)小组同学设计了如图所示装置(图中夹持仪器略去)测定牙膏样品中碳酸钙的含量。
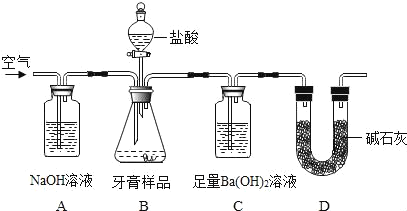
依据图示回答下列问题:
(1)B装置使用分液漏斗的优点是_____。
(2)A中氢氧化钠溶液的作用是_____。
(3)C中观察到有沉淀产生,反应的化学方程式为_____。
(4)实验过程中需持续缓缓通入空气,其作用有_____。
(解释与结论)将C中产生沉淀通过_____、洗涤、干燥、称量,通过计算求得牙膏样品中碳酸钙的含量。
(反思与评价)
反思实验过程,小刚同学提出应采取必要措施,提高测定准确度。他提出的下列各项措施中,不能提高测定准确度的是_____(填字母序号)。
a 在加入盐酸之前,排净装置内的CO2气体
b 放慢滴加盐酸的速度
c 在A﹣B之间增添盛有浓硫酸的洗气装置
d 在B﹣C之间增添盛有饱和碳酸氢钠溶液的洗气装置
(拓展延伸)小亮同学为确定A中溶质成分,进行了如表所示实验:
实验操作 | 实验现象 | 实验结论 |
(1)、取少量滤液于试管中,加入足量____ | 产生白色沉淀 | 溶质主要成分为Na2CO3和NaOH |
(2)、过滤,取少量滤液加入 | _____ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com