(2013?孝感)某化学实验小组同学将铁粉投入硫酸铜溶液中,发现生成红色固体物质的同时有较多的气泡放出.生成的是什么气体呢?同学们决定进行探究.探究前老师提示,该反应生成的气体只有一种.
提出猜想:放出的气体可能是SO
2、O
2、H
2,提出猜想的依据是
质量守恒定律
质量守恒定律
.
查阅资料:SO
2易溶于水,化学性质与二氧化碳有相似之处,它能使澄清石灰水变浑浊,生成CaSO
3.
方案设计:依据上述猜想,实验小组同学分别设计了如下方案:
(1)甲同学认为是O
2,则检验方法是
用带火星的木条检验,看木条是否复燃
用带火星的木条检验,看木条是否复燃
.
(2)乙同学认为是SO
2,则只需将放出的气体通入澄清石灰水中,看澄清石灰水是否变浑浊.写出SO
2与Ca(OH)
2反应的化学方程式
SO2+Ca(OH)2=CaSO3↓+H2O
SO2+Ca(OH)2=CaSO3↓+H2O
.
(3)实验小组同学合作设计了如下组合实验方案,排除和验证猜想的气体.
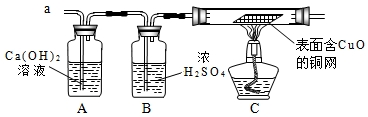
若拆去B装置,直接连接A和C装置进行实验,可能导致
C装置中的硬质玻璃管破裂
C装置中的硬质玻璃管破裂
后果发生.
实验探究:实验开始时,先将收集到的气体从a通入一段时间后,再点燃C处酒精灯;
这样操作的目的是
排出装置内的空气,以防加热时爆炸
排出装置内的空气,以防加热时爆炸
.
实验过程中发现A装置中溶液不变浑浊,C装置中表面含CuO的铜网由黑色变为光亮的红色;
结论:铁粉与硫酸铜溶液反应时,产生的气体是
氢气
氢气
.
思维拓展:由上述实验可以推出,硫酸铜溶液中可能含有
酸
酸
.

 (2013?孝感)某化学小组在课外活动时做了一个实验,在甲试管中装入固体物质,乙试管装入某溶液,按下图所示组装好仪器(图中铁架台等仪器已略去).通过分液漏斗加入足量稀盐酸,同时打开止水夹,看到乙试管溶液中有气泡冒出;再关闭止水夹,发现一段时间后乙中溶液变浑浊.符合此实验现象的一组试剂是( )
(2013?孝感)某化学小组在课外活动时做了一个实验,在甲试管中装入固体物质,乙试管装入某溶液,按下图所示组装好仪器(图中铁架台等仪器已略去).通过分液漏斗加入足量稀盐酸,同时打开止水夹,看到乙试管溶液中有气泡冒出;再关闭止水夹,发现一段时间后乙中溶液变浑浊.符合此实验现象的一组试剂是( )

