
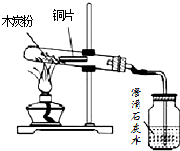
 某小组在探究木炭的还原性时,发现实际操作中,采用氧化铜粉末对实验效果有很大影响,小明同学对木炭还原氧化铜的实验进行了改进,其操作步骤如下:
某小组在探究木炭的还原性时,发现实际操作中,采用氧化铜粉末对实验效果有很大影响,小明同学对木炭还原氧化铜的实验进行了改进,其操作步骤如下:
| ||
| ||
| ||
| ||


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:
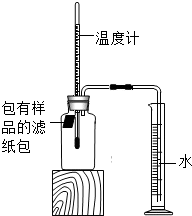 某校化学兴趣小组在探究铁的锈蚀条件后发现该实验耗时较长.为解决此问题,在教师的指导下进行了更深入的探究.探究过程如下:
某校化学兴趣小组在探究铁的锈蚀条件后发现该实验耗时较长.为解决此问题,在教师的指导下进行了更深入的探究.探究过程如下:| 序号 | 样品 | 量筒起始读数/mL | 量筒最终读数/mL | 所需时间/min |
| Ⅰ | 1g铁粉、0.2g木炭粉和10滴水 | 100 | 70 | 约120 |
| Ⅱ | l g铁粉、0.2g木炭粉、10滴水和少量氯化钠 | 100 | 70 | 约70 |
查看答案和解析>>
科目:初中化学 来源: 题型:
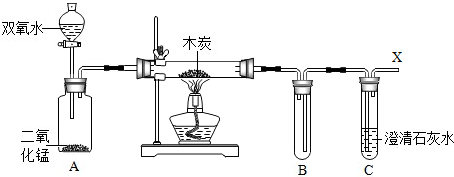
| 步骤 | 操作 | 预计现象及得出的结论 |
| ① | 澄清石灰水未变浑,说明燃烧还需要氧气 | |
| ② | 盖灭酒精灯.待仪器恢复到常温 | / |
| ③ | ||
| ④ | 点燃酒精灯加热,继续通氧气 |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解

| 实验方案 | 实现现象 | 结论 |
| ①取一定量的合金粉末,加过量的 30%NaOH溶液 30%NaOH溶液 ,充分反应后过滤,滤渣备用. |
粉末部分溶解,并有气体放出. | 合金中一定含有 铝 铝 . |
| ②取步骤①所得滤渣,加过量的 10%盐酸 10%盐酸 ,充分反应. |
滤渣部分溶解,并有气体放出,溶液呈浅绿色. | 合金中一定含有 铁和铜 铁和铜 . |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
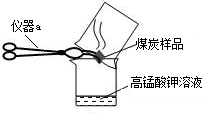
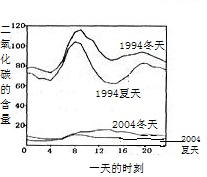
| ||
| ||
 ”.然而化学方程式中最后一种物质的化学式印刷不清楚,根据上下文了解到该物质是一种酸,请根据已学知识推测其化学式:
”.然而化学方程式中最后一种物质的化学式印刷不清楚,根据上下文了解到该物质是一种酸,请根据已学知识推测其化学式:| 测定时间/分钟 | 0 | 1 | 2 | 3 |
| pH | 4.73 | 4.62 | 4.56 | 4.55 |
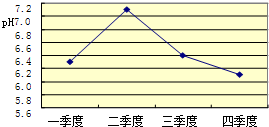
查看答案和解析>>
科目:初中化学 来源:2011年湖北省武汉市部分学校四月调研九年级化学试卷(解析版) 题型:解答题
| 序号 | 样品 | 量筒起始读数/mL | 量筒最终读数/mL | 所需时间/min |
| Ⅰ | 1g铁粉、0.2g木炭粉和10滴水 | 100 | 70 | 约120 |
| Ⅱ | l g铁粉、0.2g木炭粉、10滴水和少量氯化钠 | 100 | 70 | 约70 |

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com