


 ĆūŠ£æĪĢĆĻµĮŠ“š°ø
ĆūŠ£æĪĢĆĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŌĶĮĄķ½ā

| ČÜŅŗÖŠæÉÄÜŗ¬ÓŠµÄĄė×Ó | Éč¼ĘŹµŃéŃéÖ¤£ØŹµŃé²½Öč”¢ĻÖĻó¼°¶ŌÓ¦µÄ½įĀŪ£© |
æÉÄÜŠŌŅ»£ŗBa2+ æÉÄÜŠŌ¶ž£ŗSO42- æÉÄÜŠŌČż£ŗBa2+»ņSO42- æÉÄÜŠŌŅ»£ŗBa2+ æÉÄÜŠŌ¶ž£ŗSO42- æÉÄÜŠŌČż£ŗBa2+»ņSO42- | ¢ŁČ”ÉĻŹöČÜŅŗÉŁĮæÓŚŹŌ¹ÜÖŠ£¬¼ÓČėÉŁĮæĮņĖįÄĘČÜŅŗ£®Čō³öĻÖ°×É«³Įµķ£¬ŌņĖµĆ÷ÉĻŹöČÜŅŗÖŠŗ¬ÓŠBa2+£»Čōƻӊ³öĻÖ°×É«³Įµķ£¬ŌņĖµĆ÷ÉĻŹöČÜŅŗÖŠ²»ŗ¬ÓŠBa2+£®£¬ ¢ŚČ”ÉĻŹöČÜŅŗÉŁĮæÓŚŹŌ¹ÜÖŠ£¬¼ÓČėÉŁĮæĻõĖį±µČÜŅŗ£®Čō³öĻÖ°×É«³Įµķ£¬ŌņĖµĆ÷ÉĻŹöČÜŅŗÖŠŗ¬ÓŠSO42-£»Čōƻӊ³öĻÖ°×É«³Įµķ£¬ŌņĖµĆ÷ÉĻŹöČÜŅŗÖŠ²»ŗ¬ÓŠSO42-£® ¢ŪČ”ÉĻŹöČÜŅŗÉŁĮæÓŚŹŌ¹ÜÖŠ£¬¼ÓČėÉŁĮæĮņĖįÄĘČÜŅŗ£®Čō³öĻÖ°×É«³Įµķ£¬ŌņĖµĆ÷ÉĻŹöČÜŅŗÖŠŗ¬ÓŠBa2+£¬²»ŗ¬ÓŠSO42-£® ¢ŁČ”ÉĻŹöČÜŅŗÉŁĮæÓŚŹŌ¹ÜÖŠ£¬¼ÓČėÉŁĮæĮņĖįÄĘČÜŅŗ£®Čō³öĻÖ°×É«³Įµķ£¬ŌņĖµĆ÷ÉĻŹöČÜŅŗÖŠŗ¬ÓŠBa2+£»Čōƻӊ³öĻÖ°×É«³Įµķ£¬ŌņĖµĆ÷ÉĻŹöČÜŅŗÖŠ²»ŗ¬ÓŠBa2+£®£¬ ¢ŚČ”ÉĻŹöČÜŅŗÉŁĮæÓŚŹŌ¹ÜÖŠ£¬¼ÓČėÉŁĮæĻõĖį±µČÜŅŗ£®Čō³öĻÖ°×É«³Įµķ£¬ŌņĖµĆ÷ÉĻŹöČÜŅŗÖŠŗ¬ÓŠSO42-£»Čōƻӊ³öĻÖ°×É«³Įµķ£¬ŌņĖµĆ÷ÉĻŹöČÜŅŗÖŠ²»ŗ¬ÓŠSO42-£® ¢ŪČ”ÉĻŹöČÜŅŗÉŁĮæÓŚŹŌ¹ÜÖŠ£¬¼ÓČėÉŁĮæĮņĖįÄĘČÜŅŗ£®Čō³öĻÖ°×É«³Įµķ£¬ŌņĖµĆ÷ÉĻŹöČÜŅŗÖŠŗ¬ÓŠBa2+£¬²»ŗ¬ÓŠSO42-£® |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ


²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŌĶĮĄķ½ā
 ĪŅĆĒ¶¼ÖŖµĄCO2ÓėNaOHČÜŅŗŹĒŗÜČŻŅ×·“Ó¦µÄ£¬ĄūÓĆĻĀĶ¼×°ÖĆæɽųŠŠ”°ÅēČŖ”±ŹµŃ飮°“Ķ¼l½ųŠŠŹµŃéµÄ²½ÖčŹĒ£ŗŹ×ĻČŌŚŌ²µ×ÉÕĘæÖŠ³äĀśøÉŌļµÄCO2ĘųĢ壬ŌŚ½ŗĶ·µĪ¹ÜÖŠĪüĀśNaOHČÜŅŗ£Ø×¢Ņā£ŗŅ»°ćĒéæöĻĀ²»ÄÜČē“Ė±ćÓĆ½ŗĶ·µĪ¹Ü£©£¬°“Ķ¼1Į¬½ÓŗĆ×°ÖĆ£¬²¢¹Ģ¶ØŌŚĢś¼ÜĢØÉĻ£®Č»ŗó“ņæŖÖ¹Ė®¼Š£¬½«½ŗĶ·µĪ¹ÜÖŠµÄNaOHČÜŅŗ¼·ČėÉÕĘæÄŚ£®ŌŚµ¼¹ÜµÄ¼ā×ģ“¦¾Ķ»įŠĪ³ÉĆĄĄöµÄ”°ÅēČŖ”±£®
ĪŅĆĒ¶¼ÖŖµĄCO2ÓėNaOHČÜŅŗŹĒŗÜČŻŅ×·“Ó¦µÄ£¬ĄūÓĆĻĀĶ¼×°ÖĆæɽųŠŠ”°ÅēČŖ”±ŹµŃ飮°“Ķ¼l½ųŠŠŹµŃéµÄ²½ÖčŹĒ£ŗŹ×ĻČŌŚŌ²µ×ÉÕĘæÖŠ³äĀśøÉŌļµÄCO2ĘųĢ壬ŌŚ½ŗĶ·µĪ¹ÜÖŠĪüĀśNaOHČÜŅŗ£Ø×¢Ņā£ŗŅ»°ćĒéæöĻĀ²»ÄÜČē“Ė±ćÓĆ½ŗĶ·µĪ¹Ü£©£¬°“Ķ¼1Į¬½ÓŗĆ×°ÖĆ£¬²¢¹Ģ¶ØŌŚĢś¼ÜĢØÉĻ£®Č»ŗó“ņæŖÖ¹Ė®¼Š£¬½«½ŗĶ·µĪ¹ÜÖŠµÄNaOHČÜŅŗ¼·ČėÉÕĘæÄŚ£®ŌŚµ¼¹ÜµÄ¼ā×ģ“¦¾Ķ»įŠĪ³ÉĆĄĄöµÄ”°ÅēČŖ”±£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŌĶĮĄķ½ā

| ČÜŅŗÖŠæÉÄÜŗ¬ÓŠµÄĄė×Ó | Éč¼ĘŹµŃéŃéÖ¤£ØŹµŃé²½Öč”¢ĻÖĻó¼°¶ŌÓ¦µÄ½įĀŪ£© |
æÉÄÜŗ¬SO42- æÉÄÜŗ¬SO42- |
Č”ÉĻŹöČÜŅŗÉŁĮæÓŚŹŌ¹ÜÖŠ£¬¼ÓČėÉŁĮæĻõĖį±µČÜŅŗ£®Čō³öĻÖ°×É«³Įµķ£¬ŌņĖµĆ÷ŗ¬ÓŠSO42-£»Čōƻӊ³öĻÖ°×É«³Įµķ£¬ŌņĖµĆ÷ÉĻŹöČÜŅŗÖŠ²»ŗ¬ÓŠSO42-£® Č”ÉĻŹöČÜŅŗÉŁĮæÓŚŹŌ¹ÜÖŠ£¬¼ÓČėÉŁĮæĻõĖį±µČÜŅŗ£®Čō³öĻÖ°×É«³Įµķ£¬ŌņĖµĆ÷ŗ¬ÓŠSO42-£»Čōƻӊ³öĻÖ°×É«³Įµķ£¬ŌņĖµĆ÷ÉĻŹöČÜŅŗÖŠ²»ŗ¬ÓŠSO42-£® |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŌĶĮĄķ½ā
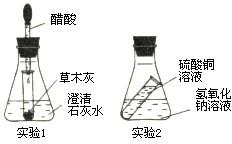 ŹµŃéĢ½¾æ£ŗĻĀĮŠŹµŃé1ŗĶŹµŃé2·“Ó¦Ē°ŗóĢģĘ½ŹĒ·ńĘ½ŗā£æĒė»Ų“šĪŹĢā£ŗ
ŹµŃéĢ½¾æ£ŗĻĀĮŠŹµŃé1ŗĶŹµŃé2·“Ó¦Ē°ŗóĢģĘ½ŹĒ·ńĘ½ŗā£æĒė»Ų“šĪŹĢā£ŗ| ŹµŃ鱹ŗÅ | ŹµŃé1 | ŹµŃé2 |
| ŹµŃéĻÖĻó | Š”ŹŌ¹ÜÖŠÓŠĘųÅŻ²śÉś£¬³ĪĒåŹÆ»ŅĖ®±ä»ė×Ē Š”ŹŌ¹ÜÖŠÓŠĘųÅŻ²śÉś£¬³ĪĒåŹÆ»ŅĖ®±ä»ė×Ē |
ÓŠĄ¶É«Šõד³ĮµķÉś³É ÓŠĄ¶É«Šõד³ĮµķÉś³É |
»Æѧ·½³ĢŹ½ |
K2CO3+2HAc=2KAc+H2O+CO2”ü Ca£ØOH£©2+CO2=CaCO3”ż+H2O K2CO3+2HAc=2KAc+H2O+CO2”ü Ca£ØOH£©2+CO2=CaCO3”ż+H2O |
CuSO4+2NaOH=Cu£ØOH£©2+Na2SO4 CuSO4+2NaOH=Cu£ØOH£©2+Na2SO4 |
| ·“Ó¦Ē°ŗóĢģĘ½ŹĒ·ńĘ½ŗā | Ę½ŗā Ę½ŗā |
Ę½ŗā Ę½ŗā |
| ÄćµÄ½įĀŪ | »Æѧ·“Ó¦Ē°ŗ󣬲Ī¼Ó·“Ó¦ĪļÖŹµÄ×ÜÖŹĮæµČÓŚÉś³ÉĪļÖŹµÄ×ÜÖŹĮæ »Æѧ·“Ó¦Ē°ŗ󣬲Ī¼Ó·“Ó¦ĪļÖŹµÄ×ÜÖŹĮæµČÓŚÉś³ÉĪļÖŹµÄ×ÜÖŹĮæ |
»Æѧ·“Ó¦Ē°ŗ󣬲Ī¼Ó·“Ó¦ĪļÖŹµÄ×ÜÖŹĮæµČÓŚÉś³ÉĪļÖŹµÄ×ÜÖŹĮæ »Æѧ·“Ó¦Ē°ŗ󣬲Ī¼Ó·“Ó¦ĪļÖŹµÄ×ÜÖŹĮæµČÓŚÉś³ÉĪļÖŹµÄ×ÜÖŹĮæ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com