
如图是甲、乙两种固体的溶解度曲线.下列说法中正确的是( )
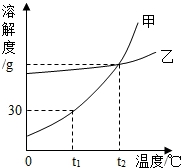
A.甲的溶解度小于乙的溶解度
B.t1℃时,50g水中最多溶解15g甲
C.t2℃时乙的饱和溶液降温至t1℃变为不饱和溶液
D.将t1℃时甲的饱和溶液升温至t2℃,溶质的质量分数增大
【考点】固体溶解度曲线及其作用.
【专题】溶液、浊液与溶解度.
【分析】A、比较物质的溶解度大小须确定温度;
B、据t1℃时甲的溶解度分析解答;
C、据乙的溶解度随温度的降低的变化情况分析判断;
D、据甲的溶解度随温度的升高溶解度变化及溶质的质量分数计算方法分析解答.
【解答】解:A、不知温度,无法比较甲、乙溶解度大小,故错误;
B、t1℃时甲的溶解度是30g,所以该温度下50g水中最多溶解15g甲,正确;
C、乙的溶解度随温度的降低而减小,所以t2℃时乙的饱和溶液降温至t1℃依然是饱和溶液,故错误;
D、甲的溶解度随温度的升高而增大,溶质质量分数= ×100%,所以将t1℃时甲的饱和溶液升温至t2℃,溶质、溶剂的质量不变,溶质的质量分数不变,故错误;
×100%,所以将t1℃时甲的饱和溶液升温至t2℃,溶质、溶剂的质量不变,溶质的质量分数不变,故错误;
故选B.
【点评】本题考查了溶解度曲线意义的应用,能较好考查学生应用知识分析、解决问题的能力.


 举一反三期末百分冲刺卷系列答案
举一反三期末百分冲刺卷系列答案科目:初中化学 来源: 题型:
某兴趣小组做以下实验探究分子的运动:

(1)实验(如图1所示):烧杯B中出现什么现象: ,产生这一现象的原因是:
(2)为使实验结论准确可靠,该兴趣小组设计了实验(如图2所示)作为对比实验,你认为有无必要?说明理由 .
查看答案和解析>>
科目:初中化学 来源: 题型:
某同学设计了测定空气中氧气含量的实验,实验装置如图所示:该同学的实验步骤如下:

①将图中的集气瓶分为5等份,并做好标记.
②在带橡皮塞和导管的燃烧匙内装入足量的红磷,将导管上的止水夹夹紧 ,在酒精灯上点燃红磷,并立即伸入集气瓶内,塞紧橡皮塞.
,在酒精灯上点燃红磷,并立即伸入集气瓶内,塞紧橡皮塞.
③充分反应后,待集气瓶冷却至室温,打开止水夹.
请回答下列问题:
(1)该实验中红磷须稍过量,目的是 ;
(2)步骤③中,打开止水夹后观察到的现象是 ,由此可得出空气中氧气的体积分数约为 .
(3)磷在空气中燃烧生成的氧化物通常可做强干燥剂.已知在标准状况下,32g氧气的体积是22.4L.在该条件下,制备71g这种干燥剂所消耗的空气的体积约为 L.
查看答案和解析>>
科目:初中化学 来源: 题型:
下列有关实验的叙述正确的是( )
A.“CO2的制取与性质”实验中,用燃着的木条放在集气瓶口检验CO2是否集满
B.“物质燃烧的条件”实验中,用玻璃杯罩住燃着的蜡烛以降低蜡烛的着火点
C.“配置一定溶质质量分数的NaCl溶液”实验中,把食盐放在托盘天平右盘称量
D.“溶液的酸碱性”实验中,测定溶液pH时将试纸预先用水湿润
查看答案和解析>>
科目:初中化学 来源: 题型:
阅读下面科普短文.
氨(NH3)常用来制化肥和硝酸,但是科学家们发现它还是一种很有前景的燃料.
现有的化石燃料燃烧时,都会产生温室气体CO2,而氨燃烧时生成N2和H2O两种对环境友好的产物.氨价格低、制造技术成熟,便于普及使用.传统的工业合成氨是将氮气和氢气在20~50MPa的高压和500℃的高温条件下,用铁作催化剂合成的.
氨很容易液化,将氨常温下加压到1MPa,或者常压下温度降到﹣33℃,均可将其液化.而为了获得含有相同能量的液态氢(H2),常温下需要136MPa的压力来压缩它,显然超出了车载燃料储存的压力极限.
氨虽然有毒,但氨具有强烈的刺激性气味,一旦发生泄漏,达到人们觉察到时浓度的1000倍才会致命,因此很容易被发现并及时补救.氨比空气轻,泄漏后扩散快,不会聚积.泄漏在大气中的氨还可以参与自然循环,随雨雪移动后,与其他物质反应或被植物吸收.
依据文章内容,回答下列问题.
(1)化石燃料都会生成CO2的原因是 .
(2)文中提到氨的物理性质有 (答出两点).
(3)从阅读材料中可以看出,将气体液化的途径有 .
(4)请写出氨燃烧生成N2和H2O的化学方程式 .
(5)德国化学家格哈德•埃特尔在固体表面化学的研究中取得了非凡的成就,其成果之一是揭示了氮气与氢气在催化剂表面合成氨的反应过程.下图为该过程的微观示意图(图中  表示氮原子,
表示氮原子, 表示氢原子,
表示氢原子, 表示催化剂).符合上述反应过程的顺序是
表示催化剂).符合上述反应过程的顺序是
(填字母序号).

A.⑤④①③②B.④⑤①②③C.④⑤①③②D.⑤④①②③
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com