
科目: 来源: 题型:解答题
 随着科技的进步,食品防腐技术在不断发展.
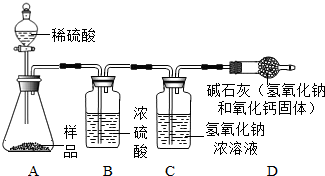
随着科技的进步,食品防腐技术在不断发展. 实验A中观察到的现象是______,反应的化学方程式为______.实验B观察到溶液由浅绿色变为黄色,小明设计上述实验的目的是______.
实验A中观察到的现象是______,反应的化学方程式为______.实验B观察到溶液由浅绿色变为黄色,小明设计上述实验的目的是______.查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
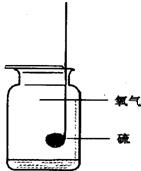 在燃烧匙里放入少量硫,加热,直到发生燃烧,然后把它伸进充满氧气的集气瓶里.如图所示,请回答下列问题:
在燃烧匙里放入少量硫,加热,直到发生燃烧,然后把它伸进充满氧气的集气瓶里.如图所示,请回答下列问题:查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:填空题
| 品名 熟黑芝麻 包装材料:OPP、CPP 营养成分:(100g) |
| 糖类≥15 g |
| 磷≥350mg |
| 铁≥12mg |
| 脂肪≥52g |
| 蛋白质≥20g |
| 钙≥1.5g |
| 维生素E≥30mg |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:填空题
| 实验操作 | 实验现象 | 实验结论 | |
| 方案一 | 取少量固体放入试管中,滴加几滴稀盐酸 | 无明显现象 | 猜想1正确 |
| 方案二 | 取少量固体放入试管中加水溶解,滴加足量澄清石灰水 | 产生白色沉淀 | 猜想2正确 |
| 取上层清液放入另一只试管中,滴加酚酞溶液 | 溶液变为红色 |
| 实验操作 | 实验现象 | 实验结论 |
| 取少量固体放入试管中加水溶解,滴加足量________ | 产生白色沉淀 | 猜想2正确 |
| 取上层清液放入另一只试管中,滴加酚酞溶液 | ________ |
查看答案和解析>>
科目: 来源: 题型:解答题
| 反应前 | 反应前 | 反应后 | |
| 实 验 数 据 | 烧杯和稀盐酸的质量 | 石灰石样品的质量 | 烧杯中混合物的质量 |
| 150g | 12g | 157.6g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com