
科目: 来源:化学教研室 题型:058
某化学兴趣小组按以下步骤探究某一温度下氯化钠饱和溶液的酸碱度.
〔猜想与假设〕溶液的
pH可能为(请将你的假设填入空格中):①pH<7,②_______,③______.〔设计与实验〕要测定该溶液的酸碱度,除有正确的操作步骤外,其中不能采用下列物质中的
______(填序号)来进行实验.①
pH试纸②紫色石蕊试液③酚酞试液组内同学进行了如下实验.
甲同学:取
pH试纸放在玻璃片上,用玻璃棒蘸取氯化钠溶液沾在pH试纸上,把试纸显示的颜色与标准比色卡比较,测得pH=7.乙同学:取
pH试纸放在玻璃片上,先用蒸馏水将pH试纸湿润,然后用玻璃棒蘸取氯化钠溶液沾在pH试纸上,把试纸显示的颜色与标准比色卡比较,测得pH=7.丙同学:将
pH试纸直接浸入氯化钠溶液中,把试纸显示的颜色与标准比色卡比较,测得pH=7.〔评论〕三位同学中操作规范的是
________同学.指出其余同学操作上的错误_______________________________________________________.〔结论和分析〕丙同学得出:“凡是盐溶液的
pH都等于7”,你认为该结论是否正确?_______,如不正确请你举例说明(如正确,此空不用填)________.查看答案和解析>>
科目: 来源:化学教研室 题型:058
某同学想用
pH试纸分别测定食盐水、稀盐酸、氢氧化钠溶液的pH.他的操作如下:在玻璃片上依次放好三片pH试纸,先用蒸馏水将三片pH试纸润湿后,将被测的三种溶液分别滴到三片pH试纸上,把试纸显示的颜色与标准比色卡比较,得出三种溶液的pH.请你:(1)
指出他操作上的错误;(2)
具体分析他测得三种溶液的pH与三种溶液实际pH的关系.查看答案和解析>>
科目: 来源:化学教研室 题型:058
已知:常温下二氧化硫是无色气体,它能与水反应生成亚硫酸
(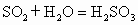 ),亚硫酸的酸性比碳酸的酸性要强.为了验证二氧化硫能与水发生反应,请你共同来研究.
),亚硫酸的酸性比碳酸的酸性要强.为了验证二氧化硫能与水发生反应,请你共同来研究.
(1)
要验证二氧化硫气体能与水反应,你认为最好用下述中的_______(填选项编号)方法来证明.[
]|
A .讨论 |
B .调查 |
C .实验 |
(2)
甲同学用图所示的方法,将二氧化硫气体通入到紫色石蕊试液中,观察溶液颜色的变化.他得出:紫色石蕊试液会变______色,证明二氧化硫能与水反应.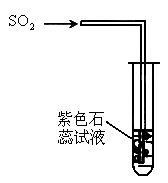
(3)
乙同学用紫色石蕊试液将白色滤纸染咸紫色,干燥后扎成了四只紫色蝴蝶,然后分别进行如下实验:①一只喷洒稀酸;②一只喷水;③一只直接放入盛有二氧化硫气体的集气瓶中;④一只喷洒水后放入盛有二氧化硫的集气瓶中.
在乙同学的实验中,紫色小蝴蝶不会变色的是
________、________(填实验编号).(4)
你觉得甲、乙同学的方案相比,哪个更好?______,你的理由:_______.(5)
你还有其他方案吗?如有,说出你的一种方案.操作:_______.现象结论;_______.查看答案和解析>>
科目: 来源:化学教研室 题型:058
某同学用石蕊试纸检验某溶液
A的酸碱性,实验如下:(1)
将溶液A滴在红色石蕊试纸上,试纸未变蓝,则溶液A可能显什么性?______;(2)
将溶液A滴在蓝色石蕊试纸上,试纸未变红,则溶液A可能显什么性?______;(3)
溶液A的pH范围是______,应该用什么方法测定它的酸碱度?简述其操作步骤:___________________________.查看答案和解析>>
科目: 来源:化学教研室 题型:058
现有
24%的硝酸钾溶液、2%的硝酸钾溶液、硝酸钾固体和水.请选用上述不同物质配制10%的硝酸钾溶液,将用量的最简整数比填入下表中相应的位置.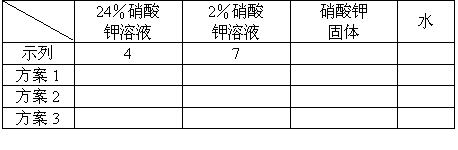
查看答案和解析>>
科目: 来源:化学教研室 题型:058
在实验室配制溶液时,常涉及以下过程:①称量、量取②过滤③蒸发结晶、干燥④计算⑤溶解
请你按要求回答下列问题:
(1)
甲同学用氯化钠和蒸馏水配制50g5%的氯化钠溶液,正确的操作顺序是________(用以上序号填空),现实验中有10mL、50mL、100mL等不同规格的量筒,配制上述溶液时最好选用______mL的量筒.(2)
乙同学用10g含杂质10%的食盐(杂质不溶于水)和蒸馏水配制50g5%的氯化钠溶液,正确的操作顺序是____________(用以上序号填空).查看答案和解析>>
科目: 来源:化学教研室 题型:058
实验室里有一瓶标签残缺的盐酸,请你来共同探究.
(1)怎样立即确定它是不是浓盐酸?有人猜测是,有人记得好像不是,大家各抒己见.你认为应该用下述中的____________(填选项编号)方法立即确认.[
]|
A .讨论 |
B ,调查 |
|
C .实验 |
D .上网 |
(2)
粗略测定该盐酸每毫升溶液中含溶质HCl的质量.同学们依据酸和碱中和反应的原理,设计了一种可行的实验方案,其操作步骤如下:第
1步,在小烧杯中滴加10g5%的NaOH溶液;第
2步,向上述烧杯中滴入2滴酚酞试液;第
3步,向10mL的量筒里注入该盐酸至一定刻度;第
4步,用胶头滴管吸取量筒中的盐酸,逐滴滴入上述烧杯中,……一直滴到溶液由红色刚刚变为无色为止;第
5步,记录实验数据;第
6步,计算,确定每毫升盐酸中含有溶质HCl的质量.请根据以上实验过程,回答下列问题:①本实验为什么要用指示剂
(酚酞)?_________________________.②第
3步中向量筒中注入盐酸,量筒中液面的位置如图所示,A与B、B与C刻度均相差1mL,如果刻度A为8,量筒中盐酸的体积是_____mL.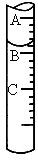
③第
4步要用玻璃棒,它的作用是_______,目的是__________.停止滴入盐酸后,胶头滴管中残留的盐酸应________________.④第
5步要记录的实验数据是___________________________.(3)
测定每毫升该盐酸中含溶质HCl的质量,有人提出用KOH等碱类试剂代替上述NaOH溶液与盐酸进行中和反应,测定耗去的盐酸的体积,通过计算确定盐酸中HCl的含量,这和上述实验属于同一种方法;你能写出其他可行的方法吗?若能,请写在下面(用文字简述所依据的原理和要测定的数据,不需要写出化学方程式).___________________________________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com