
科目: 来源:2006~2007学年度第一学期九年级期末调研考试 化学 题型:059
完成下列研究性学习的有关内容;探究氯酸钾和二氧化锰混合物中氯酸钾的质量分数.
[研究方案]先称取一定质量的氯酸钾和二氧化锰混合物,放入大试管中加热至质量不再变化为止.根据质量守恒定律,固体物质减轻的质量即为产生氧气的质量,从而求出氯酸钾的质量.(学习小组同学事先查阅资料获知,二氧化锰的质量在反应前后不变且在水中难溶)
[解决问题]实验测得固体混合物质量随加热时间变化的相关数据如下图所示.请你完成下表:
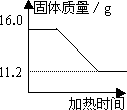
[继续研究]为了分离回收二氧化锰和氯化钾,他们在反应后的固体混合物中加入80g水使其中的氯化钾完全溶解,然后通过过滤二氧化锰与液体分离.请你计算他们得到的滤液中氯化钾的质量分数.(过滤中水的损失不计).
查看答案和解析>>
科目: 来源:2006~2007学年度第一学期九年级期末调研考试 化学 题型:059
| |||||||||||
查看答案和解析>>
科目: 来源:吴中区2006~2007学年第一学期期末考试(初三化学)-上教版 题型:059
当我们将CO2通入NaOH溶液中,发现无明显现象.那么CO2和NaOH是否发生了化学反应呢?某同学设计了如下实验方案进行了科学探究,请你帮他完成表中内容:
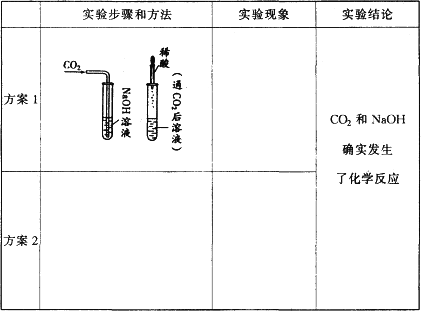
写出方案2中的有关化学反应方程式:________;________.
查看答案和解析>>
科目: 来源:苏州相城区2006-2007学年度第一学期初三年级期末测试卷(化学) 题型:059
探究影响化学反应速率的因素.
(1)发现和提出问题∶
化学反应有的很快,如爆炸,有的相当慢,如铁生锈.决定物质之间能否反应以及化学反应速率快慢的内因是反应物的结构和性质.除此以外,催化剂也能改变化学反应速率.
同学们都有这样的生活经验,木炭在氧气中燃烧比在空气中燃烧的旺∶这说明反应物的浓度对化学反应速率有影响.夏天,将食品放在冰箱里不容易腐烂;这说明温度对化学反应速率也有影响.那么,温度和浓度是如何影响化学反应速率?
(2)猜想与假设∶a.浓度越大,化学反应的速率越快.
b.温度越高,化学反应的速率越快.
(3)收集证据∶
实验仪器和试剂∶试管、试管夹、酒精灯、药匙、量筒;锌粒、5%盐酸、20%盐酸.
利用上述实验仪器和试剂进行探究,如果假设是a,你认为需要控制的变量有________.
如果假设是b,你认为需要控制的变量有________.
在实验中,通过观测________来判断反应的快慢.
(4)结论与解释∶实验证明,条件相同,盐酸的溶质质量分数越大,与金属的反应速率越快.其它条件相同,温度越高,化学反应的速率越快.从反应物的微观粒子相互作用角度,你认为其原因分别是________和________
(5)交流与反思∶通过实验探究我们知道,我们可以通过控制反应条件来控制化学反应的快慢.请你再举出一个通过控制化学反应条件来控制化学反应快慢的事例.________
查看答案和解析>>
科目: 来源:苏州相城区2006-2007学年度第一学期初三年级期末测试卷(化学) 题型:059
某同学学习了铁合金后很感兴趣,他从家中取来了铁制品样品,经除锈打磨处理后,在老师的帮助下,在实验室进行了铁的质量分数测定,他取2.3克样品,放在烧杯中,然后滴加19.6%的稀硫酸到不再产生气泡为止,共计消耗稀硫酸20克,该同学作了计算和探究.
(1)该铁制品是生铁还是钢?(生铁的含碳量为2%~4.3%,钢的含碳量为0.03%~2%)
(2)反应后所得溶液溶质质量分数为多少?
(3)该同学做完实验后,没有象往常一样将废液倒在废液杯中,他认为废液不废,作为同伴,你是否赞同他的观点?为什么?
(4)如何回收所得溶液中的溶质?
查看答案和解析>>
科目: 来源:江苏省名校济川中学2006-2007秋学期初三期末考试化学试题 题型:059
| |||||||||||||||||||||||||||||
查看答案和解析>>
科目: 来源:2007北京丰台初三化学第一学期期末试题-新人教 题型:059
某研究小组对用H2O2分解生成H2O和O2的实验条件进行探究.他们进行了以下实验:
①往盛有5 mL 5%H2O2溶液的试管中,伸入带火星的木条,木条不复燃.
②往盛有5 mL w%H2O2溶液的试管中,加入a g MnO2,伸入带火星的木条,木条复燃.
③往盛有5 mL w%H2O2溶液的试管中,加入a g Fe2O3,伸入带火星的木条,木条复燃.
④经检验,②、③中反应后试管中仍分别含有a g MnO2和a g Fe2O3.
问题:(1)MnO2、Fe2O3在上述反应中的作用是________.
(2)实验②、③中H2O2的浓度(w%)以________为宜,你的理由是________.
(3)写出实验②化学反应的方程式________.
研究小组还对溶液浓度、催化剂的种类等实验条件进行了探究.下表选取了部分实验数据:
用足量等体积H2O2溶液制取相同体积O2所需的时间
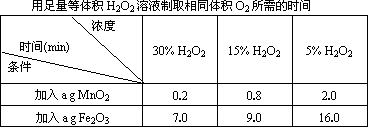
问题:(4)从上表中能得出哪些结论?
①________;
②________;
(5)再写出一个用MnO2作催化剂的化学反应方程式________.
查看答案和解析>>
科目: 来源:2006-2007学年上学期月考初三化学 题型:059
| |||||||||||||||
查看答案和解析>>
科目: 来源:2006-2007年度省港中、江大附中、华南实验学校三校九年级期中化学联考试卷 题型:059
同学们在淡水养殖场参观时,好奇的发现农民向鱼池中撒一种微黄色的固体,咨询得知,这种固体的主要成分是过氧化钙(CaO2),它和水反应时产生氧气,以增加鱼池中氧气的含量.
同学们对过氧化钙和水反应的产物进行了探究:
[提出问题一]把少量过氧化钙投入足量水中,在产生氧气的同时还产生什么物质?
[猜想与验证一](1)小明同学认为:在产生氧气的同时还产生氧化钙
(2)小红同学认为:在产生氧气的同时还产生氢氧化钙
同学们认为小明的猜想不合理,理由是________;
请设计一个实验方案来验证小红的猜想是正确的,并填入下表空格中:

同学们已学习了氧气的实验室制法,于是他们又作了进一步的探究:
[提出问题二]在实验室,过氧化钙能否用于制取氧气?
[查阅资料]过氧化钙常温下稳定,300℃时能分解产生氧气;
[猜想与验证二]小明同学依据________,提出猜想
猜想:加热CaO2能用于实验室制取氧气
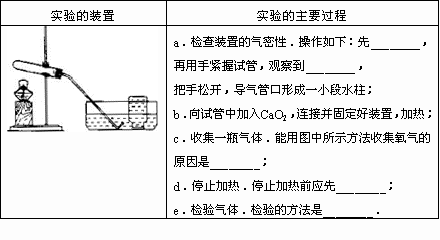
小明又联系到农民用过氧化钙增加鱼池中氧气的含量,提出猜想
猜想:过氧化钙和水反应能用于实验室制取氧气

[实验结论]加热CaO2能用于实验室制取氧气;CaO2和水反应不能用于制取氧气.
[分析与反思]用过氧化钙和水反应虽然收集不到大量的氧气,但由实验的现象分析,农民用过氧化钙和水反应以增加鱼池中氧气的含量的原因是________;
小明想改进实验以加快反应的速度,请你提出一条改进的方法________;
过氧化钠与水反应的原理:2Na2O2+2H2O=4NaOH+O2↑,且CaO2与Na2O2的化学性质非常相似.写出CaO2与H2O反应的化学方程式________.
查看答案和解析>>
科目: 来源:2006-2007年度兰州市第一学期期末考试九年级化学试卷(鲁教版) 题型:059
实验探究:KOH和NaOH有相似的化学性质.为准备KOH和稀盐酸的中和反应实验,小宇特地在几天前配制了氢氧化钾溶液.实验时,向氢氧化钾溶液中慢慢滴加稀盐酸一段时间后,小宇惊奇地发现溶液中有气泡逸出.
(1)提出问题:小宇同学感到惊奇的原因有:①产生的气体是什么气体?为什么产生这种气体?②为什么在滴加稀盐酸“一段时间”后,才产生这种气体?
(2)针对第二个问题:小宇进行了如下分析,久置于空气中的氢氧化钾溶液中主要有________ ________ ________三种离子.他猜想,问题②中的现象最有可能是________离子引起的.
(3)实验探究:为验证针对第二个问题提出的猜想,请你帮助小宇选择________和________试剂进行对比实验,观察出现________现象,即可证明猜想正确.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com