
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
| 第一组 | 第二组 | 第三组 | |||||||||
| 集气瓶编号 | ① | ② | ③ | ④ | ⑤ | ① | ② | ③ | ④ | ⑤ | ① |
| 收集的O2占容积的体积分数(%) | 10 | 20 | 30 | 40 | 50 | 31 | 33 | 35 | 37 | 39 | 34 |
| 带火星木条的状况 | 微亮 | 亮 | 很亮 | 复燃 | 复燃 | 很亮 | 很亮 | 复燃 | 复燃 | 复燃 | 很亮 |
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:解答题
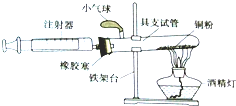 某化学小组在实验室利用自己设计的装置(如图)测定空气中氧气的含量.
某化学小组在实验室利用自己设计的装置(如图)测定空气中氧气的含量.查看答案和解析>>
科目: 来源: 题型:解答题
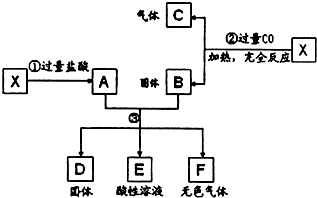 已知X为FeO和CuO的混合物,取两份等质量的X样品如右图所示的实验:设③中所得固体D的质量为32克,溶液E中只含有一种金属离子,且有酸剩余,气体F的质量为0.5克,试计算取用的每份X的质量,及X中FeO和CuO的质量比.
已知X为FeO和CuO的混合物,取两份等质量的X样品如右图所示的实验:设③中所得固体D的质量为32克,溶液E中只含有一种金属离子,且有酸剩余,气体F的质量为0.5克,试计算取用的每份X的质量,及X中FeO和CuO的质量比.查看答案和解析>>
科目: 来源: 题型:解答题


查看答案和解析>>
科目: 来源: 题型:解答题
| 总热量 | 蛋白质 | 糖类 | 油脂 | 水 | 钠 | 磷 | 钙 |
| 2060KJ | 50g | 20g | 待测 | 5g | 4.6g | 3.3g | 8mg |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com