
科目: 来源:四川省德阳市2007年初中毕业生学业考试化学试题 题型:038
某校化学实验室有一瓶标签残缺的过氧化氢溶液(如图所示).该校化学课外兴趣小组的同学为了测定其中溶质的质量分数,他们取出该溶液34 g,加入适量催化剂,待完全反应后,共收集到0.32 g氧气.试计算该溶液中溶质的质量分数.

查看答案和解析>>
科目: 来源:四川省达州市2007年高中阶段教育学校招生统一考试化学试题 题型:038
某研究性学习小组欲测定含硫酸的废液中硫酸的溶质质量分数,做了如下实验:向100 g该废液中加入足量的废铁屑,充分反应后,收集到氢气0.2 g(假如废液中其他成分不与废铁屑反应).请你计算该废液中硫酸的溶质质量分数?(要求写出计算过程)
查看答案和解析>>
科目: 来源:山东省济南市2007年高中阶段教育学校统一招生考试化学试卷 题型:038
在一烧杯中盛有22.3 g Na2CO3和NaCl组成的固体混合物,加足量水溶解,制成溶液.向其中逐渐滴加溶质质量分数为10%的稀盐酸,放出气体的总质量与所滴入稀盐酸的质量关系曲线如图所示:
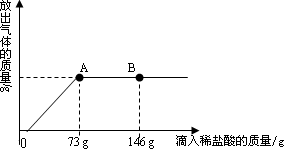
请根据题意回答问题:
(1)当滴加了73 g稀盐酸时,放出气体的总质量为________g.
(2)当滴加稀盐酸至图中B点时,烧杯中溶液里的溶质是(写化学式)________.
(3)当滴加了73 g稀盐酸时(即A点时),烧杯中为不饱和溶液,试通过计算求出其中含溶质的质量.
查看答案和解析>>
科目: 来源:江苏省淮安市2007年初中毕业暨中等学校招生文化统一考试化学试题 题型:038
我市有丰富的NaCl矿产资源,NaCl是一种重要的化工原料,可以用于生产烧碱、氯气等重要的化工产品.某化工厂购进一批以NaCl为主要成分的原料(假设杂质全部为CaCl2),化验员欲测定原料中NaCl的质量分数,先称取60.0 g样品,加足量水充分溶解后,向所得溶液中加入足量的溶质质量分数为10%的Na2CO3溶液,充分反应后,生成2.0 g白色沉淀.(已知:CaCl2+Na2CO3![]() 2NaCl+CaCO3↓)
2NaCl+CaCO3↓)
试回答下列问题(写出计算过程):
(1)原料中NaCl的质量分数是多少?
(2)当恰好完全反应时,需Na2CO3溶液的质量是多少?
查看答案和解析>>
科目: 来源:湖南省永州市2007年初中毕业学业考试化学试卷 题型:038
石灰石是我市主要矿产之一,小江同学为了寻找纯度超过85%的石灰石,对一样品进行了如下定量实验.
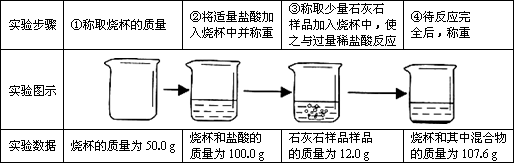
试通过分析计算:
(1)该实验中生成的二氧化碳的质量是多少克?
(2)该石灰石样品的纯度是否符合要求?(假设石灰石样品中的杂质不与盐酸反应也不溶于水)
查看答案和解析>>
科目: 来源:湖北省十堰市2007年初中毕业生学业考试化学试题 题型:038
十堰市是南水北调工程的水源地之一.近日市环保局对某工厂含少量硫酸的废水进行了抽样检查:取一定量废水用1%的氢氧化钠溶液中和(其它杂质不与氢氧化钠反应),当测得pH等于7时,消耗氢氧化钠溶液质量为40 g,同时测得反应后溶液质量为138 g.请计算该工厂排放的废水中硫酸的质量分数.
查看答案和解析>>
科目: 来源:湖北省鄂州市2007年升学考试化学试卷 题型:038
消化药片所含的物质能中和胃里过多的胃酸.某种消化药品的标签如图所示.医生给某胃酸过多的患者开出服用此药的处方为:每日3次,每次2片.试计算,患者按此处方服用该药一天,理论上可中和HCl多少毫克?(计算结果取整数)

查看答案和解析>>
科目: 来源:2007年江苏省无锡市初级中学高级中等学校招生考试化学试题 题型:038
小红同学在某化工厂进行社会实践,技术员与小红一起分析由氯化钡和氯化钠组成的产品中氯化钠的质量分数.取16.25 g固体样品,全部溶于143.6 mL水中,向所得到的混合溶液中逐滴加入溶质质量分数为10.6%的碳酸钠溶液,记录了如图所示的曲线关系.
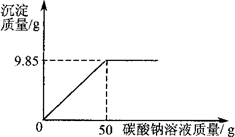
技术员给小红的提示:
①反应的化学方程式
BaCl2+Na2CO3![]() BaCO3↓+2NaCl
BaCO3↓+2NaCl
②水的密度为1 g/cm3
③相对分子质量 BaCl2:208 Na2CO3:106 BaCO3:197 NaCl:58.5
(1)当氯化钡与碳酸钠恰好完全反应时,消耗10.6%的碳酸钠溶液的质量是________g.
(2)产品中氯化钠的质量分数是多少?
(3)当氯化钡与碳酸钠恰好完全反应时,过滤,所得溶液中溶质的质量分数是多少?
查看答案和解析>>
科目: 来源:2007年江苏省南通市初中毕业、升学考试化学试题 题型:038
海洋约占地球表面积的71%,具有十分巨大的开发潜力.苦卤是海水提取食盐后的残液,利用苦卤可以制得金属镁等化工原料.下图是我市某盐场苦卤中部分成分含量柱形图.试计算:
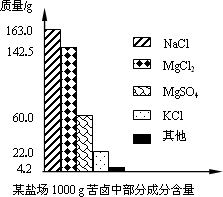
(1)若使100 g该苦卤中的MgCl2和MgSO4完全转化为Mg(OH)2沉淀,需要20% NaOH溶液多少克?
(2)将上述沉淀完全转化为无水MgCl2,并在熔融状态下进行电解,可得金属镁多少克?氯气多少升(该条件下氯气密度为3.0 g/L)?
查看答案和解析>>
科目: 来源:2007年江苏省南通市初中毕业、升学考试化学试题 题型:038
铁是人类不可缺少的微量元素,正常人每天应补充14 mg左右的铁,其中大部分来自于食物.如果全部通过服用含FeSO4·7H2O的片剂补充铁,则每天约需要服用含________mg FeSO4·7H2O的片剂.
市场上某硫酸亚铁片剂,其中Fe2+的含量为16.0%.该片剂中的Fe2+在空气中易变质,国家规定该片剂中Fe2+变质超过10.0%即不能再服用.为检验某药店出售的硫酸亚铁片剂是否失效,取10.0 g该片剂经测定含Fe2+ 1.52 g.通过计算说明该片剂是否能服用?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com