
科目: 来源:2008年江苏省常州市初中毕业升学统一考试、化学试卷 题型:038
某校化学兴趣小组为测定某硝酸铵样品的纯度,将10 g样品溶于30 g水后,再加入13.7 g氢氧化钠浓溶液共热,两者恰好完全反应(硝酸铵中的杂质不与氢氧化钠反应,也不溶于水,硝酸铵与氢氧化钠的反应方程式为:NH4NO3+NaOH![]() NaNO3+H2O+NH3↑).把产生的所有NH3用足量的硫酸溶液吸收,同时测量2分钟内硫酸溶液增加的质量,结果如下表所示:
NaNO3+H2O+NH3↑).把产生的所有NH3用足量的硫酸溶液吸收,同时测量2分钟内硫酸溶液增加的质量,结果如下表所示:

试回答下列问题:
(1)请在下面的坐标纸上,以反应时间为横坐标,以产生的NH3质量为纵坐标,画出能够表明产生气体的质量随时间变化的关系曲线;
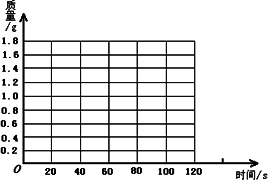
(2)表中m约为________;
(3)硝酸铵样品的纯度为________;
(4)试计算反应后所得硝酸钠溶液的溶质质量分数(不考虑反应过程中水损失的质量).
查看答案和解析>>
科目: 来源:2008年江苏省南通市初中毕业升学统一考试、化学试卷 题型:038
阳光牌小包装“脱氧剂”成分为Fe粉、活性炭及少量NaCl、水.使用一段时间后,其中的Fe粉会转变成Fe2O3而变质.某化学兴趣小组欲探究使用过的阳光牌“脱氧剂”的变质程度(已变质的Fe粉占变质前Fe粉的质量分数),设计并进行如下探究过程.
步骤(1)取食品包装袋中的阳光牌“脱氧剂”一袋,将里面的固体溶于水,过滤、洗涤、干燥滤渣.
步骤(2)取步骤(1)中的滤渣8.0 g,加入足量的稀H2SO4与滤渣充分反应,过滤、洗涤、干燥得固体1.2 g.
步骤(3)取步骤(2)中的滤液,加入足量的NaOH溶液,得到的固体经洗涤后转移到坩埚中,充分加热、冷却、称量,得到8.0 g Fe2O3(注:滤液中的Fe元素已全部转化为Fe2O3).
求:(1)8.0 g滤渣中Fe和Fe2O3两种物质的总质量.
(2)该“脱氧剂”在未变质时,Fe粉和活性炭的质量之比.
(3)该“脱氧剂”的变质程度.
查看答案和解析>>
科目: 来源:2008年广西贵港市初中毕业升学统一考试、化学试卷 题型:038
用“侯氏联合制碱法”制得的纯碱常含有少量的氯化钠.为测定某纯碱样品中碳酸钠的含量,小明称取该纯碱样品3.3 g,充分溶解于水中,再滴加氯化钙溶液,产生沉淀的质量与加入氯化钙溶液的质量关系如图所示.求:
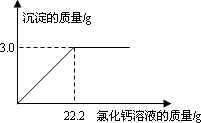
(1)该纯碱样品中碳酸钠的质量分数.(精确到0.1%)
(2)所加入氯化钙溶液的溶质质量分数.
查看答案和解析>>
科目: 来源:2008年广西省来宾市初中毕业升学统一考试、化学试卷 题型:038
有一瓶混有氢氧化钡的氢氧化钠固体,从中取出7.71 g样品,加水将其完全溶解后得到50.33 g溶液,并加人20 g硫酸钠溶液,与之恰好完全反应生成2.33 g沉淀.
[已知:Ba(OH)2+Na2SO4=BaSO4+2NaOH].试计算:
(1)7.71 g样品中氢氧化钡的质量;
(2)反应后所得溶液中溶质的质量分数.
查看答案和解析>>
科目: 来源:2008年广东省肇庆市初中毕业升学统一考试、化学试卷 题型:038
NaOH潮解后极易与空气中的CO2反应生成Na2CO3而变质.为测定实验室一瓶放置已久的烧碱中NaOH含量,某同学取适量的烧碱样品,溶于一定量的水得到200 g溶液;再加入200 g稀硫酸(足量)充分搅拌到不再放出气泡为止,称量溶液为395.6 g.
请计算:
(1)反应产生的CO2的质量为________g.
(2)若所取烧碱样品为50.0 g,则样品中NaOH的质量分数是多少?
(3)用同浓度的硫酸,与一瓶未变质、部分变质、或全部变质(杂质都是Na2CO3)的烧碱样品反应,需要硫酸的质量都相等.其原因是:________(从钠元素质量守恒的角度解释).
查看答案和解析>>
科目: 来源:2008年广东省湛江市初中毕业升学统一考试、化学试卷 题型:038
钢铁工业是国家工业的基础.2007年我国粗钢产量接近5亿吨,居世界前列.湛江的东海岛也将建设千万吨钢铁厂,这将给湛江的经济带来质的飞跃.某校兴趣小组取某种钢样进行试验,请计算:
(1)取钢样(假设只含铁单质和碳单质)粉末100 g,在氧气中充分燃烧,得到CO2气体4.4 g,此钢样粉末中碳的质量分数为________(保留到0.1%).
(2)分别向四份不同质量的钢样粉末中加入100 g稀硫酸溶液,充分反应后,测得的实验数据如下表所示:
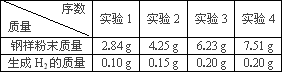
①计算硫酸溶液中溶质的质量________g
②求在实验3中溶液的溶质质量分数?
查看答案和解析>>
科目: 来源:2008年山东省枣庄市初中毕业升学统一考试、化学试卷 题型:038
维生素C是维持人体正常生理功能的微量物质,主要来自食物(青少年每人每天需要约100 mg).维生素C的化学式是C6H8O6,在橙子等新鲜水果中含量较高.小明测定了某品牌橙汁的维生素C的含量,过程如下:取10.00 g橙汁用含碘1.00%的碘溶液与其反应(反应的化学方程式为C6H8O6+I2![]() C6H6O6+2HI),恰好完全反应时消耗碘溶液12.70 g.计算:
C6H6O6+2HI),恰好完全反应时消耗碘溶液12.70 g.计算:
(1)该橙汁中维生素C的质量分数.(计算结果精确到0.01%)
(2)若维生素C全部来自橙汁,小明一天需要喝多少毫升该橙汁?(假定橙汁的密度为1.00 g/mL,计算结果精确到0.01)
查看答案和解析>>
科目: 来源:2008年山东省临沂市初中毕业升学统一考试、化学试卷 题型:038
刘明用石灰石(杂质不与酸反应,也不溶于水)和稀盐酸反应制取二氧化碳,在准备将反应后的废液倒进废液缸时,发现实验桌上有一瓶未知质量分数的Na2CO3溶液,他决定利用该废液,测定Na2CO3溶液中溶质的质量分数.他将废液过滤,然后向废液中慢慢滴加Na2CO3溶液,加入Na2CO3溶液的质量与生成沉淀质量的关系如图所示.
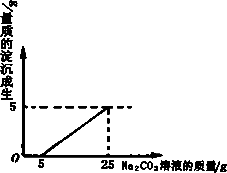
(1)在加入Na2CO3溶液的过程中,开始时没有发现沉淀生成,说明滤液中的溶质除含有CaCl2外,还含有________;
(2)计算Na2CO3溶液中溶质的质量分数.(计算结果精确到0.1%)
查看答案和解析>>
科目: 来源:2008年山东省东营市初中毕业升学统一考试、化学试卷 题型:038
为了测定黄铜屑(有锌和铜形成的合金)样品组成,甲、乙、丙、丁四位同学分别取样和稀硫酸反应(稀硫酸的密度为1.17 g/mL),实验数据记录如下:

(1)上表中n的数值为________.
(2)样品中碳酸钙的质量分数是________.
(3)求盐酸中溶质的质量分数.
查看答案和解析>>
科目: 来源:2008年安徽省芜湖市初中毕业升学统一考试、化学试卷 题型:038
让奥运火炬登上珠峰,是北京在申办2008年奥运会时对世界的一个承诺,也是奥林匹克史无前例的壮举.奥运火炬“祥云”使用的燃料为丙烷(化学式C3H8).
(1)丙烷燃烧的化学方程式为:C3H8+5O2![]()
![]() CO2+
CO2+![]() H2O,请你帮助完成化学方程式的配平;
H2O,请你帮助完成化学方程式的配平;
(2)请计算22 g丙烷完全燃烧需要消耗氧气的质量.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com