
科目: 来源:2013年湖北省十堰市高级中等学校招生考试化学 题型:043
某厂废液中的溶质只含有少量硫酸和硫酸钠,取废液样品30 g于小烧杯中(经测定该废液样品中含水的质量是29.22 g),向其中慢慢滴加2%的NaOH溶液20 g,并不断搅拌,恰好完全反应,所得溶液为不饱和溶液.(提示:H2SO4+2NaOH=Na2SO4+2H2O)
(1)计算该废液中硫酸的质量.
(2)恰好反应时,所得溶液溶质的质量分数.
查看答案和解析>>
科目: 来源:2013年湖北省十堰市高级中等学校招生考试化学 题型:043
2013年党的十八大提出“美丽中国”的构想.水是生命之源,是“美丽中国”的重要元素,目前由于工农业的发展使水的污染有扩大的趋势.
(1)请你说出两种不同净化水的方法;
(2)检验硬水和软水的简单方法及实验现象.
查看答案和解析>>
科目: 来源:2013年湖北省十堰市高级中等学校招生考试化学 题型:043
已知A、B、C、D、E均为初中化学常见的酸、碱、盐.其中A为胃酸的主要成分,B是碱,C是生理盐水的组成成分,E在工业上广泛的应用于玻璃、造纸等的生产.将它们配成溶液后,存在如图所示的转化关系,已知A和E能反应产生气体,请回答下列问题.(“-”表示相互间能反应,“→”表示在某种条件下能生成该物质)
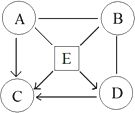
(1)写出A、E的化学式:A:________,E:________;
(2)写出B与D反应的化学方程式:________;
(3)如果用另一种化合物来代替C,其它物质和条件不变,也符合如图所示要求,那么这种化合物的化学式是________.
查看答案和解析>>
科目: 来源:2013年湖北省咸宁市高级中等学校招生考试化学 题型:043
将6.8 g含杂质的锌粒,加入到盛有50.0 g过量的稀硫酸的烧杯中(杂质不溶于水,也不与稀硫酸反应),充分反应后,称得烧杯内物质的总质量为56.6 g.试计算:
(1)生成氢气的质量.
(2)锌粒中所含锌的质量分数(精确到0.1%).
查看答案和解析>>
科目: 来源:2013年湖北省咸宁市高级中等学校招生考试化学 题型:043
二氧化碳的“捕捉”与“封存”是实现温室气体减排的重要途径之一.实际生产中,经常利用足量NaOH溶液来“捕捉”CO2,流程图如下(部分条件及物质未标出).
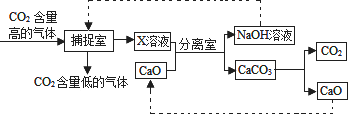
(1)分离室中进行的操作是________.
(2)该流程图所标出的物质中,溶于水放出大量热的氧化物是________.
(3)“捕捉室”内发生反应的化学方程式为________.
(4)将CaO加入到x溶液中,其中发生复分解反应的化学方程式是________.
查看答案和解析>>
科目: 来源:2013年湖南省长沙市高级中等学校招生考试化学 题型:043
实验室常用过氧化氢溶液与二氧化锰混合制取氧气.现将2.5 g二氧化锰放入盛有100 g过氧化氢溶液的锥形瓶中,反应完全结束后,共收集到1.6 g气体.请完成下列问题∶
(1)反应结束后,过滤,洗涤并烘干滤渣,称得滤渣的质量为________g.
(2)计算原过氧化氢溶液中溶质的质量分数.
查看答案和解析>>
科目: 来源:2013年湖南省长沙市高级中等学校招生考试化学 题型:043
化合物A、B、C都含三种元素,其中两种元素的质量比均为1∶2.它们之间有如图所示的关系,在图示的三个化学反应中(“→”表示转化关系)∶一个反应有沉淀生成,另一个反应有气体生产,还有一个反应既有沉淀又有水生成.请回答下列问题∶
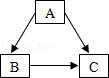
(1)写出A的化学式________;
(2)写出B→C反应的化学方程式________.
查看答案和解析>>
科目: 来源:2013年湖南省娄底市高级中等学校招生考试化学 题型:043
某化学兴趣小组的同学对一份固体样品进行了探究.通过实验已确定该样品由氧化铁和铁粉混合而成.他们称取了13.6 g固体样品,用图1所示的装置继续实验,测定的部分数据图2所示.

请计算:(1)固体样品中氧化铁的质量是________克.
(2)在上述反应后的固体中加入100 g稀盐酸,恰好完全反应,求反应后所得溶液中溶质的质量分数.(结果精确到0.1%)________
查看答案和解析>>
科目: 来源:2013年山东省日照市高级中等学校招生考试化学 题型:043
“黄铜”是铜、锌合金,为了测定某黄铜样品中锌的质量分数,甲、乙、丙三位同学分别进行实验,实验数据如下:(烧杯质量均为56 g)
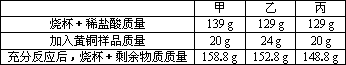
请回答下列问题:
(1)________同学取用的稀盐酸和样品恰好完全反应,他制取的氢气的质量
是________.
(2)计算黄铜样品中锌的质量分数.
查看答案和解析>>
科目: 来源:2013年山东省日照市高级中等学校招生考试化学 题型:043
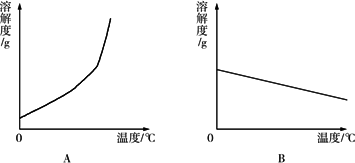
下表是Ca(OH)2和NaOH的溶解度数据.请回答下列问题:
(1)依据上表数据,绘制Ca(OH)2和NaOH的溶解度曲线,下图中能表示NaOH溶解度曲线的是________(填A或B).
(2)要想把一瓶接近饱和的Ca(OH)2溶液变成饱和溶液,具体措施有:
①加入氢氧化钙,
②升高温度,
③降低温度,
④加入水,
⑤蒸发水后再恢复到原温度,
⑥加入生石灰.
其中措施正确的是________.
A.②④⑥
B.③④
C.①③⑤⑥
D.①②⑤⑥
(3)20℃时,191 g饱和NaOH溶液,蒸发10 g水后,再降温到20℃,可析出NaOH晶体的质量为________.
(4)现有20℃时Ca(OH)2的饱和溶液(甲溶液),向其中加入一定量CaO后得到的溶液(乙溶液),此时溶液中溶质的质量分数乙________甲(填“>”、“<”或“=”).
(5)现有60℃时含Ca(OH)2和NaOH两种溶质的饱和溶液,若要得到较纯净的NaOH晶体,应采取的物理方法是________.
(6)20℃时,欲测定NaOH溶液的pH,若先将pH试纸用蒸馏水润湿,再进行测定,则所测溶液的pH________(填“偏大”、“偏小”或“不受影响”).
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com