
科目: 来源:江西省南昌市2011年初中毕业暨中等学校招生考试化学试题 题型:058
铝制品在日常生活中应用广泛,但铝制品却不宜长时间盛放腌制食品.资料显示:“铝制品表面虽然有一层致密的氧化膜保护……氯化钠也会破坏氧化膜的结构,加速铝制品的腐蚀.”
[提出问题]氯化钠溶液中的哪一种离子对氧化膜产生了破坏作用?
[实验方案]
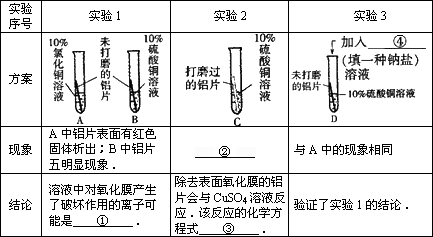
[反思]针对实验3,莹莹认为还应增做一个对比实验,她的方案是向B试管中再加入Na2SO4溶液,结构无明显现象.该实验可这么溶液中对氧化膜不产生破坏作用的离子是 ⑤ .
查看答案和解析>>
科目: 来源:江苏省盐城市2011年高中阶段教育招生统一考试化学试题 题型:058
(1)4月26日,全省最大的啤酒生产企业重啤集团盐城公司20万千升重啤项目正式投料生产.
①公司花园式的厂区里飘溢着阵阵麦芽香味.能闻到香味说明________.
A.分子很小
B.分子间有间隔
C.分子在不断运动
D.分子可以分成原子
②啤酒酿造过程中,酵母是“魔术师”,能将麦芽汁转化为酒精和二氧化碳.该变化属于________变化(选填“物理”或“化学”),酵母的作用是________.
③啤酒酿造需要大量除去矿物盐的软水.实验室常用________试剂区别软水和硬水.
④啤酒呈微酸性,过期的啤酒可用来浇灌喜酸花卉.测定啤酒的酸碱度可用________.
⑤啤酒贮存和运输时要防止阳光暴晒,原因是________.
(2)去年入秋以来,我市干旱少雨.在农业生产上,用0.1%的氯化钙溶液以1∶1浸种5~6小时后播种,可以提高种子在干旱条件下的出芽率.
①欲配制20 kg 0.1%的氯化钙溶液浸种,需要氯化钙________kg.
②以工业碳酸钙(含有少量Na+、Al3+、Fe3+等杂质)生产氯化钙的主要流程如下.
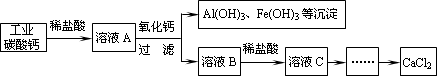
碳酸钙与稀盐酸反应的化学方程式为________,向溶液B中加入稀盐酸的作用是________.
查看答案和解析>>
科目: 来源:江苏省泰州市2011年初中毕业、升学统一考试化学试题 题型:058
已知:①金属钠是一种活泼的金属,与水反应生成氧氧化钠和氢气;②难溶于水的碱受热分解生成相应的氧化物和水.A、B、C、D、E、F、G、H是初中化学中常见的物质,甲、乙、丙是三种金属.其中甲最活泼,乙是红色金属,丙能被磁铁吸引.各物质间相互转化关系如下图:
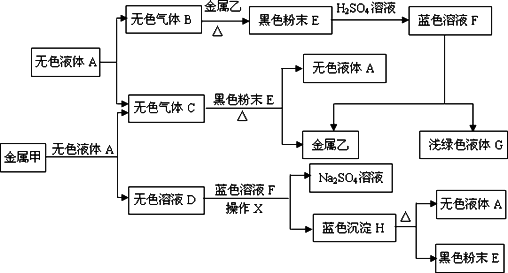
请回答下列问题:
(1)写出A、E、G的化学式:A________,E________,G________.
(2)操作X的名称是________.
(3)①无色溶液D与蓝色溶液F反应的化学方程式为________;
②金属甲与无色液体A反应的化学方程式为________,该反应的基本类型________;
③蓝色沉淀H受热分解反应的化学方程式为________.
(4)甲、乙、丙三种金属的活动性由强到弱的顺序是________,无色气体C在点燃或加热前必须进行的操作是________.
查看答案和解析>>
科目: 来源:四川省宜宾市2011年高中阶段学校招生考试化学试题 题型:058
早在西汉时期,我国就用铁与硫酸铜溶液反应制取铜,称为“湿法炼铜”.求:
(1)请写出“湿法炼铜”的化学方程式________.
(2)若用该方法制得铜32 g,反应的铁的质量________g,若同时消耗了500 g硫酸铜溶液,则该硫酸铜溶液中硫酸铜的质量分数为________%.
查看答案和解析>>
科目: 来源:2011年江苏省苏州市初中毕业暨升学考试化学试题 题型:058
已知碳酸氢钠在270℃左右就能分解为碳酸钠、水和二氧化碳,而碳酸钠受热不分解.现有某工厂生产出的一批碳酸氢钠中混有少量的碳酸钠,为了测定产品中碳酸氢钠的质量分数,具体的检验步骤如下:
①取一只洁净的坩埚,称其质量为a g;再向其中加入样品.称得总质量为m1 g;
②加热该盛有样品的坩埚;
③将坩埚充分冷却,称量坩埚和剩余固体的质量;
④多次重复步骤②和③至恒重,称得坩埚和剩余固体的总质量为m2 g.
(1)写出碳酸氢钠受热分解的化学方程式________.
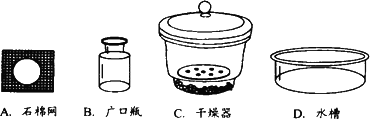
(2)用________(填仪器名称)将加热后的坩埚放到________中(填序号)冷却.
(3)根据题意,用a、m1、m2的代数式表示样品中碳酸氢钠的质量分数为________.
(4)步骤①、③和④都需要用到精度为0.1 g的托盘天平称量,若本题中(m1-m2)的值超过0.6 g,假设样品中碳酸氢钠的质量分数为90%,则至少需称样品多少克?
查看答案和解析>>
科目: 来源:山东省济宁市2011年高中阶段学校招生考试化学试题 题型:058
小林的妈妈把家庭久置不用的食盐、纯碱、漂白粉(主要成分是氯化钙和碳酸钙)和生石灰干燥剂中的一种或几种打包准备扔掉.小林为研究白色粉末的组成,将其带到实验室,设计并进行了以下实验:
(1)将部分粉末放人烧杯中,加适量水充分搅拌后,得到白色浊液,杯壁温度无明显变他得出:粉末中一定含有________,一定没有________,可能含有________;
(2)向实验(1)的浊液中滴加酚酞试剂,浊液变红.查阅资料知食盐、氯化钙溶液呈中性他又得出粉末中一定含有________.
经反思,小林感觉实验设计还不完善,不能确定粉末中是否含有食盐.
查看答案和解析>>
科目: 来源:山东省烟台市2011年高中招生考试化学试题 题型:058
小华同学用排水法收集了一大瓶沼气池中气体(下图中的A),为了弄清它的成分,进行了有关实验.请你与他一起完成以下探究活动:
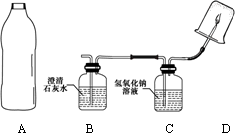
[对气体猜想]猜想Ⅰ:全部是CH4;
猜想Ⅱ:全部是CO;
猜想Ⅲ:是CO和CO2的混合气体;
猜想Ⅳ:是CH4和CO2的混合气体.
[实验和推断]将A中的气体依次通入B、C中,在D处点燃.
(1)要将A中的气体通入后面的装置中,应选下图中的________(填序号)“注水装置”.
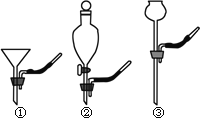
(2)若B中石灰水变浑浊,则说明A中的气体中含有________气体.
(3)装置C作用是________.
(4)若D处倒扣的是涂有澄清石灰水的烧杯,出现浑浊,且B中无明显现象,则“猜想”可能成立;若D处倒扣的是干冷的大烧杯,杯壁有水雾出现,有同学认为“猜想Ⅰ、Ⅳ”可能成立,另有同学认为此现象不能证明收集到的气体中一定含有CH4,理由是________;要排除这种干扰可采取的措施是________.
(5)采取(4)中的排除干扰措施后:若D处分别倒扣干冷的烧杯和涂石灰水的烧杯,分别出现水雾和浑浊,且B中也出现浑浊,则证明“猜想________”成立.
查看答案和解析>>
科目: 来源:山东省烟台市2011年高中招生考试化学试题 题型:058
某化学兴趣小组利用下图装置探究制取气体的原理、方法及性质.结合装置图,回答下列问题:

(1)写出图中标号仪器的名称:a________,b________.
(2)用双氧水和二氧化锰制取氧气时,可选用的发生装置是________(填上图字母),可选用C装置收集氧气,其原因是________.
(3)实验室常用氯化铵固体与碱石灰固体共热来制取氨气(NH3),应选择的发生装置是________(填上图字母).
(4)该小组设计了如下图所示的实验装置,既可用于制取气体,又可用于探究物质性质.
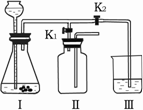
①当打开K1、关闭K2时,利用I、Ⅱ装置,可进行的实验是________(填字母).
a.大理石与稀盐酸反应制取二氧化碳
b.锌与稀硫酸反应制取氢气
②当打开K2、关闭K1时,可以利用工、Ⅲ装置制得二氧化碳并验证其性质.实验室制取二氧化碳的化学方程式是________;若要证明二氧化碳能与水发生反应,应向烧杯的水中加入________.
查看答案和解析>>
科目: 来源:山东省烟台市2011年高中招生考试化学试题 题型:058
无土栽培是利用营养液栽培作物的一种方法.
(1)下列化学肥料中属于复合肥的是________(填序号).
①硝酸铵
②磷酸二氢铵
③硝酸钾
④硫酸钾
(2)某同学要在实验室配制150 g溶质质量分数为2%的硝酸钾溶液,需要硝酸钾的质量为________g.

(3)现有一种无色的营养液,可能由KNO3、Ca(NO3)2、K2CO3、KCl中的一种或几种物质组成,为探究其成分,某同学设计并完成了如下图所示的实验.
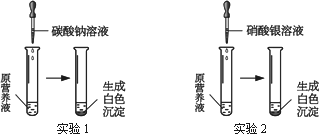
根据以上实验,请你进行有关推断.
①由实验1可确定原营养液中一定没有的物质是________;
②根据实验1、实验2推测原营养液的组成可能有________种情况;
③若测得原营养液中K+和Cl一的数目之比为1∶1,则原营养液的组成中的溶质是________.
查看答案和解析>>
科目: 来源:福建省福州市2011年初中毕业会考、高级中等学校招生考试化学试卷 题型:058
某课外活动小组同学用下图装置(固定装置未画出)测定含有杂质的镁带中镁单质的质量分数(杂质与酸接触不产生气体).实验过程是:
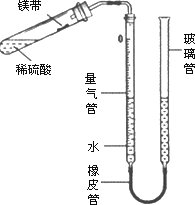
①取一段镁带样品,准确称得其质量为0.030 g.
②往量气管内装水至低于刻度“0”的位置.按图所示(未装药品)装配好仪器.
③检查装置气密性.
④在试管中加入足量的稀硫酸,稍倾斜试管,将用水湿润的镁带小心贴在试管壁上,塞紧橡皮塞.
⑤调整量气管液面,使两边的液面保持同一水平,记录量气管中液面位置.
⑥把试管底部略为抬高,使镁带与稀硫酸接触完全反应.
⑦待冷却至室温后,再次记录量气管中液面位置.
⑧算出量气管中增加的气体体积为23.96 mL.
已知:同温同压下,不同气体混合后体积等于混合前各气体体积之和.
请回答下列问题:
(1)写出镁与稀硫酸反应的化学方程式________.
(2)能否用托盘天平称量0.030 g镁带样品________.(填“能”或“不能”)
(3)若不改变温度,如何用较简单的方法检查图所示装置的气密性?
________.
(4)经换算,该实验获得的氢气质量为0.0020 g.该镁带中单质镁的质量分数是________.
(5)实验过程⑦中再次记录量气管的液面位置时,试管中留有氢气,是否会影响实验最终结果________(填“是”或“否”).理由是________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com