
科目: 来源:江苏省淮安市2012年中考化学试题 题型:058
在古代,人们常用贝壳(主要成分是碳酸钙,杂质不参加反应且不溶于水)和纯碱为原料制取烧碱,某小组同学按图所示流程进行实验,请你参与讨论并回答相关问题.
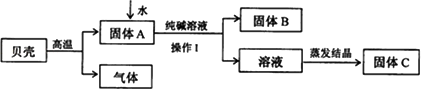
(1)贝壳高温煅烧时,发生反应的化学方程式是________;
(2)操作Ⅰ中用到的玻璃仪器有烧杯、________、玻璃棒;
(3)溶液蒸发结晶得到固体C的过程中,常用玻璃棒搅拌,其目的是________;
[问题与发现]该小组同学所得到固体C一定是纯净的NaOH吗?
[猜想与假设]根据反应原理,甲、乙、丙三位同学提出以下猜想:
甲:纯净的NaOH
乙:NaOH和Na2CO3的混合物
丙:NaOH和Ca(OH)2的混合物
[探究与验证]甲、乙、丙三位同学分别设计下列方案,对自己的猜想进行验证.实验操作、现象和结论如下表,请参与他们的探究并完成所缺内容.
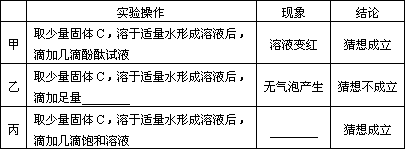
查看答案和解析>>
科目: 来源:江苏省南京市2012年中考化学试题 题型:058
钢铁工业是国家工业的基础.
(1)下图是教材中炼铁高炉及炉内化学变化过程示意图,根据图示回答下列问题.
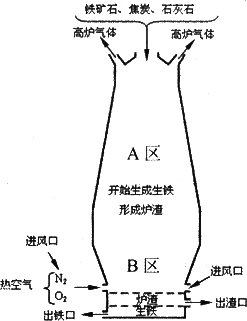
若图中采用的铁矿石的主要成分为氧化铁,请写出A区和B区所发生主要反应的化学方程式:
A区________
B区________
(2)某兴趣小组在实验室中模拟炼铁化学原理的实验,对固体产物成分等进行探究.
[设计实验]
用一氧化碳还原纯净的氧化铁粉末,实验装置如下图.
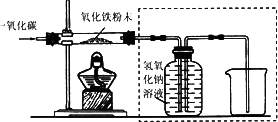
[进行实验]
该小组按上述实验设计,在一定温度下进行了实验,测得下列数据:
①反应前玻璃管和内盛氧化铁粉末的总质量66.0 g(玻璃管的质量为60.0 g)
②反应后玻璃管和内盛黑色固体的总质量65.8 g(冷却到室温称量)
③
[分析与讨论]
本实验中,玻璃管内固体粉末由红色全部变为黑色.小明同学认为该黑色固体全部是铁,但小华同学提出了质疑,于是大家提出查阅资料.
[查阅资料]
①一氧化碳还原氧化铁的固体产物的成分与反应温度、反应时间等因素有关.
②一氧化碳还原氧化铁的实验过程中固体产物可能有四氧化三铁、氧化亚铁、铁.
[实验与猜想]
①该小组同学将反应后的黑色固体研磨后,再用磁铁吸引,发现黑色固体粉末全部能被吸引,则该黑色固体粉末中不可能含有氧化铁和________.
②进行猜想:黑色固体粉末可能
a.全部为铁
b.________
c.________.
[得出结论]
通过实验中获得的数据进行计算,得出黑色固体粉末为(写名称)________.
[反思与评价]
①一氧化碳还原氧化铁的实验中,若要得到铁可适当提高反应温度和延长反应时间.
②实验装置图中采用虚线框内的装置,其作用有________.
A.收集一氧化碳
B.吸收二氧化碳
C.检验二氧化碳
查看答案和解析>>
科目: 来源:广西玉林市、防城港市2012年中考化学试题 题型:058
造成酸雨的主要物质是二氧化硫(SO2),某兴趣小组的同学收集某地刚降到地面的雨水进行实验.
相关信息:①用pH计(测pH的仪器)每隔几分钟测一次pH,其数据如下表所示:
③BaSO3不溶于水,但能跟稀盐酸反应,BaSO4既不溶于水,也不与稀盐酸反应
分析讨论:①酸雨能使土壤酸化,农业上常用________中和酸性土壤.
②酸雨能腐蚀金属制品,请写出一种防止室外金属被腐蚀的方法________.
③收集的酸雨样品放置一段时间后pH减小,原因是SO2与H2O反应生成H2SO3被氧化为H2SO4,请写出H2SO3被氧化生成H2SO4的化学方程式________.
提出猜想:同学们对收集到的酸雨样品的溶质进行猜想:
猜想Ⅰ:酸雨中溶质为H2SO3
猜想Ⅱ:酸雨中溶质为H2SO4
猜想Ⅲ:酸雨中溶质为________
实验探究:向收集的酸雨样品中滴加过量的Ba(OH)2溶液,有白色沉淀生成,过滤,向沉淀中加入足量的稀盐酸,请完成下表:
④请写出加入稀盐酸后沉淀溶解并放出有刺激性气味气体的化学方程式________.
拓展延伸:酸雨中含有的酸除了上面的H2SO3和H2SO4以及空气中CO2与H2O反应生成的H2CO3外,还可能含有的酸根是________.
查看答案和解析>>
科目: 来源:广东省梅州市2012年中考化学试题 题型:058
现有银、铜、铁三种金属,某研究小组的同学为探究银、铜、铁的金属活动性顺序,设计了三个实验:Ⅰ.将铁片浸入稀硫酸中;Ⅱ.将银片浸入稀硫酸中;Ⅲ.将铁片浸入硫酸铜溶液中.
(1)实验Ⅰ的现象是:有气泡产生,溶液由无色逐渐变为浅绿色.反应的化学方程式为________;反应产生的气体可用________的方法检验.
(2)上述三个实验还不能完全证明三种金属的活动性顺序,请你补充一个实验来达到实验目的(写出实验操作和现象)________.根据以上探究,三种金属的活动性由强到弱的顺序是________.
(3)将银、铜、铁中的两种金属分别放入________溶液中,即可验证这三种金属的活动性强弱.
(4)将铜片加热,铜片表面变黑.同学们设计如下实验证明此黑色物质是氧化铜.

查看答案和解析>>
科目: 来源:广东省梅州市2012年中考化学试题 题型:058
请根据下图所示实验装置回答问题:
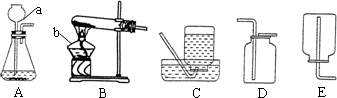
(1)写出图中标号仪器的名称:a________,b________.
(2)实验室若用装置A制取氧气,则发生反应的化学方程式为________.若用装置B制取氧气,药品选用高锰酸钾,则发生反应的化学方程式为________,在试管口放一团棉花的作用是________.
(3)实验室收集二氧化碳选用装置________(填序号).若收集某气体只能采用装置E,由此推测该气体具有的性质是________.
查看答案和解析>>
科目: 来源:广东省揭阳市2012年中考化学试题 题型:058
某实验小组用图A完成课本实验“碳酸氢钠与盐酸反应的探究”后,他们发现两种反应物的用量不同时反应后溶液中的成分也可能不同,于是他们对碳酸氢钠与盐酸反应后的大试管中溶液的成分进行探究,请回答以下问题:
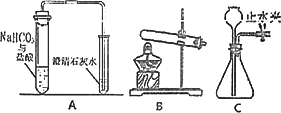
(1)写出图A中大试管发生反应的化学方程式:________;
写出小试管中发生反应的化学方程式:________;
(2)若实验室制二氧化碳应选装置________(填B或C),药品为:________(填名称):
[提出假设]小组成员认为A中大试管的溶液的溶质只能存在三种情况:
假设1.两溶液恰好完全反应,溶质为NaCl;
假设2.两溶液完全反应后,盐酸过量,溶质为NaCl和HCl;
假设3.________.
[设计并进行实验和得出结论]小组同学讨论后发现只要用反应物本身两种试剂(碳酸氢钠溶液和稀盐酸)就可以完成实验,请填写下表中的实验内容:

查看答案和解析>>
科目: 来源:广东省佛山市2012年中考化学试题 题型:058
漂白粉的主要成分为次氯酸钙[Ca(ClO)2]和氯化钙,即可用作漂白剂,又可用作消毒剂.漂白粉中有效成分是[Ca(ClO)2],漂白的原理是:Ca(ClO)2在空气中发生反应
Ca(ClO)2+CO2+H2O![]() CaCO3↓+2HClO;HClO是一种酸性比盐酸弱的酸,不稳定,具有漂白性,能使品红等有色物质褪色.
CaCO3↓+2HClO;HClO是一种酸性比盐酸弱的酸,不稳定,具有漂白性,能使品红等有色物质褪色.
(1)漂白粉是一种________(填“纯净物”或“混合物”).
(2)HClO在常温下分解,反应为2HClO=2HCl+O2↑.某瓶HClO溶液放置一段时间后,溶液的pH________(填“增大”或“减小”或“不变”).
(3)在漂白粉中滴加盐酸,能加快漂白的速率.写出漂白粉中加入盐酸反应的化学方程式________.
(4)有一包长时间放置的漂白粉,想知道该漂白粉是否变质,某同学设计了下列探究实验.
[提出问题]长时间放置的漂白粉是否变质?
[猜想]
猜想1:该漂白粉未变质,固体成分为CaCl2、Ca(ClO)2;
猜想2:该漂白粉部分变质,固体成分为________;
猜想3:该漂白粉全部变质,固体成分为CaCl2、CaCO3.
[实验探究]限选试剂及仪器:盐酸、石灰水、品红溶液、试管、带导管的单孔塞.

查看答案和解析>>
科目: 来源:广东省佛山市2012年中考化学试题 题型:058
某学习小组围绕“气体实验室制取”进行了研讨.请你参与完成下面的问题.
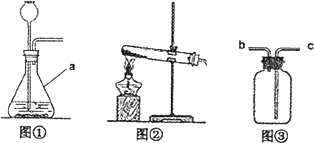
(1)原理分析:实验室制取CO2的化学方程式为________.
不用Na2CO3与盐酸反应制取CO2的原因是________.
(2)发生装置:图①装置中仪器a的名称是________.实验室常用无水醋酸钠固体与碱石灰在加热的情况下制CH4,应选图________(填序号)发生装置.
(3)收集装置:实验室收集NH3应采用的方法是________.收集有毒气体SO2时,常采用③收集装置,气体应从________(填字母)端通入.
(4)实验操作:用KMnO4制取O2的操作过程可概括为“组装仪器→________→________→加入试管→收集气体→停止加热”.
(5)实验反思:在加热KClO3制O2的过程中,发现产生O2的速率很慢,经检查不是KClO3变质,也不是装置气密性不好,你认为最可能的原因是________.
查看答案和解析>>
科目: 来源:山西省2012年中考理综试题化学部分 题型:058
同学们在学习酸碱的化学性质时构建了如图知识网络,A、B、C、D是不同类别的无机化合物,“-”表示物质在一定条件下可以发生化学反应.请回答下列问题:
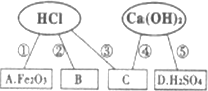
(1)反应①的化学方程式为:________,实验现象为________.
(2)写出图中一个中和反应的化学方程式________.
(3)物质C应具备的条件是________.
查看答案和解析>>
科目: 来源:山东省烟台市2012年中考化学试题 题型:058
2012年3月6日,包括圆明园兽首在内的一批珍贵文物首次在烟台展出.小霞看到这些240年前的铜质兽首后,她想探究铜是怎么冶炼出来的.

[查阅资料](1)冶炼铜可以用常见的铜矿石——孔雀石,其主要成分是碱式碳酸铜[Cu2(OH)2CO3].碱式碳酸铜是一种绿色的不溶于水的固体,加热易分解,能与酸反应.Cu2(OH)2CO3![]() 2CuO+CO2↑+H2O,Cu2(OH)2CO3+4HCl
2CuO+CO2↑+H2O,Cu2(OH)2CO3+4HCl![]() 2CuCl2+CO2↑+3H2O.
2CuCl2+CO2↑+3H2O.
(2)实验室可以用至少三种方法来制取铜:①用氢气在加热的条件下还原氧化铜(生成铜和水);②电解氯化铜溶液(生成铜和氯气,氯气有毒);③用活泼金属从铜的盐溶液中置换.
[设计方案]在实验室中以碱式碳酸铜、铁粉、稀盐酸为原料来制取铜.请你仿照下图①帮她画出另外两种制取铜的流程图.
①![]()
②_________________________________
③_________________________________
[反思评价](1)上述三种制取铜的方案中,你认为最理想的是________,与其他两种方案比较,它有哪些优点(至少答一点):________.
(2)铜锈的主要成分也是碱式碳酸铜[Cu2(OH)2CO3].铜生锈除了与空气中的氧气和水关外,从碱式碳酸铜的化学式推知,还可能与空气中的________有关.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com