
科目: 来源:江苏省阜宁县2012年中考适应性考试化学试题 题型:058
下图是实验室常用的实验装置,请回答有关问题:

(1)装置C由导管、________和________(填仪器的名称)组成.
(2)实验室用H2O2和MnO2制取O2的化学方程式为________,选用的发生装置是________(填序号,下同);若用KClO3和MnO2制取O2时,则选用的发生装置是________.
(3)实验室制取二氧化碳,选用的发生装置为________(填序号),该反应的化学方程式为________.将产生的二氧化碳气体通入F中,看到的现象是:________.
(4)实验室制取H2应选用的收集装置是________或________.(填序号)
查看答案和解析>>
科目: 来源:河南省襄城区2012届初三中考模拟考试化学试题 题型:058
小亮对铁丝在氧气里燃烧时出现的红热球状物产生了兴趣,随后他进行了以下探究活动.
[问题1]铁燃烧后剩下来的球状物质中还有没有铁呢?
[实验探究]将剩下来的球状物质碾碎,加入________溶液,观察到的现象是________,说明铁燃烧时溅落下来的黑色物质中还含有铁.
[问题2]铁燃烧的产物为什么不是Fe2O3呢?
[查阅资料]
(1)自然界中铁的氧化物主要是Fe3O4和Fe2O3两种(FeO极易被氧化为Fe2O3);
(2)Fe3O4和Fe2O3的分解温度、铁的熔点见表:
(3)Fe2O3高温时分解成Fe3O4
[理论探讨]实验测定铁在氧气里燃烧的产物是Fe3O4,结合表中数据,可推知铁在氧气里燃烧时产生的高温应在________℃之间,在此温度范围内________已分解.
[拓展延伸]
(1)实验中为了防止集气瓶炸裂,必须________;
(2)有些食品包装盒的透明盖内放有黑色的FeO粉末,若粉末的颜色________,就说明包装盒破损进气,这样售货员就能及时发现并处理.
查看答案和解析>>
科目: 来源:江苏省扬州中学教育集团树人学校2012年中考第二次模拟考试化学试题 题型:058
化学兴趣小组对某品牌牙膏中碳酸钙含量进行以下探究.该牙膏摩擦剂主要由碳酸钙、氢氧化铝组成,其他成分遇到盐酸时无气体生成.现利用下图所示装置(图中夹持仪器略去)进行实验,充分反应后,测定B中生成的BaCO3沉淀质量,以确定碳酸钙的质量分数.请回答下列问题.
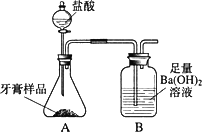
(1)装置A中牙膏样品放置在________(填仪器名称)中,装置A中至少发生________个反应.
(2)若测定值比实际值小,可能的原因有________.(填数字序号)
①装置A中水蒸气、HCl等进入装置B中
②装置A中CO2未完全进入装置B
③CO2气流速度太快导致Ba(OH)2未完全吸收
④盐酸未滴加过量
(3)为减少误差,现采取一些措施:为防止HCl进入B装置,可在A、B之间增加装有________(填药品名称或化学式)溶液的洗气瓶;将装置B中的长导管下方增加一个带孔球泡,可以提高________;在装置B的后面再增加一个装有________(填药品名称或化学式)固体的干燥管.
(4)准确称取8.00 g样品三份,进行测定,测得BaCO3平均质量为3.94 g.则样品中碳酸钙的质量分数为________.
查看答案和解析>>
科目: 来源:江苏省东台市2012届九年级下学期第一次阶段检测化学试题 题型:058
某校兴趣小组同学准备进行常见酸、碱、盐的性质实验时,发现实验台上摆放的药品中(如下图),有一装溶液的试剂瓶未盖瓶盖且标签破损,于是决定对这瓶溶液进行实验探究:
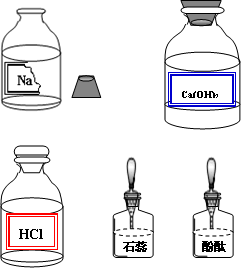
[提出问题]这瓶溶液是什么溶液?
[获得信息]酸、碱、盐的性质实验中用到含有钠元素的物质是氯化钠、氢氧化钠、碳酸钠
[提出猜想]这瓶溶液是:猜想一:氯化钠溶液;猜想二:氢氧化钠溶液;
猜想三:碳酸钠溶液.
[实验推断]
(1)小丽取样滴加无酚酞试液,溶液呈红色,得出结论:该溶液不可能是________溶液,理由是________;
(2)小刚另取样滴加稀盐酸有________产生,反应的化学方程式为________,小刚得出结论:该溶液是碳酸钠溶液.
(3)小青认为小刚的结论不完全正确,理由是________.
小组同学讨论后一致认为还需要进行如下实验:
[继续探究]另取样加入过量的CaCl2溶液,观察到有________产生,设计这一步骤的目的是________;静置后,取上层清液,滴入酚酞试液,溶液呈红色.
[实验结论]这瓶溶液是________.
[探究启示]实验取完药品后应________.
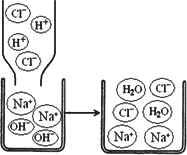
[拓展迁移]若该溶液与盐酸发生中和反应,恰好完全反应的微观过程如图所示,反应的实质表达式为:H++OH-=H2O,则反应后溶液中存在的阴、阳离子是________(填符号);请写出[继续探究]实验中加CaCl2溶液反应的实质表达式:________(用化学符号表示)
查看答案和解析>>
科目: 来源:江苏省东台市2012届九年级下学期第一次阶段检测化学试题 题型:058
A、B、C是三种不同类别的含有氧元素的化合物,物质间相互反应的关系如图所示(图中“─”表示相连的两种物质能在溶液中发生反应).若B为纯碱,A、C间的反应为复分解反应,回答下列问题:
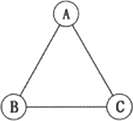
(1)物质A、B、C的化学式是A________ B________ C________.
(2)物质A和C在溶液中反应的化学方程式是________.
(3)纯碱的一种用途是________.
查看答案和解析>>
科目: 来源:江苏省东台市2012届九年级下学期第一次阶段检测化学试题 题型:058
硫酸和盐酸既是实验室常用的试剂,也是重要的化工原料.它们既有相似之处,又有不同之处.
(1)它们水溶液的PH都________7(填“大于”、“小于”或“等于”).
(2)它们都能除铁锈,写出盐酸与铁锈主要成分反应的化学方程式________.
(3)它们都能与碱反应生成盐和水,该类反应叫________反应.
(4)打开两瓶分别盛有浓硫酸和浓盐酸的试剂瓶,瓶口出现白雾的是________.
(5)请写出把硫酸转变为盐酸的化学方程式________.
查看答案和解析>>
科目: 来源:江苏省盐城市亭湖区2012届九年级下学期第一次调研考试化学试题 题型:058
纳米碳酸钡是一种重要的无机化工产品,下图是某厂生产纳米碳酸钡的工艺流程.请回答下列问题:
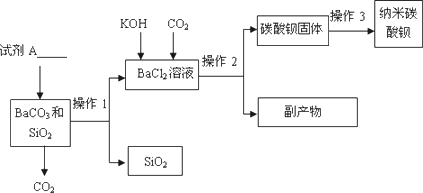
(1)试剂A的化学式________,若在实验室中进行该实验,操作1和操作2的名称是________,该实验中玻璃棒的作用________.
(2)操作3为洗涤、检验和________,洗涤的作用是________,检验洗涤是否干净可选用试剂________(写化学式).
(3)上述流程中可循环利用的物质是________,该流程中的副产物可用作________.(写一种用途)
(4)分析该流程可得出SiO2部分性质,下列属于其物理性质________,化学性质________.
A.不溶于水
B.可溶于水
C.不与盐酸反应
D.能与盐酸反应
(5)某同学查阅资料得知,二氧化硅能与氢氧化钠溶液反应生成可溶性的硅酸钠(Na2SiO3),该反应的化学方程式________.根据此原理该同学设计出如下方案制备:取碳酸钡和二氧化硅混合物,滴加________(填“少量”或“过量”)的氢氧化钠溶液,过滤,洗涤,烘干得碳酸钡固体.
查看答案和解析>>
科目: 来源:江苏省盐城市亭湖区2012届九年级下学期第一次调研考试化学试题 题型:058
人体缺乏维生素C(简写“Vc”)会患坏血病.下图所示为某种“维生素C”说明书的一部分,请回答:

(1)“Vc”属于________化合物(填“无机”或“有机”);
(2)“Vc”中C、H、O三种元素的质量比是________;
(3)若正常成人每天对“Vc”的最低需要量为60 mg:
①当这些“Vc”完全来自上图的“维生素C”时,则每次服用“维生素C”至少________片;
②当这些“Vc”完全来自某种新鲜蔬菜(每1000 g这种蔬菜含“Vc”120 mg)时,每天至少应食用这种蔬菜________g;
(4)取2片“维生素C”溶于水,滴入紫色石蕊试液变红色,说明“Vc”溶液的PH________7
查看答案和解析>>
科目: 来源:江苏省盐城市亭湖区2012届九年级下学期第一次调研考试化学试题 题型:058
下图是某研究性学习小组设计的几种装置,请你分析并回答下列问题:

(1)图中标号仪器为:a________,b________.
(2)装置A可用作实验室制取O2或CO2的发生装置,用此装置制取O2的化学方程式是________.
(3)某同学从装置A得到启发,在装置A的基础上增加了隔离铜网改成装置B来制取氢气,又用一支底部有一个小洞的试管和矿泉水瓶组合成装置C(夹持仪器都略去).则B与A相比优点是________.而装置B显示的化学反应状态为________(填“进行中”或“已停止”).
(4)在实验室用装置C制取CO2的化学反应方程式为________,若隔离网改用铁丝做成,则产生的后是________,说明金属活动性Fe________Cu(填“=”或“>”或“<”).
查看答案和解析>>
科目: 来源:四川省南充市阆中中学2012届九年级下学期第一次月度检测化学试题 题型:058
小明家购买了一瓶白醋,标签上注明醋酸的质量分数≥5%.小明想:这瓶白醋中醋酸的含量是否与标签的标注相符?请你用有关酸碱的知识,定量测定白醋中醋酸的含量.
实验原理:
(1)用已知浓度的氢氧化钠溶液和醋酸反应,反应的化学方程式为:
CH3COOH+NaOH=CH3COONa+H2O
(2)在混合溶液中,当醋酸和氢氧化钠完全中和时,再增加1滴氢氧化钠溶液,溶液就呈碱性,而1滴氢氧化钠溶液约为0.05 ml,对测定结果的影响很小,可忽略不计.
实验步骤:
(1)用________取12.0 mL白醋(密度近似为1.0 g/ml),倒入烧杯中,加入20 ml蒸馏水稀释,再滴入几滴酚酞试液.
(2)量取45.0 ml溶质质量分数为1.0%的氢氧化钠溶液(密度近似为1.0 g/ml),用胶头滴管取该氢氧化钠溶液,逐滴地滴加到稀释后的白醋中,同时不断地搅拌烧杯中的溶液.滴至恰好完全反应,剩余氢氧化钠溶液5.0 ml.
交流反思:(1)在实验步骤①中,加适量水稀释白醋,对实验结果有无影响?为什么?
(2)在实验步骤②中,小明如何确定醋酸和氢氧化钠已完全中和?
数据处理:根据实验数据,通过计算判断白醋中醋酸的含量是否与标签的标注相符?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com