
科目: 来源: 题型:填空题
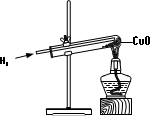
在自然界里大多数金属是以化合物的形式存在的。常用的金属冶炼是通过氢气、一氧化碳、碳粉与金属氧化物在高温下反应来实现的。小明在实验室里做氢气还原氧化铜的实验,请回答以下有关问题:
(1)下面是该实验的四个步骤,正确的操作顺序是 。
| A.加热 | B.通入氢气 | C.停止通入氢气 | D.停止加热 |
查看答案和解析>>
科目: 来源: 题型:填空题
钓鱼岛、黄岩岛自古就是中国的固有领土,为宣示主权2012年5月9日,我国深水钻井平台“981”在南海正式开钻,这座平台总用钢量达3万多吨.试回答:
(1)该平台操控室内的一些设备使用了不锈钢,不锈钢的成分是 ;
(2)漏出水面的钢铁平台均采用防锈措施,原因是 ;
(3)用发电机钻井时其能量转化主要是 ;
(4)平台建成后,抽出的石油会产生一些气体,其中,甲烷气体排入大气中会引发的后果是 ,因此,混合气体全部通过一根管道引到远离平台的地方点燃烧掉(如图),其中有毒气体硫化氢燃烧时,生成两种常见的氧化物,该反应的化学方程式为 .
查看答案和解析>>
科目: 来源: 题型:填空题
金属在生活和生产中有广泛的应用.
(1)下列金属制品中,利用金属导热性的是 (填字母序号).
(2)铁生锈的条件是 .
(3)工业上用一氧化碳和赤铁矿炼铁反应的化学方程式为 .
(4)工业上生产电路板及处理废液的工艺流程如下: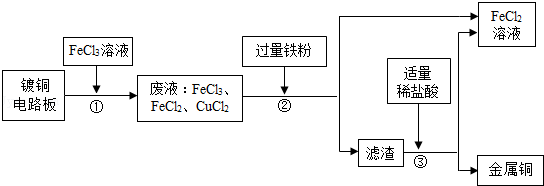
Ⅰ.步骤①反应的化学方程式为 .
Ⅱ.步骤②得到滤渣的成分是 .
查看答案和解析>>
科目: 来源: 题型:填空题
铝、铁、铜是我们生活中常见的金属。
(1)铝的利用比铜、铁晚是因为金属大规模开发和利用的先后顺序与 有关(填字母)
A.金属的活动性 B.金属的导电性 C.金属在底壳中的含量
(2)铝具有很好的抗腐蚀性能,原因是 。
(3)化学新材料的应用,使人们的生活质量不断提高.如图是不同年代常用的水管。
①图示所有水管中,含有的金属元素是 。
②每年全世界钢铁的产量很高,但钢铁的锈蚀也给人类带来了巨大的损失,铁在空气中锈蚀,实际上是铁跟 共同作用的结果;工业上常用稀盐酸来除铁锈(Fe203),该反应的化学方程式是 。请你提出一种防止铁制品锈蚀的方法: 。
③铁丝在空气中不能燃烧却在氧气中剧烈燃烧,其燃烧的化学方程式为 。
(4)印发铜制电路板的“腐蚀性”为FeCl3溶液反应,化学方程式分别为①Cu+2FeCl3=2FeCl2+CuCl2;②Fe+2FeCl3=3X.则②中X的化学式为 。
查看答案和解析>>
科目: 来源: 题型:填空题
同学们即将初中毕业.在离开母校之际,整理自己的物品时,若清理出如下物品:①废作业纸 ②易拉罐 ③变质饼干 ④生锈铁钉。
(1)应该放入“不可回收垃圾箱”的是 (用序号填写)。
(2)生锈铁钉可用酸除锈,把一根生锈放入过量稀盐酸中,过一会儿,可看到现象是 ,此时溶液中的阳离子有 ;过一段时间,还会看到铁钉表面有 产生,产生该现象的化学方程式为 。
(3)X、Y、Z是金属活动性顺序表中的三种固态金属,如果把X、Y、Z分别放入稀硫酸中,X溶解并产生氢气,Y、Z不反应;把Y和Z分别放入硝酸银溶液中,过一会儿,在Z表面有银析出,而Y没有变化。根据以上实验事实,回答下列问题:
①X、Y和Z的金属活动性由强到弱的顺序为 ;
②写出在Z表面有银析出的反应化学方程式 。
查看答案和解析>>
科目: 来源: 题型:填空题
人类的生产、生活离不开金属。
(1)目前年产量最高的金属是 ;
(2)铁在潮湿的空气里会发生锈蚀,证明氧气一定参加了反应必须要做的实验是 ;
| A.①② | B.①③ | C.②③ | D.①②③ |
查看答案和解析>>
科目: 来源: 题型:填空题
铁是生产生活中应用最广泛的一种金属。
(1)铁元素与地壳中含量最多的元素组成的化合物化学式为 (写出一种即可)。高铁酸钠(Na2FeO4)是一种新型高效的净水剂,高铁酸钠中铁元素的化合价为 价。
(2)常见的食品脱氧剂多为无机铁系脱氧剂,其主要成分为活性炭铁粉。请将下列脱氧中主要反应的化学方程式补充完整:4Fe(OH)2+O2+2 =4Fe(OH)3。
(3)高温条件下一氧化碳能把铁从赤铁矿石(主要成分为Fe2O3)中还原出来,反应的化学方程式
是 。
查看答案和解析>>
科目: 来源: 题型:填空题
金属材料在生产、生活中有广泛的用途.
(1)黄铜是铜、锌合金,下列说法中不正确的是 。
| A.黄铜属于纯净物 | B.黄铜属于金属材料 |
| C.黄铜的硬度比铜大 | D.黄铜的抗腐蚀性能更好 |
查看答案和解析>>
科目: 来源: 题型:填空题
神舟十号飞船将在2013年夏天与“天宫一号”交会对接
(1)镍钛合金被人们称为“形状记忆合金”,可制作的飞船自展天线.关于此天线制作材料的描述错误的是( )
| A.具有形状记忆功能; | B.具有极低的熔点; | C.具有良好的延展性; | D.具有良好的导电性 |
查看答案和解析>>
科目: 来源: 题型:填空题
在FeCl3溶液蚀刻铜箔制造电路板的工艺中,废液(主要含有FeCl2和CuCl2)处理和资源回收的过程简述如下:
I:向废液中投入过量铁屑,充分反应后分离出固体和滤液;
II:向滤液中加入一定量石灰水,调节溶液pH,同时鼓入足量的空气。
试回答下列问题:
(1)过程I加入铁屑的主要作用是 ;试写出其对应的化学方程式: ;
(2)从固体中分离出铜需采用的方法是 ;
(3)滤液中溶质主要为 (写出化学式);已知过程II生成的最终产物为Fe(OH)3,则Fe(OH)2与氧气和水反应的化学方程式为: 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com