
科目: 来源: 题型:填空题
(8分)归纳总结是化学学习的常用方法,下图是对生成物质A的反应关系的归纳与整理。
请回答下列问题:
(1)写出A的化学式: ,反应③
的基本厦应类型是 。
(2)写出反应⑤的化学方程式:
。
该反应在医疗上的用途是: 。
(3)反应⑥能够进行的原因是 。
(4)请根据上图的反应关系,总结出盐酸化学性质。(任写2点)
、 。
查看答案和解析>>
科目: 来源: 题型:填空题
生活离不开化学,化学与生活息息相关。
(1)下列生活用品中,所使用的主要材料属于金属材料的是________(填序号,下同),属于有机合成材料的是________。
(2)食物为我们提供了必需的营养物质。
①下列食物中,富含糖类的是________。
A. 花生油 B. 馒头 C. 蔬菜
②在超市中常看到“高钙奶”、“铁强化酱油”等食品,这里的“钙”和“铁”是指________(填“原子”或“元素”)。缺铁会对人体造成的影响是________(填“佝偻病”或“贫血”)。
(3)厨房中蕴藏着许多化学知识。
①我们常用洗洁精清除餐具上的油污,这是利用了它的________作用。
②小苏打在医疗上可治疗胃酸过多。写出小苏打与胃酸反应的化学方程式:
____________________________________________________。
③水壶内壁会结水垢[主要成分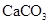 、
、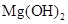 ]。下列物质能除水垢的是________。
]。下列物质能除水垢的是________。
A. 开水 B. 白醋 C. 洗洁精
(4)为了保护空气,很多公交车用“压缩天然气”作燃料。天然气的主要成分是________,其充分燃烧的化学方程式是________________________。
查看答案和解析>>
科目: 来源: 题型:填空题
(3分)食醋是一种能增强食品酸味的常用调味剂,其主要成分为醋酸(CH3COOH),它与我们的生活密切相关。请你根据所学知识,回答下列问题:
(1)食醋有酸味,因为醋酸的水溶液显____ .(填“酸性“、“中性”或“碱性”)。
(2)醋酸中,质量分数最大的元素是____ 元素。
(3)生活中,可用食醋软化鱼骨和鸡蛋壳,因为醋酸能与它们的主要成分反应,生成醋酸钙、二氧化碳和水。由此可推知鱼骨、鸡蛋壳主要成分是(填化学式)____ ____ 。
查看答案和解析>>
科目: 来源: 题型:填空题
(3分)用所学化学知识回答下列问题。
(1) 炉具清洁剂中含有一种常见的碱是 。
(2) 金刚石、石墨、C60的化学性质相似,但物理性质却有很大差异,为什么?
(3) 亚硝酸钠(NaNO2)是一种工业用盐,有剧毒,外观与食盐相似,其水溶液显碱性,食盐水溶液显中性,现有两瓶这两种物质的无色稀溶液,怎样用pH试纸把它们区分开来?
查看答案和解析>>
科目: 来源: 题型:填空题
硫酸和盐酸既是实验室常用的试剂,也是重要的化工原料。写出用稀硫酸除去铁锈的化学方程式: ; 打开盛有浓盐酸和浓硫酸试剂瓶的瓶盖,立即就能把它们区分开来,这是因为: ;将20g质量分数为98%的浓硫酸稀释为10%的硫酸,需要水的质量为 g。
查看答案和解析>>
科目: 来源: 题型:填空题
下图装置可以完成多个简单实验,具有药品用量少、实验现象明显、尾气不外逸等优点。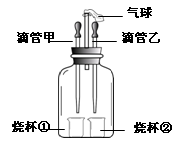
(1)若甲中吸有浓氨水,乙中吸有无色酚酞溶液,将甲、乙中的液体同时挤出,一段时间后,观察到无色酚酞溶液变红,说明分子具有的性质是________。
(2)若甲中吸有水,乙中吸有稀硫酸,烧杯①中盛有用石蕊溶液染成紫色的干燥纸花,烧杯②中盛有碳酸钠粉末。为了验证使石蕊变色的物质是碳酸而不是二氧化碳,应采取的实验操作是_______ _ 。
(3)若先将甲中的液体挤出,观察到气球明显鼓起,一段时间后恢复原状;再将乙中的液体挤出,气球又明显鼓起。请将下表中的试剂补充完整。
| | 滴管甲 | 烧杯① | 滴管乙 | 烧杯② |
| 试剂 | H2O | | | Mg |
查看答案和解析>>
科目: 来源: 题型:填空题
(6分)甲、乙、丙、丁为初中化学常见物质。由H、C、O、Cl、Na、Ca、Fe七种元素中的一种或几种组成。用下图所示装置进行实验。
(1)若A中盛有固体甲,从C放入溶液乙,打开K,观察到A中固体消失,B中有气泡冒出,则溶液乙是 。
(2)若A中盛有固体甲,从C放入液体乙,打开K,观察到B中有气泡冒出,
一段时间后,B中液面下降, 则A中发生反应的化学方程式为 。B中液面下降的原因是 。
(3)若A中盛有物质甲,从C放入溶液乙,观察到B中溶液流入A中,并出现浑浊现象, 溶液变浑浊的原因主要是(用化学方程式表示) 。
(4)若A中盛有固体甲,打开K,从C放入溶液乙,观察到B中溶液变浑浊。关闭K,B又变澄清,则此时B中溶液的溶质可能是 (写出所有可能组合)。
查看答案和解析>>
科目: 来源: 题型:填空题
“白铁皮”具有较强的耐腐蚀性,是生产中常用的金属材料之一。镀锌层犹如铁皮的保护层,这层膜的厚度是判断镀层质量的重要指标。某研究性学习小组为了测定镀锌铁皮镀锌层的厚度,设计了下面的实验方案。
(1)讨论:在铁皮表面镀锌是为了 。(填字母)
a 锌没有铁活泼,镀在铁的表面可防止生锈
b 锌比铁活泼,并且在空气中容易形成致密的氧化膜,防止生锈
(2)甲同学的方案是:如图1,将镀锌铁皮浸泡在盐酸中,先用盐酸将镀锌铁皮表面的锌反应掉,通过测量因产生气体而形成差量计算出锌的质量,然后再计算得到锌层的厚度。但是乙同学回顾起上课时老师演示的“用足量盐酸除铁锈”的实验现象,马上对甲同学的方案的可行性提出了异议,乙同学的理由是 。
(3)乙同学查阅资料:ZnCl2、FeCl2都能与NaOH溶液反应,生成难溶于水Zn(OH)2和
Fe(OH)2,而Zn(OH)2既可以溶于酸也可以溶于碱,Fe(OH)2则只能溶于酸,于是设计了如下方案:
步骤②中加入足量氢氧化钠的目的是 。
(4)丙同学设计通过测量镀锌铁皮与酸反应产生气体的体积来计算锌层的厚度,他设计了如图2所示装置。其中仪器A中盛放的是镀锌铁皮,仪器B中盛放的是稀硫酸。
①选择用稀硫酸而不用浓盐酸的原因是 。
②检查量气装置气密性:连接好装置,关闭弹簧夹,从量气管注水,若观察到 ,说明该量气装置气密性良好。
③若分液漏斗上方不连接导管a,则测出气体体积会 (选填“偏小”、“偏大”或“没有影响”)。
查看答案和解析>>
科目: 来源: 题型:填空题
(6分)化学兴趣小组的同学用如下图所示装置做中和反应实验,请按要求回答问题。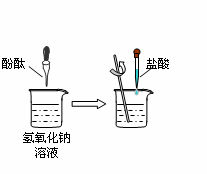
(1)向盛有氢氧化钠溶液的烧杯中滴入酚酞溶液,溶液变为红色,此时溶液的pH 7(填“>”或“<”或“=”),用胶头滴管吸取盐酸逐滴加入烧杯中,并不断用玻璃棒搅拌,当溶液刚好由红色变成 色时,恰好完全中和,停止加入盐酸,该反应的化学方程式为 。
(2)实验(1)中,某同学又多加了几滴盐酸,这时溶液显 性,此时溶液中的溶质为 。
查看答案和解析>>
科目: 来源: 题型:填空题
(4 分)建国 60 多年来,我国化学基础科学的发展,取得了举世瞩目的成就。我国科学家用滤纸和二氧化钛(TiO2)薄膜制作出一种新型“纳米纸”,又在纳米纸上“铺”一层“萘胺”(C10H9N)染料,制成一种试纸,用于检测食品中亚硝酸盐浓度的高低。
(1)二氧化钛中 Ti 的化合价为 。
(2)萘胺的一个分子中,C、H、N 三种原子的个数之比为 (填最简整数比)。
(3)已知 NaNO2 能发生如下反应(化学方程式已配平):
2NaNO2+2KI+2H2SO4=I2+2M↑+2H2O+Na2SO4+K2SO4,则 M 的化学式是 。
(4)根据上述反应,可用化学试纸及生活中常见物质进行实验来鉴别亚硝酸盐和食盐,现有碘化钾淀粉试纸,则还需选用下列生活中的常见物质为________(填序号)。
①食用油 ②白酒 ③食醋 ④牛奶
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com