
科目: 来源: 题型:探究题
人教版新课标化学教材九年级上册(2012教育部审定)“分解过氧化氢制氧气的反应中二氧化锰的催化作用”,以及“寻找新的催化剂”研究性实验,引起了化学探究小组的兴趣。
【提出问题】氧化铁能否作过氧化氢溶液分解的催化剂?如果能,其催化效果如何?
【实验探究】
| 实验步骤 | 实验现象 |
| I.分别量取5mL5%过氧化氢溶液放入A、B 两支试管中,向A试管中加入ag氧化铁粉末,并分别在A、B两支试管中插入带火星木条,观察现象。 | A试管中产生气泡,带火星木条复燃,B试管中无明显现象 |
| II.待A试管中没有现象发生时,重新加入过氧化氢溶液,并把带火星的木条伸入试管,如此反复多次试验,观察现象。 | 试管中均产生气泡,带火星木条均复燃 |
| III.将实验II中的剩余物小心过滤,并将所得滤渣进行洗涤、干燥、称量,所得固体质量仍为ag。 | |
| IV分别量取5mL5%过氧化氢溶液放入C、D 两支试管中,向C试管中加入ag氧化铁粉末,向D试管中加入ag二氧化锰粉末,观察现象。 | |

查看答案和解析>>
科目: 来源: 题型:探究题
实验是学习化学的重要手段,请阅读下列实验装置图,回答有关问题。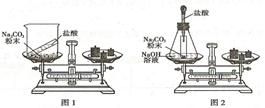
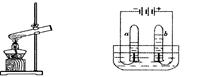
图3水蒸发实验 图4电解水实验
(1)同学们先按图1的方式实验,该实验中,大家进行了两次称量,有四个小组得到下列数据,其中有问题的两组数据是 (填序号)。
| | A | B | C | D |
| 盐酸加入Na2 CO3粉末前称量/g | 85.3 | 82.8 | 84.8 | 86.5 |
| 盐酸加入Na2 CO3粉末后称量/g | 85.3 | 80.6 | 83.2 | 87.8 |
查看答案和解析>>
科目: 来源: 题型:探究题
在化学反应前后,物质的总质量会发生变化吗?针对此问题,小王同学通过下面的实验进行探究。
[猜想假设]猜想1:化学反应前后物质的总质量增大;猜想2:化学反应前后物质的总质量 ;猜想3:化学反应前后物质的总质量 。
[设计实验]到底哪种猜想正确?小王想设计了下面的实验进行探究。
实验:用热的玻璃棒点燃白磷,使其燃烧,测定反应前后物质的质量变化。
[实验现象]白磷燃烧产生 ;气球先变大,后又变小.天平最后仍平衡。
[实验反思](1)实验中气球先变大,后又变小的原因是 。
小王根据该实验现象,再结合前面所学的碳酸钙和盐酸反应前后的质量变化情况的实验探究得出了下列结论:当用有气体参加或生成的化学反应来验证质量守恒定律时,应在 ,才能判定参加化学反应的反应物总质量和生成物总质量是否相等。
查看答案和解析>>
科目: 来源: 题型:探究题
乙炔(C2H2)气体和氧气反应能产生高温火焰,工人师傅常用氧炔焰切割或焊接金属。乙炔由碳化钙(块状固体,化学式为CaC2)与水反应生成,同时生成一种白色固体。
【查阅资料】电石主要成分为碳化钙(CaC2),它没有可燃性。
【提出问题】白色固体是什么物质?
【做出猜想】小明经过思考认为有以下几种可能:
猜想一:CaO;猜想二: ;猜想三:Ca(OH)2。
他的依据是 。
【交流反思】经过同学们交流讨论,认为猜想一不成立。否定猜想一的理由是:
。
【进行实验】
(一)取少量白色固体放入试管中,滴加稀盐酸,没有观察到 ,证明猜想二不成立。
(二)取少量白色固体加入到水中,取上层清液,通入 ,有白色浑浊出现,证明猜想三成立。该反应的化学方程式为: 。
结论:白色固体是Ca(OH)2。
【拓展应用】某市一辆满载电石的货车遇大雨引发熊熊大火,其中的可燃物是________,且该反应放出大量热,使可燃物达到_______________。
【交流反思】通过上述实验可知,电石在保存和运输时的注意事项__________________
查看答案和解析>>
科目: 来源: 题型:探究题
小明、小华、小林和小军四位位同学利用下图所示装置在实验室制取O2和CO2,并对它们的有关性质进行研究,请回答下列问题。
(1)小明同学用KMnO4固体制取O2,应选用上图中的 装置(填编号),该反应的化学方程式为 ;该反应的基本反应类型__________当O2收集满并取出集气瓶后,停止该实验的正确操作方法是__________
(2)小华同学用浓HCl(具有挥发性)与大理石在C装置中反应,制取CO2并检验其有关性质,观察到烧杯中紫色石蕊试液变红,对这一现象的解释不合理是 (填序号)。
a.产生的CO2直接使石蕊试液变红
b.产生的CO2与H2O反应生成H2CO3,使石蕊试液变红
c.挥发出的氯化氢溶于水,使石蕊试液变红
(3)小林同学用A装置制取氢气,他需要做的改动是__________________,点燃氢气前一定要_______________________。写出氢气燃烧的化学方程式__________________。
(4)小军也用A装置制取氧气,分别倒入适量的6%、15%的双氧水,再加入等量的MnO2,各收集一集气瓶气体,发现浓度大的先收集满。由此可以得出,其它条件相同时,化学反应速率与反应浓度的关系是__________________。
查看答案和解析>>
科目: 来源: 题型:探究题
将一张滤纸(组成元素为C、H、O)用FeCl3浓溶液浸润,在酒精灯上烘干后点燃,滤纸变黑、红热,最终转化为黑褐色物质。针对该黑褐色物质,甲同学认为其中含有单质铁;乙同学则认为不含单质铁。为验证各自的猜想,他们进行了如下探究:
(1)甲同学将黑褐色物质放入稀盐酸中,发现有连续的微小气泡产生。如果黑褐色物质中含有单质铁,则反应的化学方程式为 。
(2)乙同学提出疑问:(1)中实验产生的气泡也可能是滤纸碳化后吸附的空气。为此,甲同学又做了(1)中实验的对比实验: ,观察到有微小气泡产生,但很快停止。证明(1)中实验产生的连续的微小气泡是由铁与稀盐酸反应产生的。
(3)通过以上探究,乙同学赞同甲同学的观点,在甲同学的启发下,乙同学提出了另一种证明黑褐色物质中含有单质铁的方法:将黑褐色物质放入硫酸铜溶液中,观察到 现象,说明其中含有单质铁。
查看答案和解析>>
科目: 来源: 题型:探究题
为探究二氧化碳的性质,某同学设计了如图所示的实验: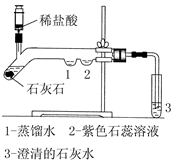
(1)写出石灰石与稀盐酸反应的化学方程式: 。
(2)用注射器注入稀盐酸,一段时间后,可观察到在1、2两处中有一处有明显的现象发生,该实验现象是 。
(3)3处的澄清石灰水变浑浊,这是由于 的缘故。
查看答案和解析>>
科目: 来源: 题型:探究题
某化学兴趣小组的同学在学完《酸和碱的中和反应》后,集体创作了一个小魔术:“变色玫瑰”——用滤纸编制的白玫瑰喷洒无色液体乙后变红,继续喷洒该液体后又变为白色。组员揭密:喷洒无色液体乙前,白玫瑰先用某无色液体甲处理过;喷洒的无色液体乙是由两种液体混合而成的;组成甲、乙两种液体的物质都是初中化学常见的物质。
(1)液体乙可能是 。
(2)液体甲中的溶剂是 。
(3)玫瑰花由红色变为白色时发生反应的化学方程式可能是 。
查看答案和解析>>
科目: 来源: 题型:探究题
某校研究性学习小组在学习了双氧水分解制氧气的实验后,知道催化剂(Mn02,)能改变化学反应速率。到底Mn02是不是该反应的催化剂以及还有哪些因素与化学反应速率有关呢?
【小组讨论】:小明同学观点:化学反应速率与反应物的质量分数有关;
小红同学观点:化学反应速率与反应温度有关;
小峰同学观点:化学反应速率与 有关。
【设计实验】:为了验证他们的观点,设计并进行了以下实验:
(1)请你写出实验中所发生的化学反应方程式 ;
(2)____实验证明小明的观点是正确的,_______实验证明小红的观点是正确的。
| A.①和② | B.②和③ | C.③和④ | D.①和④E.②和⑤ |
查看答案和解析>>
科目: 来源: 题型:探究题
同学们对美术组的环保石头纸(主要成分为碳酸钙,加入适量聚乙烯和少量胶合剂)展开探究:
[拓展实验一] 探究影响石头纸与盐酸反应快慢的因素
(1)甲、乙两同学设计实验如下:
| | 甲 | 乙 |
| 实验过程 |  |  |
| 现象 | 试管①、②、③中产生气泡快慢的顺序为: ①>②>③。 |  |
| 分析结论 | Ⅰ 碳酸钙与稀盐酸反应的化学方程式为 Ⅱ 对比甲同学实验①②可知, ,化学反应的速度越快; Ⅲ 对比甲同学实验 (填实验序号)可知,反应物的接触面积越大,反应速率越 。 Ⅳ乙同学的实验中,数据记录纸上应该连续记录的实验数据是 和 。 | |

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com