
科目: 来源: 题型:
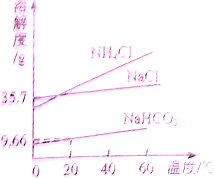 实验室模拟“侯氏制碱法”制纯碱,其原理是NaCl+NH4HCO3=NaHCO3+NH4Cl,再将碳酸氢钠加热分解得到纯碱.如图是NaCl、NH4Cl、NaHCO3的溶解度曲线,下列说法正确的是( )
实验室模拟“侯氏制碱法”制纯碱,其原理是NaCl+NH4HCO3=NaHCO3+NH4Cl,再将碳酸氢钠加热分解得到纯碱.如图是NaCl、NH4Cl、NaHCO3的溶解度曲线,下列说法正确的是( )| A、NaHCO3从溶液中分离出,可采用的操作是蒸发结晶 | B、NH4Cl饱和溶液的溶质质量分数一定大于NaCl饱和溶液的溶质质量分数 | C、40℃时,溶解度大小关系是:NH4Cl>NaCl>NaHCO3 | D、20℃时,100g水中加入11.7g NaCl和15.8g NH4HCO3固体,充分反应后,理论上可析出7.14g NaHCO3晶体 |
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
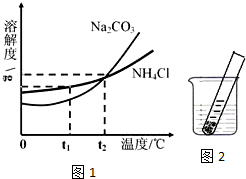 海洋是巨大的资源宝库,为人类提供了宝贵的自然资源.
海洋是巨大的资源宝库,为人类提供了宝贵的自然资源.查看答案和解析>>
科目: 来源: 题型:
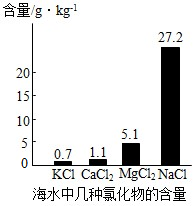 (1)从化合物分类看,KCl、CaCl2、MgCl2、NaCl属于
(1)从化合物分类看,KCl、CaCl2、MgCl2、NaCl属于查看答案和解析>>
科目: 来源: 题型:
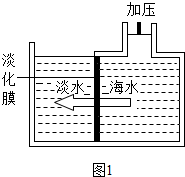 海洋中蕴含丰富的资源.
海洋中蕴含丰富的资源.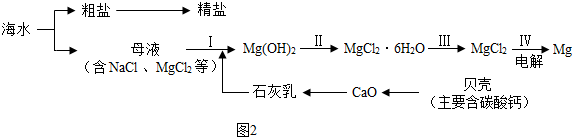
查看答案和解析>>
科目: 来源: 题型:
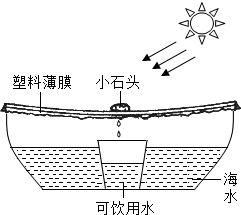 海水是种宝贵资源.
海水是种宝贵资源.| 温度(℃) | 0 | 20 | 40 | 60 | 80 |
| 溶解度(g/100g水) | 3 | 5 | 9 | 15 | 23 |
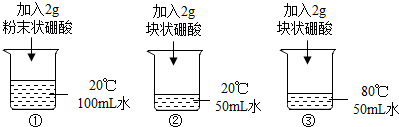
查看答案和解析>>
科目: 来源: 题型:
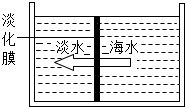 海洋是巨大的资源宝库,请你运用学过的知识回答下列问题:
海洋是巨大的资源宝库,请你运用学过的知识回答下列问题:查看答案和解析>>
科目: 来源: 题型:
| A、浩瀚的海水中蕴藏着丰富的化学资源,海水中含有80多种元素 | B、水体污染,影响工农业、渔业生产,破坏水生态系统 | C、为了节约用水,把农业和园林浇灌、浸灌改为喷灌、滴灌 | D、我国水资源丰富,人均水量居世界前列 |
查看答案和解析>>
科目: 来源: 题型:
| A、从海水中不但可提取金属镁,还可得到其他很多产品 | B、“可燃冰”是在低温、低压条件下形成的冰状固体,属于不可再生资源 | C、蒸馏法淡化海水属化学变化 | D、“可燃冰”燃烧后几乎不产生任何残渣和废弃物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com