
科目: 来源:不详 题型:填空题

查看答案和解析>>
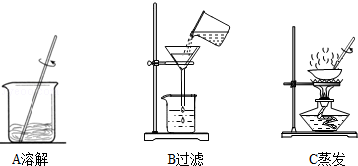
科目: 来源:不详 题型:实验题
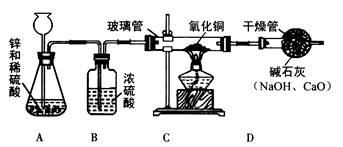
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.只含有Mg2+、SO42- |
| B.一定含有K+、Mg2+、Cl-、SO42- |
| C.一定含有Mg2+、SO42-,可能含有Cl-、K+ |
| D.一定含有Cl-、K+,可能含有Mg2+、SO42- |
查看答案和解析>>
科目: 来源:不详 题型:实验题
| | NaHCO3 | Na2CO3 |
| 加入稀盐酸 | 现象Ⅰ | 产生气泡 |
| 加入饱和石灰水 | 溶液变浑浊 | 现象Ⅱ |
| 加入CaCl2溶液 | 无明显现象 | 溶液变浑浊 |
| 加热溶液至沸腾,将气体通入澄清石灰水 | 澄清石灰水变浑浊 | 澄清石灰水无明显变化 |
| 实验步骤 | 实验现象 | |
| ①取少量样品溶于水,加入过量的CaCl2溶液。 | ; | 该反应的方程式: 。 |
| ②将上述反应后的混合液过滤,取滤液 。 | ; | 证明猜想②成立。 |
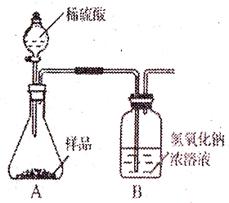 ① ;
① ;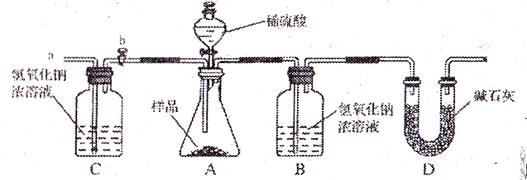
查看答案和解析>>
科目: 来源:不详 题型:实验题
| 实验 | 水的体积 | 所加物质 | 测量液体温度(℃) |
| 实验1 | 50mL | NH4Cl | 15 |
| 实验2 | 50mL | CaCl2 | 28 |
| 实验3 | X | NaCl | 21 |
| 实验4 | 50mL | 无 | 22 |
查看答案和解析>>
科目: 来源:不详 题型:实验题
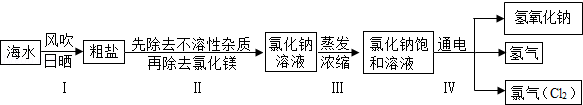
| 阴离子 阳离子 | OH﹣ | 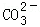 |
| Ca2+ | 微 | 不 |
| Mg2+ | 不 | 微 |
| 实验步骤 | 实验现象 | 实验结论 |
| 步骤一:取一定量的氯化钠溶液于试管中,加入适量的NaOH溶液 | 无明显现象 | 说明MgCl2 (填“已”或“未”)除尽 |
| 步骤二:往步骤一所得溶液中加入适量的 溶液 | 产生白色沉淀 | 说明溶液中含有CaCl2 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
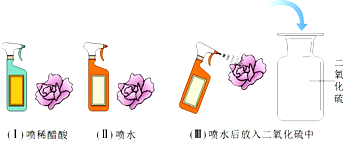
| 实验操作 | 实验现象 |
| | |
查看答案和解析>>
科目: 来源:不详 题型:实验题
| 实验操作 | 实验现象 | 结论 |
| 取白色沉淀甲,滴加足量的稀硝酸 | 沉淀部分消失 | 白色沉淀甲中一定含有 |
| 实验操作 | 实验现象 | 结论 | |
| 实验Ⅰ | 取适量无色滤液乙,加入碳酸钠溶液 | 无明显现象 | 无色滤液乙中一定不含 |
| 实验Ⅱ | 步骤①:取适量无色滤液乙,加入过量的 溶液,过滤 | 生成白色沉淀 | 原白色固体样品中一定存在该物质 |
| 步骤②:取步骤①中的滤液,滴加 溶液 | | ||
查看答案和解析>>
科目: 来源:不详 题型:实验题
| 实验步骤 | 实验现象 | 实现结论 |
 相同浓度的NiSO4 | 铁片表面有固体析出,铜片表面 . | 三种金属活动性由强到弱的顺序为 . |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com