
科目: 来源:不详 题型:填空题

| 实验中可能出现的现象 | 结论 |
| 红色粉末不变色,石灰水不变浑浊 | 假设1成立 |
| 红色粉末全部变为黑色,石灰水变浑浊 | 假设2成立 |
| | 假设3成立 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
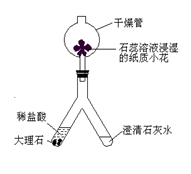
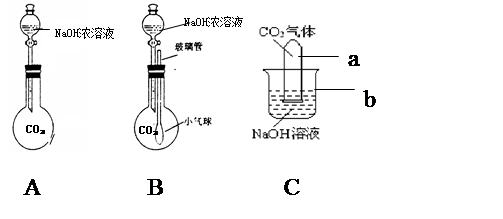
查看答案和解析>>
科目: 来源:不详 题型:实验题

| 实验步骤 | 实验现象 | 结论和化学方程式 |
| | | |
查看答案和解析>>
科目: 来源:不详 题型:实验题

查看答案和解析>>
科目: 来源:不详 题型:实验题
| 实验步骤 | 实验现象 | 结论 |
| 取少量滤液放在试管中,再滴入氯化钙溶液 | 若生成白色沉淀 | 碳酸钠过量 |
| 若无明显现象 | 恰好反应 |
| 实验步骤 | 实验现象和结论 |
| | |
| |

查看答案和解析>>
科目: 来源:不详 题型:实验题


查看答案和解析>>
科目: 来源:不详 题型:实验题

查看答案和解析>>
科目: 来源:不详 题型:实验题
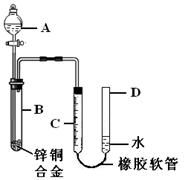
| A.反应前加入稀酸的体积 | B.反应前加入稀酸的质量分数 |
| C.实验前反应装置中空气的体积 | D.实验条件下氢气的密度 |
查看答案和解析>>
科目: 来源:不详 题型:实验题
| 性质 | NaOH | Na2CO3 | NaHCO3 |
| 溶解性 | 20℃时溶解度109g | 20℃时溶解度21.5g 溶解时放热 | 20℃时溶解度9.6 g 溶解时放热 |
| 加热 | 不分解 | 不分解 | 发生分解反应,分解产物为碳酸钠、二氧化碳和水。 |
| 实验步骤 | 实验现象 | 实验结论 | |
| 第一步:在5支试管中分别放入少量的5种白色固体,分别标上A、B、C、D、E,然后依次加入一定量的水并振荡。 | A、C、D的溶液为无色;B的溶液为浑浊;E的溶液呈蓝色。 | B是 E是 | |
| 第二步:向上述A、C、D溶液中分别滴加无色的酚酞溶液。 | 三支试管中的酚酞溶液均变红。 | 结论: | |
| 第三步: 依据右图装置,对A、B、C进行实验。 | 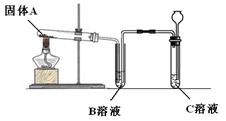 | | |
| ①加热固体A | B溶液无明显现象。 | A是Na2CO3 | |
| ②待①停止加热后,通过长颈漏斗向C溶液中加入稀盐酸 | C溶液中有气泡产生,B溶液中有气泡逸出并有白色沉淀生成。 | B溶液中发生反应的化学方程式为 | |
| 第四步:依据右图装置,对B、C进行实验。 | 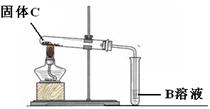 | 被加热的试管口有无色液滴生成,B溶液中有气泡逸出且溶液变浑浊。 | C是 利用排除法得出: D是NaOH |
| 实验步骤 | 实验现象和结论 |
| | |
查看答案和解析>>
科目: 来源:不详 题型:实验题

| | OH– | Cl- | CO32- | SO42- |
| Ca2+ | 微 | 溶 | 不 | 微 |
| Mg2+ | 不 | 溶 | 不 | 溶 |
| Fe3+ | 不 | 溶 | — | 溶 |
| Cu2+ | 不 | 溶 | 不 | 溶 |

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com