
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
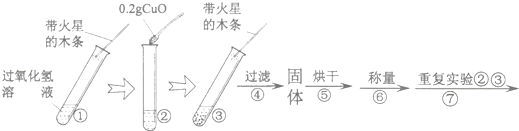
| 步骤③现象 | 步骤⑥结果 | 步骤⑦现象 | 结论 |
______ 带火星的木条复燃 | ______ | 溶液中有气泡放出 ______ | 猜想Ⅰ、Ⅱ不成立 猜想Ⅲ成立 |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
| 实验步骤 | 实验现象 | 结论 |
| ①取样于小试管中,加水,用手触摸试管外壁 | ______ | 干燥剂中含有CaO |
| ②取少量用样品制得的溶液于试管中,滴入几滴酚酞试液 | ______ | 干燥剂中含有Ca(OH)2干燥剂部分变质 |
查看答案和解析>>
科目: 来源: 题型:填空题
| 实验 操作 | 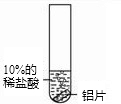 | 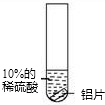 |
| 实验 现象 | 铝片表面有气泡产生 | 没有明显现象 |
| 操作步骤 (用图示说明或文字叙述均可) | 可能观察到的实验现象 | 相应的结论 |
查看答案和解析>>
科目: 来源: 题型:解答题
| 空烧杯的质量 | 实验前样品和烧杯的总质量 | 加入稀盐酸的质量 | 反应后烧杯和剩余物的总质量 |
| 100.2g | 112.2g | 50g | 157.8g |
查看答案和解析>>
科目: 来源: 题型:单选题
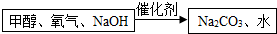
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:解答题
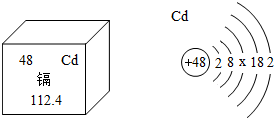 今年,广州“镉大米”事件再次引发了人们对食品安全、环境污染问题的思考.小明同学查阅了镉的相关信息:①镉元素位于第五周期ⅡB族.②镉是银白色有光泽的金属,熔点320.9℃,沸点765℃,密度8.64g/cm3,有韧性和延展性;镉在潮湿空气中缓慢氧化并失去金属光泽;镉可溶于酸,但不溶于碱.③镉对人体十分有害,摄入过量镉污染的食品和水,会引起肺和肾脏疾病.回答下列问题:
今年,广州“镉大米”事件再次引发了人们对食品安全、环境污染问题的思考.小明同学查阅了镉的相关信息:①镉元素位于第五周期ⅡB族.②镉是银白色有光泽的金属,熔点320.9℃,沸点765℃,密度8.64g/cm3,有韧性和延展性;镉在潮湿空气中缓慢氧化并失去金属光泽;镉可溶于酸,但不溶于碱.③镉对人体十分有害,摄入过量镉污染的食品和水,会引起肺和肾脏疾病.回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com