
科目: 来源: 题型:
| ||
| 实验操作 | 主要实验现象 | 实验结论及解释 | |
| ① | 检查装置的气密性.向装置中加入药品. | 装置的气密性良好. | |
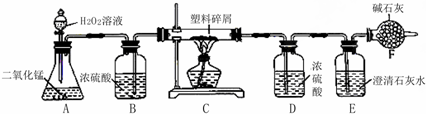
② | 打开分液漏斗活塞,向A装置中缓慢加入稀盐酸. | A装置中观察到的现象有 | C装置的作用是 |
| ③ | 一段时间后用带火星的木条在D内进行检验. | 带火星的木条复燃. | 过氧化钠与二氧化碳反应并生成氧气. |
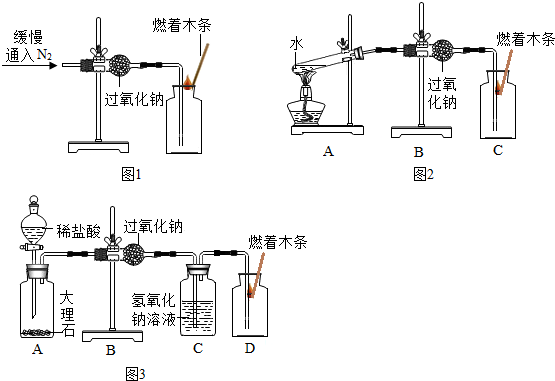
查看答案和解析>>
科目: 来源: 题型:
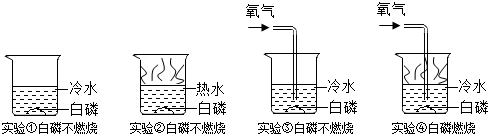
查看答案和解析>>
科目: 来源: 题型:
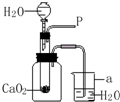 卫生部等7部委联合发布公告,禁止在面粉生产中添加过氧化钙(用作面粉增白).李明同学闻知后,对过氧化钙很感兴趣,就去买了一些回来做实验.
卫生部等7部委联合发布公告,禁止在面粉生产中添加过氧化钙(用作面粉增白).李明同学闻知后,对过氧化钙很感兴趣,就去买了一些回来做实验.查看答案和解析>>
科目: 来源: 题型:
 某化学小组利用如图所示装置(图中固定装置已略去)测定铜锌合金中锌的质量分数.探究过程如下:
某化学小组利用如图所示装置(图中固定装置已略去)测定铜锌合金中锌的质量分数.探究过程如下:查看答案和解析>>
科目: 来源: 题型:
| 验证 | 实验 | 对比实验 |
| 假设1 | 在空气中点燃蜡烛,蜡烛燃烧 | |
| 假设2 | 在空气中点燃蜡烛,蜡烛燃烧 | |
| 假设3 | 在空气中点燃蜡烛,蜡烛燃烧 |
查看答案和解析>>
科目: 来源: 题型:
| A | 食品保护的办法 | B | 燃烧与灭火实例与原理 |
| 填充氮气-防止变质 放入生石灰-防止受潮 | 油锅着火时用锅盖盖灭-隔绝空气 爆炸一定是化学变化 扑灭森林火灾时设置隔离带-隔离可燃物 | ||
| C | 日常生活物质的区别 | D | 化学中常见的“三” |
| 硬水和软水-加肥皂水并搅拌 羊毛和化纤-点燃后闻气味 | 三种可燃性气体-H2、CO、CH4 三种可加热仪器-试管、烧杯、蒸发皿 三种构成物质的粒子-分子、原子、离子 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目: 来源: 题型:
| 实验步骤 | 实验现象 | 实验结论 |
| | | 浓度越大,过氧化氢分解的速率越快 |
| | |
查看答案和解析>>
科目: 来源: 题型:
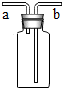 如图有多种功能,如收集气体、洗涤气体、贮存气体等.回答下列问题
如图有多种功能,如收集气体、洗涤气体、贮存气体等.回答下列问题查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com