
科目: 来源: 题型:
| A、SO2的摩尔质量是64 g |
| B、1 mol SO2中含有1 mol O2 |
| C、SO2的物质的量是指SO2的质量 |
| D、SO2中氧原子与硫原子的物质的量之比大于它们的质量比 |
查看答案和解析>>
科目: 来源: 题型:
| A、物质的量就是6.02×1023个微粒的集合体,单位是mol |
| B、物质的量是联系宏观世界和微观粒子的桥梁 |
| C、物质的量就是物质所含微粒的数量 |
| D、物质的量是国际单位制中的一个物理量,用符号“mol”表示 |
查看答案和解析>>
科目: 来源: 题型:
| 实验编号 | 实验目的 | 温度 | 催化剂 | 浓度 |
| 甲组实验Ⅰ | 探究 | 25℃ | 二氧化锰 | 10mL 2%H2O2 |
| 甲组实验Ⅱ | 25℃ | 二氧化锰 | 10mL 5%H2O2 |
| 实验步骤 | 现象 | 结论 |
| | | |
查看答案和解析>>
科目: 来源: 题型:
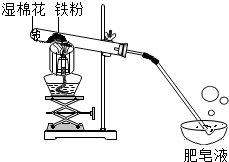 常温下没有氧气存在时,铁与水几乎不反应,但高温下,铁与水蒸气能反应生成一种常见铁的氧化物和一种气体.小明很好奇,设计如下实验探究铁粉与水蒸气反应后的产物.
常温下没有氧气存在时,铁与水几乎不反应,但高温下,铁与水蒸气能反应生成一种常见铁的氧化物和一种气体.小明很好奇,设计如下实验探究铁粉与水蒸气反应后的产物.| 常见铁的氧化物 | FeO | Fe2O3 | Fe3O4 |
| 颜色、状态 | 黑色粉末 | 红棕色粉末 | 黑色晶体 |
| 能否被磁铁吸引 | 否 | 否 | 能 |
| 能否溶于稀盐酸 | 能 | 能 | 能 |
| 实验操作 | 实验现象及结论 |
| 取少量黑色固体试管中,加入足量的稀盐酸 | 若 |
查看答案和解析>>
科目: 来源: 题型:
 甲、乙两位同学根据下列转化关系在实验室中模拟炼铁,并对生成物的成分进行探究.
甲、乙两位同学根据下列转化关系在实验室中模拟炼铁,并对生成物的成分进行探究.
| 实验方法 | 实验操作 | 实验现象 | 实验结论 |
| 物理方法 | 假设二成立 | ||
| 化学方法 | 假设二成立 |
查看答案和解析>>
科目: 来源: 题型:
| 序号 | 实验装置 | 主要实验步骤 | 实验现象 |
| 实 验 1 |  | 向两支试管中分别加入等量的甲、乙两瓶中的过氧化氢溶液,对比观察 | 两支试管中均有细微的气泡产生 |
| 实 验 2 |  | 将两个相同的蜡烛分别点燃后放入两个烧杯中,然后分别向两个烧杯中加入等量的甲、乙两瓶中的过氧化氢溶液,再向过氧化氢溶液中加入等量的二氧化锰固体 | 两烧杯内液体中均产生气泡、有白雾,两烧杯内蜡烛均继续燃烧,但加入甲瓶溶液的烧杯中,蜡烛燃烧得更明亮 |
| 实 验 3 |  | 向装有等量二氧化锰的两个锥形瓶中分别加入等量的甲、乙两瓶中的过氧化氢溶液 | 两锥形瓶内液体中均产生气泡、有白雾,同时有现象①出现 |
查看答案和解析>>
科目: 来源: 题型:
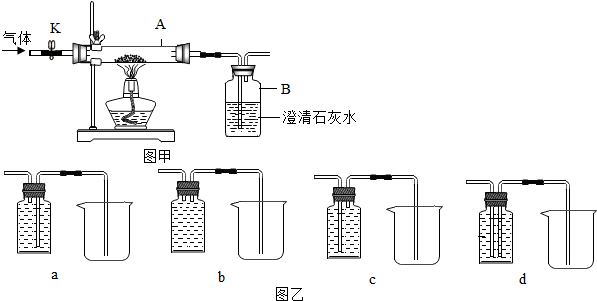
查看答案和解析>>
科目: 来源: 题型:
| 序号 | 实验装置 | 主要实验步骤 | 实验结果 |
实验1 |  | ①读取反应前电子天平的示数(m1) ②将过量的稀盐酸全部倒入烧杯中 ③待反应停止后,立即读取电子天平的示数(m2) | 测得样品纯度的平均值为93.8% |
| 实验2 |  | ①在气密性良好的装置中装入药品 ②称量反应前烧杯和烧杯中液体的质量(m3) ③迅速加入过量的稀盐酸 ④待反应停止后,立即称量烧杯和烧杯中液体的质量(m4) | 测得样品纯度的平均值为25.0% |
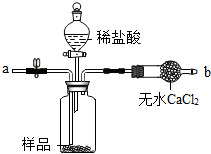
查看答案和解析>>
科目: 来源: 题型:
| 实验步骤 | 实验现象 | 实验结论及化学方程式 |
| (1)用球胆收集汽车排出气体 | -------- | -------- |
| (2)闻该气体气味 | 有刺激性气味 | 该气体中可能含有 |
| (3)将该气体通入足量澄清石灰水中 | 有白色沉淀生成 | 该气体中一定含有 |
(4) | C中新鲜血液颜色变暗;D中有红棕色气体产生 | 该气体中,除了(3)所确定的成分外,下列有关其余成分的说法一定不正确的是 ①只含NO ②只含NO2 ③只含CO ④含NO和NO2 ⑤含CO和NO2 ⑥含NO和NO2 ⑦含CO、NO和NO2 |
| (5)将(4)中C导出的气体通入 | 观察到 | 该气体中一定含有CO |
查看答案和解析>>
科目: 来源: 题型:

| A、甲实验中黄铜片能在铜片上刻画出痕迹,可以说明黄铜的硬度比铜片大 |
| B、乙实验中酚酞溶液变红,可以说明分子在不断运动 |
| C、丙实验既可以说明二氧化碳易溶于水,又可以说明二氧化碳具有酸性 |
| D、丁实验既可以说明铁能与硫酸铜反应,又可以验证质量守恒定律 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com