
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
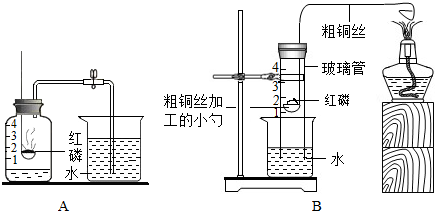
 我们已经知道空气的主要成分是氮气和氧气,如图为测定空气中氧气会含量的实验示意图.查阅资料:固体红磷跟空气中的氧气在点燃的条件下发生反应,生成固态的五氧化二磷(白色,能溶于水).化学兴趣小组的同学用如图的装置测定空气中氧气的含量.
我们已经知道空气的主要成分是氮气和氧气,如图为测定空气中氧气会含量的实验示意图.查阅资料:固体红磷跟空气中的氧气在点燃的条件下发生反应,生成固态的五氧化二磷(白色,能溶于水).化学兴趣小组的同学用如图的装置测定空气中氧气的含量.| 1 |
| 5 |
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
| A、从溶解度曲线可以知道一定温度下某个物质的溶解度 |
| B、从金属活动性顺序表可以知道金属活泼性的强弱 |
| C、一定温度下,向溶液中加入溶质都会使其浓度增大 |
| D、配平化学方程式的依据是质量守恒定律 |
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com