
科目: 来源: 题型:
| ||
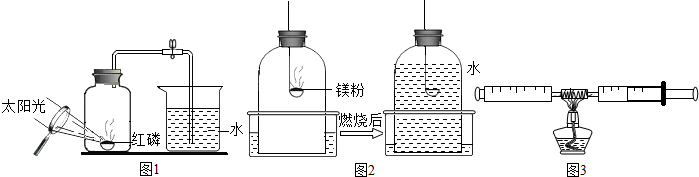
| 反应前容器内空气体积 | 反应后容器内气体体积 |
| 30mL | X mL |
查看答案和解析>>
科目: 来源: 题型:
| 实验步骤 | 实验现象 |
| Ⅰ.分别量取5mL同种浓度的双氧水放入A、B两支试管中,向A试管中加入ag水泥块,并分别在A、B两支试管中插入带火星木条,观察现象. | A试管中产生气泡,带火星木条复燃,B试管中无明显现象 |
| Ⅱ.待A试管中没有现象时,重新加入双氧水,并把带火星木条伸入试管,如此反复多次实验,观察现象. | 试管中均产生气泡,带火星木条均复燃 |
| Ⅲ.将实验Ⅱ中的剩余物小心过滤,并将所得滤渣进行洗涤、干燥、称量. | 水泥块的质量仍为ag |
查看答案和解析>>
科目: 来源: 题型:
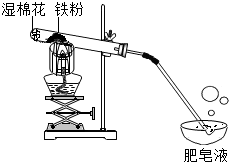 常温下没有氧气存在时,铁与水几乎不反应,但高温下,铁与水蒸气能反应生成一种常见铁的氧化物和一种气体.小明很好奇,设计如下实验探究铁粉与水蒸气反应后的产物.
常温下没有氧气存在时,铁与水几乎不反应,但高温下,铁与水蒸气能反应生成一种常见铁的氧化物和一种气体.小明很好奇,设计如下实验探究铁粉与水蒸气反应后的产物.| 常见铁的氧化物 | FeO | Fe2O3 | Fe3O4 |
| 颜色、状态 | 黑色粉末 | 红棕色粉末 | 黑色晶体 |
| 能否被磁铁吸引 | 否 | 否 | 能 |
查看答案和解析>>
科目: 来源: 题型:
| 实验编号 | 实验药品 | 分解温度(℃) |
| ① | KClO3 | 580 |
| ② | KClO3、MnO2(质量比1:1) | 350 |
| ③ | KClO3、CuO (质量比l:1) | 370 |
| ④ | KClO3、Fe2O3(质量比1:1) | 390 |
查看答案和解析>>
科目: 来源: 题型:
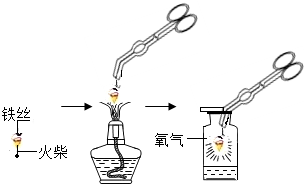 某化学兴趣小组在做“铁在氧气里燃烧”实验时,进行了一系列探究活动,请你一同参与.
某化学兴趣小组在做“铁在氧气里燃烧”实验时,进行了一系列探究活动,请你一同参与.| O2% | 90% | 70% | 60% | 55% |
| 实验现象 | 燃烧剧烈、燃烧时间长,效果好 | 燃烧比90%弱,燃烧时间短,实验成功 | 燃烧比70%弱,燃烧时间更短,实验成功 | 难以燃烧,只是发红 |
| 物质 | 纯铁丝 | 含碳0.05%的铁丝 | 含碳0.2%的铁丝 | 含碳0.6%的铁丝 |
| 燃烧时 的现象 | 无火星四射现象, 熔断 | 剧烈燃烧 极少火星 | 剧烈燃烧 少量火星 |
查看答案和解析>>
科目: 来源: 题型:
A、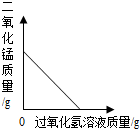 向一定量的二氧化锰中加入过氧化氢溶液 |
B、 碳在盛有氧气的密闭容器内燃烧 |
C、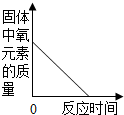 加热一定质量的高锰酸钾固体 |
D、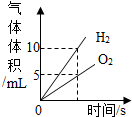 将水通电电解一段时间 |
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:

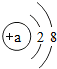 .
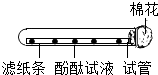
.
查看答案和解析>>
科目: 来源: 题型:
 我国化工专家侯德榜曾为世界制碱工业作出了突出贡献.“侯氏制碱法”是
我国化工专家侯德榜曾为世界制碱工业作出了突出贡献.“侯氏制碱法”是
| ||
| ||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com